калий йодноватокислый это что
Йодат калия
| Йодат калия | |
|---|---|
 | |
 | |
| Систематическое наименование | Йодат калия |
| Традиционные названия | Йодноватокислый калий |
| Хим. формула | KIO3 |
| Состояние | бесцветные кристаллы |
| Молярная масса | 214,00 г/моль |
| Плотность | 3,93 г/см³ |
| Температура | |
| • плавления | с разл. 560 °C |
| • разложения | 560 °C |
| Растворимость | |
| • в воде | 4,6 0 ; 8,1 20 ; 24,5 80 ; 32,3 100 г/100 мл |
| ГОСТ | ГОСТ 4202-75 |
| Рег. номер CAS | 7758-05-6 |
| PubChem | 24448 |
| Рег. номер EINECS | 231-831-9 |
| SMILES | |
| Кодекс Алиментариус | E917 |
| ChemSpider | 22856 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Йодат калия — неорганическое соединение, соль щелочного металла калия и йодноватой кислоты с формулой KIO3, бесцветные кристаллы, растворимые в воде.
Содержание
Получение
Физические свойства
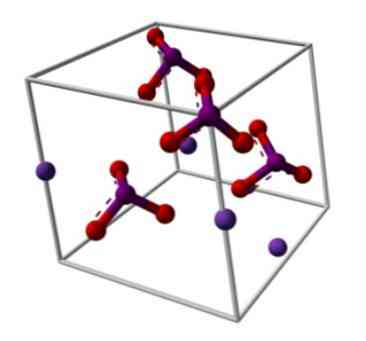
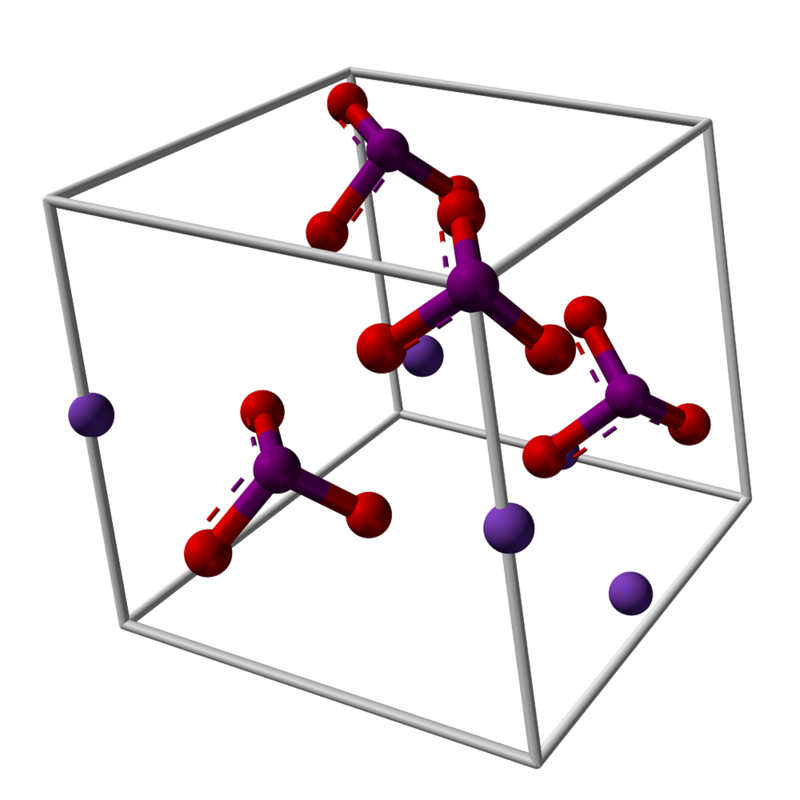
Иодат калия образует бесцветные кристаллы с выраженным полиморфизмом. В зависимости от условий выращивания образуются кристаллы похожей упаковки, но разной симметрии:
Хорошо растворяется в воде, растворы имеют нейтральную реакцию.
Не растворяется в этаноле.
Из кислых растворов кристаллизуются аддукты состава KIO3•HIO3 и KIO3•2HIO3.
Химические свойства
Йодат калия — сильный окислитель, широко применяемый в разных отраслях реактив
Йодат калия — неорганическая соль калия и йодноватой кислоты KIO3. 
Калий йодноватокислый взрывоопасен в смеси с органическими соединениями, взрывается при ударе, поэтому требует аккуратного обращения и хранения отдельно от других веществ, особенно от окисляющих и легковоспламеняющихся.
Водный раствор реагента имеет нейтральную реакцию. Сам йодат калия — сильный окислитель. Вступает в реакции с кислотами, вытесняя из них водород и образуя соответствующие соли калия.
При проглатывании вещество вызывает раздражение слизистых пищеварительного тракта. Проводить лабораторные опыты с реактивом следует в помещении с вентиляцией, в вытяжном шкафу. Хранить хим. реактив следует в сухих, крытых помещениях.
Предположения о токсичности реактива

В принципе йодат калия может причинить вред, только если его съесть очень много — гораздо больше, чем это возможно при использовании его как пищевой добавки. Тем более что сейчас для пищевой промышленности изготавливают химикат высокой чистоты. Однако то, что у специалистов есть опасения насчет токсичности этого вещества, следует знать.
Применение
Производство йодата калия относится к многотоннажному. Реактив применяется во многих сферах деятельности:
— В электротехнике используется при производстве мощных резервных источников тока, в которых катодом является смесь йодата калия с графитом.
— Применяется для очистки сточных вод, тяжелых масел, угля.
— KIO3— сильный окислитель, это свойство используется в промышленности.
— В пищевой индустрии применяется для получения иодированной соли.
— Как регулятор синтеза тироксина применяется в медицине и фармакологии. Им обязательно комплектуются наборы первой помощи при радиоактивном облучении, используется для профилактики облучения.
— Входит в состав дезинфицирующих жидкостей для ветеринарии.
— Реактив добавляют в шампуни, с его помощью избавляются от запаха «химии».
— В аналитической химии калий йодноватокислый используется в титриметрическом анализе, а также для качественного определения некоторых веществ.
— Используется в процессе золочения.
— Соль калия и йодноватой кислоты добавляется в порошкообразное сырье как антислеживающая добавка.
В «ПраймКемикалсГрупп» продаются реактивы в широком ассортименте, представлен и калий йодноватокислый «чда», а также лабораторная посуда из темного стекла, отлично подходящая для его хранения
Калий йодноватокислый это что
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
КАЛИЙ ЙОДНОВАТОКИСЛЫЙ КИСЛЫЙ
Reagents. Potassium hydrogen biiodate. Specifications
ОКП 26 2113 0430 07
1. РАЗРАБОТАН И ВНЕСЕН Министерством химической промышленности СССР
Е.П.Крысин, Л.Е.Ускова, И.Л.Ротенберг, Л.Я.Мазо, Л.3.Климова, Т.К.Палдина
2. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 04.05.71 N 842
4. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
Обозначение НТД, на который дана ссылка
Номер пункта, подпункта
3.3.1, 3.4.1, 3.5, 3.6.1, 3.8.1, 3.10.1, 3.10.4
3.4.1, 3.6.1, 3.8.1, 3.10.1, 3.10.4
3.3.1, 3.6.1, 3.8.1, 3.10.1, 3.10.4
3 3.1, 3.4.1, 3.5, 3.7, 3.8.1, 3.9, 3.10.4, 3.11.1
5. Срок действия продлен до 01.01.95; Постановлением Госстандарта СССР от 27.06.89 N 2068
6. ПЕРЕИЗДАНИЕ (август 1989 г.) с Изменениями N 1, 2, утвержденными в ноябре 1979 г., в июне 1989 г. (ИУС 11-79, 11-89)
Настоящий стандарт распространяется на кислый йодноватокислый калий, представляющий собой белый кристаллический порошок, растворимый в воде. Светочувствителен.
Формула:
(Измененная редакция, Изм. N 2).
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1а. Кислый йодноватокислый калий должен быть изготовлен в соответствии с требованиями настоящего стандарта по технологическому регламенту, утвержденному в установленном порядке.
(Введен дополнительно, Изм. N 2).
1.1. По физико-химическим показателям кислый йодноватокислый калий должен соответствовать нормам, указанным в таблице 1
Химически чистый (х. ч.) ОКП 26 2113 0433 04
Чистый для анализа (ч.д.а)
ОКП 26 2113 0432 05
Чистый (ч.)
ОКП 26 2113 0431 06
1. Массовая доля кислого йодноватокислого калия 
2. Массовая доля нерастворимых в воде веществ, %, не более
5. Массовая доля сульфатов 
8. Массовая доля тяжелых металлов 
9. Массовая доля воды, %, не более
(Измененная редакция, Изм. N 1, 2).
2. ПРАВИЛА ПРИЕМКИ
(Измененная редакция, Изм. N 2).
2.2. (Исключен, Изм. N 2).
3. МЕТОДЫ АНАЛИЗА
При взвешивании применяют весы 2-го класса точности с наибольшим пределом взвешивания 200 г и ценой деления 0,1 мг и 3-го класса точности с наибольшим пределом взвешивания 500 г или 1 кг и ценой деления 10 мг или 4-го класса точности с наибольшим пределом взвешивания 200 г и ценой деления 1 мг.
Допускается применение импортной лабораторной посуды и аппаратуры по классу точности и реактивов по качеству не ниже отечественных.
(Введен дополнительно, Изм. N 2).
3.1. Пробы отбирают по ГОСТ 3885-73. Масса средней пробы должна быть не менее 160 г.
3.2. Растворение навески препарата при нагревании следует проводить в вытяжном шкафу.
3.1, 3.2. (Измененная редакция, Изм. N 2).
3.3. Определение содержания кислого йодноватокислого калия
3.3.1. Посуда, реактивы и растворы
Колба Кн-2-250-34 ТХС по ГОСТ 25336-82.
Вода дистиллированная, не содержащая углекислоты; готовят по ГОСТ 4517-87.
Натрия гидроокись по ГОСТ 4328-77, раствор концентрации с
Спирт этиловый ректификованный технический по ГОСТ 18300-87, высшего сорта.
Фенолфталеин (индикатор), спиртовой раствор с массовой долей 1%; готовят по ГОСТ 4919.1-77.
3.3.2. Около 1,0000 г препарата помещают в колбу и растворяют в 100 см воды при нагревании. К горячему раствору прибавляют 2-3 капли раствора фенолфталеина и, не охлаждая, титруют раствором гидроокиси натрия до появления розовой окраски.
Йодоат калия свойства, структура, использование и риски
Он синтезируется путем взаимодействия гидроксида калия с йодной кислотой: HIO3(aq) + KOH (s) => KIO3(вод) + H2O (l) Кроме того, он может быть синтезирован путем взаимодействия молекулярного йода с гидроксидом калия: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).
Физико-химические свойства
Это белое твердое вещество без запаха, с мелкими кристаллами и кристаллической структурой моноклинного типа. Он имеет плотность 3,98 г / мл, молекулярную массу 214 г / моль и имеет полосы поглощения в инфракрасном (ИК) спектре..
Растворимость в воде варьируется от 4,74 г / 100 мл до 0ºC, до 32,3 г / 100 мл при 100ºC, образуя бесцветные водные растворы. Кроме того, он нерастворим в спирте и азотной кислоте, но растворим в разбавленной серной кислоте.
Его сродство к воде не заметно, что объясняет, почему он не гигроскопичен и не существует в форме гидратированных солей (KIO)3· H2O).
Окисляющий агент
Йодат калия, как указано в его химической формуле, содержит три атома кислорода. Это сильно электроотрицательный элемент, и благодаря этому свойству он «обнаруживает» электронный дефицит в облаке, окружающем йод.
Этот недостаток или вклад, в зависимости от обстоятельств, можно рассчитать как степень окисления йода (± 1, +2, +3, +5, +7), равную +5 для случая этой соли.
Следуя этому объяснению, можно определить, что йодат калия является окислительным соединением, которое сильно реагирует с восстановителями во многих окислительно-восстановительных реакциях; один из них известен как йодные часы.
Химическая структура
Но что означают эти штативы? Правильные геометрические формы этих анионов на самом деле представляют собой тригональные пирамиды, в которых атомы кислорода образуют треугольное основание, а неразделенная пара электронов в йоде указывает вверх, занимая пространство и заставляя IO-связь вниз, а две ссылки I = O.
Кристаллы этой соли могут претерпевать переходы структурной фазы (другие структуры, кроме моноклинной) вследствие различных физических условий, которые их подвергают..
Использование и применение йодата калия
Терапевтическое использование
Йодат калия обычно используется для предотвращения накопления радиоактивности в щитовидной железе в виде 131 I, когда этот изотоп используется при определении поглощения йода щитовидной железой как компонента функционирования щитовидной железы.
Кроме того, йодат калия используется в качестве местного антисептика (0,5%) при инфекциях слизистой оболочки.
Использование в промышленности
Добавляется в корм сельскохозяйственных животных в качестве йодной добавки. Поэтому в промышленности йодат калия используется для улучшения качества муки.
Аналитическое использование
В аналитической химии благодаря своей стабильности он используется в качестве основного стандарта при стандартизации стандартных растворов тиосульфата натрия (Na2S2О3), чтобы определить концентрации йода в образцах.
Йод, я2, называется с раствором Na2S2О3 для его стандартизации.
Использование в технологии лазеров
Исследования продемонстрировали и подтвердили интересные пьезоэлектрические, пироэлектрические, электрооптические, сегнетоэлектрические свойства и нелинейную оптику кристаллов KIO.3. Это приводит к огромному потенциалу в области электроники и технологии лазеров для материалов, изготовленных из этого соединения..
Риски для здоровья йодата калия
В больших дозах может вызывать раздражение слизистой оболочки полости рта, кожи, глаз и дыхательных путей.
Эксперименты по токсичности йодата калия у животных позволили заметить, что у собак, соблюдающих голодание, в дозах 0,2-0,25 г / кг массы тела, вводимых перорально, соединение вызывает рвоту.
Из-за своей окислительной способности он представляет риск возгорания при контакте с легковоспламеняющимися материалами..
Йодат калия в качестве добавки
Йодат калия (калий йодноватокислый) – это соединение неорганической этимологии, соль К и HIO3. Твердый белый рассыпчатый материал, сформированный не имеющими цвета кристаллами. Вкус – горько-кислый. Запах либо отсутствует, либо ощущается, но не сильно. В воде растворяется хорошо, растворам характерна нейтральная реакция; в этиловом спирте растворению не поддается.
Молярная масса – 214,00 г/моль, плотность – 3,93 г/см³, t плавления – 560 °C (с разложением). Формула: KIO3.
Получение возможно несколькими способами:
— окисление KI с помощью Cl2;
— окисление I2 бертолетовой солью или броматом калия;
Применение
Данное вещество находит применение в разных отраслях (гальванике, химии, косметологии, фармакологии, ветеринарии и т.д.). Одна из основных – пищепром. Здесь йодат калия выступает добавкой к пище Е917.
С его помощью, в основном, создают йодированную поваренную соль. Йодирование заключается во внесении в соль 40±15 мкг/г йода.
Также он выступает улучшителем муки и хлебобулочной продукции с окислительным воздействием. Он не дает сырью слеживаться и препятствует появлению комков, улучшает качество теста и предотвращает расплывание. Благодаря ему мякиш имеет пористую структуру, а готовые продукты – увеличенный объем.
Е917 в Украине разрешена для применения в пищевой индустрии. Ее задача – восполнение дефицита йода в организме человека с помощью еды. В разных странах ее для этого добавляют в разные продукты: сыры, колбасы, молочку и т.д. У нас же это, преимущественно, поваренная соль, йодирование которой очень важно. Ведь если норма потребления йода в сутки составляет 150 мгк, то с обычной пищей человек употребляет не более 80 мгк. А это чревато нарушениями работы щитовидки. Обычные фрукты, овощи и животноводческая продукция не всегда способны поставлять йод в нужных объемах.
Поваренная соль – лучший продукт, который стоит насыщать данной добавкой. Использование в качестве улучшителя муки может привести к увеличению суточной дозы до 2000 мкг. И если малые количества опасности не представляют, то большие чреваты следующими негативными последствиями: вред для ЖКТ, печени, почек и кровеносной системы, а также аллергические проявления.
В поваренную соль для аналогичных целей могут добавлять и йодид калия, но йодат имеет перед ним важные преимущества: не улетучивается при термообработке пищи и не влияет на ее вкус и цвет, также почти не реагирует с иными хим. составляющими соли и может сохраняться в ней до года.
Еще с помощью йодноватокислого калия промывают технологические трубопроводы на предприятиях пищевого направления.
Примечательно, что йодат калия безопасен для человека. Раньше, когда он использовался в слабо очищенном виде, еще можно было говорить о каком-то вреде. Сегодня благодаря тщательной очистке беспокоиться не о чем. Серьезное негативное влияние возможно только при регулярном употреблении этой добавки в больших объемах.
Необходим йодат калия? Есть вопросы по поводу приобретения? Обращайтесь! Наши специалисты помогут вам в этом!