кардиопротекторное действие что это такое
Кардиопротективные свойства антигипертензивных лекарственных средств
Всовременных рекомендациях по диагностике и лечению артериальной гипертензии (АГ) основная цель лечения определена как достижение максимального снижения долгосрочного риска сердечно-сосудистых осложнений (ССО).
Всовременных рекомендациях по диагностике и лечению артериальной гипертензии (АГ) основная цель лечения определена как достижение максимального снижения долгосрочного риска сердечно-сосудистых осложнений (ССО). Достичь этой цели возможно как за счет снижения повышенного артериального давления (АД), так и путем коррекции сопутствующих факторов риска. У всех пациентов с АГ следует снижать АД по меньшей мере до уровня 140/90 мм рт. ст. и ниже при хорошей переносимости.
В настоящее время основной концепцией антигипертензивной терапии является органопротекция, которая предполагает, с одной стороны, защиту органов-мишеней от повреждений, с другой — восстановление уже имеющихся в них структурных и функциональных изменений.
Если говорить о сердце как органе-мишени, то последствиями негативного воздействия на него повышенного АД являются гипертрофия миокарда левого желудочка (ЛЖ), развитие фиброза, различные варианты ремоделирования, апоптоз, что в конечном итоге повышает риск развития ССО.
На ранних стадиях артериальной гипертонии развитие гипертрофии миокарда является результатом структурной адаптации ЛЖ к повышенной нагрузке давлением. По результатам Фремингемского исследования эхокардиографические признаки гипертрофии миокарда ЛЖ были отмечены у 5–49% женщин и у 8–33% мужчин в возрасте от 30 до 70 лет. Степень гипертрофии ЛЖ определяют наследственные и конституциональные факторы (пол, возраст), факторы питания (избыточный вес, чувствительность к соли), а также состояние симпатической нервной и ренин-ангиотензин-альдостероновой (РААС) систем. Результаты многочисленных клинических исследований показали, что гипертрофия миокарда является независимым фактором риска развития ССО, таких как стенокардия напряжения, аритмия, инфаркт миокарда и сердечная недостаточность.
Гипертрофия миокарда ЛЖ (ГМЛЖ) приводит к нарушению функциональных свойств миокарда, причем в первую очередь нарушается его диастолическое наполнение, а затем и систолическая функция. При ГМЛЖ нарушается коронарное кровообращение, что проявляется снижением коронарного резерва и недостаточной перфузией субэндокардиальных слоев миокарда. При наличии ГМЛЖ частота желудочковых аритмий также повышается.
Риск развития коронарной недостаточности, желудочковых нарушений ритма сердца при увеличении массы миокарда левого желудочка на 50% возрастает по меньшей мере вдвое.
Было отмечено, что в группе с выраженной гипертрофией ЛЖ риск сердечной недостаточности возрастает в 5 раз. У 30–40% больных с признаками сердечной недостаточности отмечается нормальное состояние систолической функции, т. к. на ранних стадиях гипертрофического ремоделирования возникают прежде всего нарушения диастолического наполнения ЛЖ и признаки диастолической дисфункции. Таким образом, у больных АГ диастолическая дисфункция является самостоятельным фактором развития сердечной недостаточности. Говоря о кардиопротективных свойствах лекарственных средств (ЛС), мы в первую очередь оцениваем их влияние на ГМЛЖ.
Ретроспективный анализ клинических исследований показал, что антигипертензивная терапия, уменьшающая ГМЛЖ, позволяет добиться снижения риска ССО.
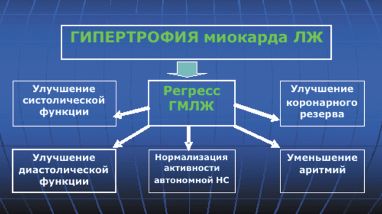
К чему приведет снижение массы миокарда ЛЖ в результате приема антигипертензивных ЛС? В настоящее время доказано, что регресс ГМЛЖ сопровождается улучшением систолической функции, уменьшением миокардиального фиброза и улучшением диастолической функции ЛЖ, увеличением коронарного резерва, нормализацией локальной нервной системы и уменьшением аритмий, что в конечном счете может снизить риск ССО и улучшить прогноз (рис. 1).
Поэтому, говоря о «кардиопротективности» применительно к антигипертензивным ЛС, мы предполагаем не только способность ЛС снижать ГМЛЖ, но и их способность влиять на жесткие конечные точки, такие как сердечно-сосудистая смертность и другие показатели сердечно-сосудистого риска.
Поскольку пусковым фактором развития ГМЛЖ является повышенное АД, следует предположить, что любой антигипертензивный препарат способен вызывать регресс ГМЛЖ.
В настоящее время вопрос о влиянии различных антигипертензивных ЛС на процессы гипертрофического ремоделирования миокарда ЛЖ остается в центре внимания. В 90-х годах был опубликован ряд обзоров клинических исследований, сравнивающих эффективность различных групп антигипертензивных препаратов на степень регресса ГМЛЖ. Авторы четырех наиболее крупных метаанализов, в которых проводилось сравнение разных групп препаратов по способности вызывать регресс гипертрофии ЛЖ, пришли к согласованному заключению — наиболее эффективно уменьшают ГМЛЖ препараты, снижающие активность РААС, — на 11,8–15% от исходного уровня.
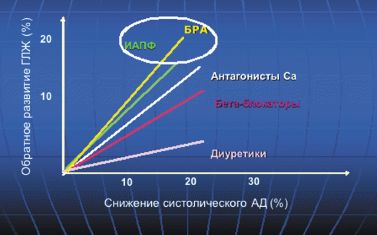
В работе Klingbeil и соавт. (метаанализ 80 двойных слепых клинических исследований) также показано, что наибольшая степень снижения индекса массы миокарда ЛЖ на 13% была отмечена у больных, получавших терапию блокаторами рецепторов ангиотензина (БРА), на 11% — антагонистами кальция пролонгированного действия (АК), на 10% — ингибиторами ангиотензин-превращающего фермента (АПФ), на 8% — диуретиками, на 6% — бета-адреноблокаторами (БАБ) (рис. 2).
Таким образом, лидирующие позиции в этом списке также занимают блокаторы ренин-ангиотензиновой системы — ингибиторы АПФ и БРА, что свидетельствует о высокой роли активации ангиотензиновых рецепторов 1 типа в процессах развития гипертрофии миокарда ЛЖ.
Ингибиторы АПФ и блокаторы рецепторов ангиотензина
Кардиопротективные свойства ингибиторов АПФ и БРА заключаются не только в их способности вызывать регресс гипертрофии миокарда ЛЖ за счет блокады компонентов циркулирующей и тканевой РААС. Потенциальные кардиопротективные эффекты, такие как антиишемическое и антиаритмическое действие, связаны с возможностью этих препаратов восстанавливать нарушенную функцию эндотелия, стимулировать высвобождение оксида азота и простациклина за счет снижения деградации брадикинина, уменьшать потребность миокарда в кислороде за счет регрессии гипертрофии миокарда, снижать активность симпато-адреналовой системы, обусловленной стимуляцией ангиотензина II.
Нами были изучены долгосрочные эффекты различных ингибиторов АПФ и БРА на процессы ремоделирования у больных АГ. Было выявлено достоверное снижение показателей ГМЛЖ на фоне длительной (до трех лет) терапии ингибиторами АПФ эналаприлом, рамиприлом и каптоприлом и БРА ирбесартаном и телмисартаном (рис. 3). Динамика снижения показателей суточного мониторирования АД за период наблюдения была однонаправленной и достоверно значимой при лечении всеми препаратами. При анализе динамики снижения индекса массы миокарда ЛЖ было отмечено более выраженное достоверно значимое снижение данного показателя в группе больных, получавших терапию БРА, что согласуется с данными ряда других исследований.
Особого внимания заслуживают антиишемические свойства ингибиторов АПФ, которые были подтверждены рядом клинических исследований. Так, в исследовании HOPE (Heart Outcomes prevention evaluation study) с рамиприлом (ингибитор АПФ с высокой аффинностью к тканевой АПФ) было включено 9297 больных старше 55 лет с высоким риском ССО. Через 4,5 года наблюдения было отмечено достоверное снижение риска развития острого инфаркта миокарда, инсульта и коронарных событий, требующих проведения реваскуляризации, — то есть тех осложнений, которые являются привычными «спутниками» прогрессирующего атеросклеротического процесса. Результаты этого исследования еще раз подтвердили обоснованность и правомочность концепции, согласно которой предупреждение сердечно-сосудистой заболеваемости и смертности возможно путем блокады РААС на тканевом уровне.
Клиническое изучение антиишемических свойств ингибиторов АПФ у больных АГ в сочетании с ишемической болезнью сердца (ИБС), стабильной стенокардией напряжения было проведено на нашей кафедре. Под влиянием лечения периндоприлом и эналаприлом у больных АГ в сочетании с ИБС, стабильной стенокардией напряжения хорошая антигипертензивная эффективность сочеталась с антиангинальным эффектом и положительной динамикой показателей теста с физической нагрузкой. У больных, получавших терапию периндоприлом, отмечено также снижение суммарной продолжительности эпизодов ишемии миокарда (по результатам Холтеровского мониторования ЭКГ), уменьшение проявлений дисфункции эндотелия, улучшение диастолической функции миокарда у больных с нарушениями релаксации, а также улучшение локальной сократимости миокарда в виде уменьшения количества гипокинетичных сегментов как в покое, так и на высоте физической нагрузки (в условиях проведения стресс-ЭХО-КГ).
В последние годы стали широко доступны результаты крупных многоцентровых клинических исследований, посвященных изучению различных аспектов кардиопротекции относительно нового класса антигипертензивных ЛС — блокаторов рецепторов ангиотензина II. Так, в клиническом исследовании LIFE (Losartan Intervention For Endpoint reduction in hypertension) кардиопротективные свойства лозартана оценивались у 9193 больных АГ с ГМЛЖ по амплитудным критериям ЭКГ. Больные были разделены на группы лечения лозартаном или атенололом. В случае недостаточного контроля АД к терапии добавляли гидрохлортиазид. Длительность лечения составила в среднем 4,8 года. Между группами не было различий по исходным показателям АД и степени снижения АД на фоне активного лечения. В группе больных, получавших лозартан, было отмечено более выраженное снижение количественных признаков гипертрофии миокарда, чем в группе атенолола. Риск развития ССО был на 13% меньше в группе лозартана (23,8 событий на 1000 больных в год), чем в группе атенолола (27,9 событий на 1000 больных в год). Смертность ССО в группе лозартана была недостоверно ниже.
В рандомизированном двойном слепом исследовании CATCH (Candesartan Assessment in the Treatment of Cardiac Hypertrophy) было проведено сравнение эффективности кандесартана (8–16 мг/сут) и эналаприла (10–20 мг/сут) у больных АГ с ГМЛЖ (по данным ЭХО-КГ — индекс массы миокарда ЛЖ (ИММЛЖ) > 100 г/м 2 у женщин и > 120 г/м2 у мужчин). Длительность наблюдения составила 1 год. В обеих группах отмечалось достоверное снижение ИММЛЖ (10,9 ± 15,5% и 8,4 ± 17,4%, p 2 у больных, получавших комбинированную терапию. У больных, получавших монотерапию эналаприлом, снижение данного показателя составило 3,9 ± 23,9 г/м 2 (p
Витамины для сердца: список лучших
Витамины для сердца (кардиотрофические препараты) одна из наиболее распространенных групп препаратов в детской и взрослой кардиологии. Механизм действия данных препаратов очень разнообразен и направлен на различные этапы развития болезни.
Метаболические препараты, они же витамины для сердца, применяются при различных заболеваниях, таких как: ревматизм, кардиты, кардиомиопатии, ИБС, миокардиодистрофии или вторичные кардиопатии. Они также используются при лечении нарушений ритма сердца, таких как: наджелудочковые и желудочковые экстрасистолии, блокады ножек пучка Гисса, пароксизмальные тахикардии, нарушения реполяризации и прочее.
Данная группа препаратов применяется также и в спорте с целью коррекции нарушений сердечно-сосудистой системы, вызванных интенсивной физической нагрузкой. Эти нарушения зачастую имеют и свое название – «спортивное сердце».
Название данных заболеваний могут вам показаться незнакомыми, но они вас могут знать вас. По распространенности заболевания сердечно-сосудистой системы занимают первое место. Отсюда становится понятно, что и распространенность препаратов для лечения сердца и сосудов очень велика. Прежде чем перейти к списку лучших витаминов для сердца, необходимо разобраться на что они влияют и как оказывают благоприятный эффект для сердца.

Как витамины влияют на сердце
Механизм действия витаминов для сердца:
Препараты для сердца, которые можно считать лучшими
А теперь можно ознакомиться с лучшими кардиотрофическими препаратами (витаминах для сердца):
Данные препараты назначаются курсом, чаще всего, не менее 1 месяца. В ряде случаев используется ступенчатая терапия ( переход с внутривенного или внутримышечного пути введения лекарственного средства на обычный прием в виде таблеток). Режим дозирования и длительность терапии в каждом случае индивидуальны и назначаются лечащим врачом с учетом данных обследований.
Данные препараты назначаются курсом, чаще всего, не менее 1 месяца. Перед применением проконсультируйтесь у специалиста.
Берегите сердце
Человек представляет собой организм, который состоит из различных систем. Одной из самых уязвимых является сердечно-сосудистая система. Появление таких симптомов, как усталость, вялость, сердцебиение, одышка, колющие боли в грудной клетке, бледность или синюшность кожи может указывать на патологию со стороны сердечно-сосудистой системы и требует незамедлительной консультации врача-кардиолога.
Только после проведения дополнительных лабораторных и инструментальных методов исследования (ЭКГ, ЭхоКГ, Холтер ЭКГ, АД; тредмилл-тест, тилт-тест и т.д.) выставляется окончательный диагноз и назначается лечение. Витамины для сердца являются лишь частью лечения и применяются в составе комплексной терапии для лечения заболеваний.
Кардиопротекция у пациентов с высоким сердечно-сосудистым риском
Определение и виды кардиопротекторов, критерии кардиозащитного действия, ишемическая болезнь сердца, применение антигипоксантов (триметазидин, мельдоний).
Эта статья в формате видеолекции здесь.
Данная статья посвящена теме метаболической терапии при различных ишемических состояниях и также широко рассматривается на наших курсах повышения квалификации по терапии, кардиологии и функциональной диагностике.
В соответствии с рекомендациями Европейского общества кардиологов (ESC) к категории пациентов высокого и очень высокого суммарного риска развития смертельных сердечно-сосудистых событий относятся:
— пациенты с систолическим артериальным давлением (САД) более 180 мм.рт.ст. и/или диастолическим артериальным давлением (ДАД) более 110 мм.рт.ст.;
— пациенты с САД более 160 мм.рт.ст. и низким ДАД (менее 70 мм.рт.ст.); больные с сахарным диабетом (СД) 2-го типа; больные метаболическим синдромом;
— пациенты с тремя факторами риска и более;
— лица с одним или более субклиническим органным повреждением (гипертрофия левого желудочка (ГЛЖ), подтвержденная на ЭКГ и ЭхоКГ, утолщение комплекса интима-медиа или атеросклеротическая бляшка по данным ультрасонографии, повышение уровня сывороточного креатинина, снижение клубочковой фильтрации (СКФ) или клиренса креатинина, микроальбуминурия (МАУ) или протеинурия);
— пациенты с уже имеющимся подтвержденным сердечно-сосудистым
заболеванием, в том числе с анамнезом перенесенного острого коронарного синдрома (ОКС).
В течение первых 9-12 месяцев после перенесенного ОКС у больных сохраняется:
— высокий уровень активности тромбоцитов, выделяющих тромбоксан А, что способствует повышенному образованию тромбина;
— инфильтрация атеросклеротических бляшек воспалительными клетками (макрофагами, Т-лимфоцитами);
— повышенное разрушение коллагена и других компонентов соединительной ткани в месте разрыва атеросклеротической бляшки (длительное незаживление дефекта);
— усиленная констрикторная активность сосуда в области стеноза.
Все это обуславливает наиболее высокий риск повторного ОКС и острого инфаркта миокарда или инсульта именно в этот период времени!
Дополнительное повышение риска ишемических осложнений ассоциировано с:
— пожилым возрастом;
— привычными интоксикациями;
— ранее перенесенными сосудистыми катастрофами;
— тяжестью сопутствующей патологии: сахарный диабет (СД), анемия, хроническая болезнь почек (ХБП).
Согласно точкам приложения, КПр делятся на:
1. моделирующие функцию клеточной мембраны: антагонисты кальция.
2. стабилизирующие клеточные мембраны митохондрий, лизосом: мельдоний, токоферол, препараты супероксиддисмутазы, церулоплазмин, триметазидин, фосфокреатин.
3. влияющие на обмен веществ за счет сохранения пула креатинфосфата (КФ), увеличения содержания АТФ, вследствие угнетения окисления жирных кислот и использования в качестве источника энергии глюкозы: мельдоний, триметазидин, L-карнитин, фосфокреатин, никотиновая кислота, инсулин.
Источником энергии в организме является глюкоза (гликоген) и жирные кислоты. Существует прямая зависимость между концентрацией жирных кислот в организме и развитием внезапной смерти. Высокие концентрации жирных кислот блокируют в клетках кальциевый, натриевый и калиевый насосы, а также АТФ насос.
Триметазидин безопасен у подавляющего большинства больных, не влияет на гемодинамику и при этом значимо улучшает переносимость ишемии, способствует уменьшению частоты ангинозных приступов; повышает толерантность к физическим нагрузкам, улучшает сократительную способность миокарда. Имеются данные положительного влияния данного препарата после перенесенного инфаркта миокарда на снижение смертности и предупреждение сердечно-сосудистых осложнений, в том числе повторных ОКС, реваскуляризаций и госпитализаций.
Все перечисленное отразилось на включении триметазидина в международные и отечественные рекомендации по ведению больных: стабильной ишемической болезнью сердца (класс рекомендации IIb, уровень доказательности – В); хронической сердечной недостаточностью (класс рекомендации IIb, уровень доказательности – А); подвергшихся коронарному шунтированию; перенесенным инфарктом миокарда.
В качестве вторичной профилактики сердечно-сосудистых заболеваний в список препаратов метаболического действия включен мельдоний, обладающий антиангинальными и вазопротекторными эффектами, а также способностью улучшать когнитивные функции.
Согласно официальным инструкциям, к лекарственным препаратам, содержащим в своем составе мельдония дигидрат, он может применяться при стенокардии, инфаркте миокарда, хронической сердечной недостаточности, дисгормональной кардиомиопатии, при острых и хронических нарушениях мозгового кровообращения (инсульты и цереброваскулярная недостаточность), при пониженной работоспособности и физическом перенапряжении (в том числе у спортсменов), в послеоперационный период для ускорения реабилитации, при синдроме абстиненции при хроническом алкоголизме (в комбинации со специфической терапией алкоголизма).
В клинической практике длительное использование мельдония показало, что он обладает выраженным антиишемическим и антиангинальным действием у широкого круга пациентов с ИБС.
Мельдоний оказывает кардиопротективное действие как в условиях острой, так и при хронической ишемии. Оптимизируя метаболизм кардиомиоцитов, мельдоний обладает не только антиангинальным действием, но и способствует жизнеспособности и функциональной активности хронически ишемизированного миокарда. Его прием в комплексном лечении ИБС уменьшает частоту приступов стенокардии в среднем на 55,6%, а потребность в нитроглицерине на 55,1%, достоверно увеличивая толерантность пациентов к физической нагрузке на 28,7%, с улучшением качества жизни на 27,8%. Это может быть отнесено к лицам молодого и пожилого возраста, а также пациентам, страдающим СД и имеющим болевую и безболевую ишемию.
Включение мельдония в период постгоспитальной реабилитации острого инфаркта миокарда ускоряет восстановление физической толерантности и оказывает позитивное влияние на состояние параметров систолодиастолической функции левого желудочка. Мельдоний обладает антитромбоцитарным действием: ингибируя агрегацию и адгезивную активность тромбоцитов, препятствует росту внутрикоронарного тромбоцитарного тромба, ингибирует вход кальция в тромбоциты и подавляет высвобождение серотонина из тромбоцитов, частично принимает участие в ингибировании образования из каскада арахидоновой кислоты тромбоксана А2, изменяет текучесть мембраны эритроцитов и тромбоцитов.
Мельдоний не влияет на параметры гемодинамики, его механизм действия в корне отличается от механизмов, на которые воздействуют антиангинальные препараты с гемодинамическими эффектами. Это позволяет эффективно использовать комбинацию мельдония с другими антиангинальными препаратами и получать синергистические защитные эффекты.
Принимая во внимание результаты проведенных исследований, а также различные точки приложения и механизмы действия данных кардиопротекторов, рационально использовать комбинированную кардиопротекцию с целью увеличения эффективности общего действия терапии.
Выводы:
У коморбидных пациентов высокого сердечно-сосудистого риска, перенесших острый коронарный синдром, раннее добавление к триметазидину вспомогательных кардиопротекторов с их последующим курсовым приемом (предпочтительнее мельдоний) в дополнение к комплексной терапии ишемической болезни сердца безопасно в отношении гемодинамических параметров и способствует:
— улучшению прогноза больных, потенциированию снижения частоты рецидива коронарных событий и госпитализаций по поводу декомпенсации кардиоваскулярной патологии в первый год после пересенной коронарной «катастрофы»;
— улучшению качества жизни больных, облегчению клинического течения ИБС, снижению частоты развития эпизодов стенокардии и ее эквивалентов, снижению потребности в органических нитратах;
— повышению результативности медицинской реабилитации, профилактике хронической сердечной недостаточности и уменьшению частоты осложнений (в том числе аритмий) в постинфарктном периоде.
Кардиопротекторы. Недооцененные возможности
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Длительный и тщательный отбор терапии ишемической болезни сердца, сопровождающийся многочисленными рандомизированными исследованиями во всех странах мира, позволил четко определить стратегию и тактику лечения, что было зафиксировано в рекомендациях Европейского общества кардиологов. Стратегические цели лечения стабильной стенокардии (СС) как одной из форм ИБС во временном интервале подразделяются на ближайшие и отдаленные. Ближайшая цель лечения заключается в достижении антиангинального эффекта. Задачи более отдаленные включают улучшение прогноза заболевания, предупреждение развития осложнений, инфаркта миокарда, внезапной смерти, увеличение продолжительности жизни и улучшение ее качества.
Тактика подбора медикаментозной терапии поэтапная, напрямую зависит от индивидуальных особенностей пациента, течения процесса, совокупности сопутствующих заболеваний и эффективности назначенной группы препаратов. Рекомендации приняты Европейским обществом кардиологов в 2006 г.
Рекомендации по антиангинальной и/или противоишемической терапии
у больных СС (ЕОК, 2006 г.)
1. Короткодействующий нитроглицерин для купирования стенокардии и ситуационной профилактики (пациенты должны получить адекватные инструкции по применению нитроглицерина) (В).
2. Оценить эффективность b –блокаторов и титровать их дозу до максимальной терапевтической, оценить целесообразность применения длительно действующих препаратов (А).
3. При плохой переносимости или низкой эффективности b –блокаторов назначить монотерапию антагонистами кальция (А), длительно действующими нитратами (С).
4. Если монотерапия b –блокаторами недостаточно эффективна, добавить дигидропиридиновый антагонист кальция (В).
1. При плохой переносимости b –блокатора назначить ингибитор if–каналов синусового узла – ивабрадин (В).
2. Если монотерапия антагонистами кальция или комбинированная терапия антагонистами кальция и b –блокаторами оказывается неэффективной, заменить антагонист кальция на пролонгированный нитрат. Избегать развития толерантности к нитратам (С).
1. Препараты метаболического действия могут быть использованы в дополнение к стандартным средствам или в качестве альтернативы им при плохой переносимости (В).
Рекомендации по фармакотерапии, улучшающей прогноз у больных СС (ЕОК, 2006 г.)
1. Ацетилсалициловая кислота (АСК) в дозировке 75 мг/сут. у всех больных при отсутствии противопоказаний (активное желудочно–кишечное кровотечение, аллергия на АСК или ее непереносимость) (А).
2. Статины у всех больных с коронарной болезнью сердца (А).
3. Ингибиторы АПФ при наличии артериальной гипертонии, сердечной недостаточности, дисфункции левого желудочка, перенесенного инфаркта миокарда с дисфункцией левого желудочка или сахарного диабета (А).
4. b –блокаторы внутрь больным после инфаркта миокарда в анамнезе или с сердечной недостаточностью (А).
1. иАПФ у всех больных со стенокардией и подтвержденным диагнозом коронарной болезни.
2. Клопидогрел как альтернатива АСК у больных, которые не могут принимать АСК, например, из–за аллергии.
3. Статины в высоких дозах при наличии высокого риска (сердечно–сосудистая смертность 2% в год) у больных с доказанной коронарной болезнью сердца.
1. Фибраты при низком уровне ЛПВП или высоком содержании ТГ у больных сахарным диабетом или при метаболическом синдроме.
Анализ групп препаратов, перечисленных в представленных выше рекомендациях, выявляет отсутствие в них лекарственных веществ, восстанавливающих метаболические процессы в поврежденном миокарде. Речь идет о группе кардиопротекторов. Но, т.к. отрицать изменения кардиомиоцитов при ишемии миокарда невозможно, значит, и попытка защитить и нормализовать функцию клеток продолжает являться актуальной и востребованной задачей. Интерес к разработке таких препаратов не стихает и, наоборот, набирает новую силу.
Объяснение необходимости разработок в данном направлении кроется в механизмах метаболизма клеток миокарда в физиологических условиях и в периоды ишемического воздействия.
В норме энергетическое обеспечение (образование АТФ) кардиомиоцита осуществляется за счет расщепления 2 главных клеточных субстратов – углеводов (глюкозы) и жирных кислот (ЖК). За счет b –окисления ЖК образуется около 60–70% АТФ, однако для этого требуется большое количество кислорода. Остальная часть АТФ синтезируется за счет молочной кислоты (лактата). Конечными продуктами катаболизма глюкозы являются углекислый газ и вода, а также большое количество энергии, аккумулированной в молекулах АТФ.
При дефиците О 2 в условиях временной или постоянной ишемии миокарда метаболизм глюкозы заканчивается на этапе пирувата, что сопровождается снижением выработки энергии примерно в 20 раз. Кроме того, формируется метаболический ацидоз, приводящий к повышению внутриклеточной концентрации ионов кальция и натрия. Усугубляет ситуацию конкурентное в условиях ишемии b –окисление ЖК, исходом, которого является внутриклеточный ацидоз и еще большее накопление натрия и кальция. Возникающие диспропорции, в конечном счете, и приводят к снижению сократимости миокарда и дальнейшему прогрессированию заболевания.
В группу «кардиопротекторов» включены лекарственные вещества, способные влиять на:
1. клеточный метаболизм;
2. ионный гомеостаз;
3. структуру и функцию мембран клеток, препятствуя развитию необратимого их повреждения и реперфузии.
Рассмотрение фармакологических свойств различных групп медикаментозных препаратов позволяет сделать вывод о влиянии как минимум на один из вышеозначенных пунктов веществ, используемых с целью получения антиангинального или противоишемического эффекта.
Совокупность данных позволила выделить 2 группы препаратов с кардиопротекторными свойствами: прямого действия (уменьшают выраженность влияния экзо– и эндогенных факторов непосредственно на кардиомиоциты в норме и при патологии сердечной мышцы) и непрямого (уменьшают нагрузку на сердечную мышцу, снижая таким образом вероятность развития или предупреждая нарушения метаболизма в сердечной мышце, влияя на другие органы и системы). Дополнительными градациями в группе прямых кардиопротекторов является разделение по основным точкам приложения их действия: моделирующие функцию клеточной мембраны, стабилизирующие клеточные мембраны, влияющие на обмен веществ в миокарде. Примером воздействия лекарственных средств, моделирующих функцию клеточных мембран, являются препараты группы антагонистов кальция. Стабилизация клеточных мембран происходит за счет уменьшения интенсивности перекисного окисления липидов, что способствует более эффективному использованию углеводов в качестве источника энергии, стабилизации мембран митохондрий, лизосом. Перечень препаратов данной группы включает: мельдоний, токоферол, препараты супероксиддисмутазы, церулоплазмин, триметазидин, фосфокреатинин.
Лекарственные средства, влияющие на обмен веществ в миокарде, проявляют свое влияние за счет сохранения в миокарде пула креатинфосфата, повышения содержания АТФ вследствие угнетения окисления жирных кислот и использования в качестве источника энергии глюкозы. Примерами таких препаратов могут служить: мельдоний, триметазидин, L–карнитин, никотиновая кислота, инсулин.
Перечень непрямых кардиопротекторов достаточно объемен: антигипертензивные средства различного механизма действия, средства, влияющие на реологические свойства крови, препараты, влияющие на липидный обмен.
Другими, несомненно, положительными, эффектами являются низкая токсичность и адаптогенный эффект, что проявляется в усилении неспецифической резистентности организма.
Мельдоний снижает концентрацию ацилкарнитина и карнитина, ограничивает транспорт и накопление в митохондриях активированных жирных кислот и способствует ускорению их b –окисления. Уменьшается очаг некроза, происходит расширение периферических и венечных сосудов.
Дальнейшие разработки препаратов группы кардиопротекторов также демонстрируют оптимистические результаты. Примером может служить препарат Кардионат (МНН: мельдоний). Механизм действия основан на воздействии непосредственно на мембрану кардиомиоцита и на метаболизм клетки, что позволяет отнести его к группе прямых кардиопротекторов.
В НИИ кардиологии Томского научного центра СО РАМН изучено влияние 4–недельной терапии Кардионатом на эффективность антиангинальной и антиишемической терапии, качество жизни и физическую толерантность у 30 больных ИБС в сочетании с артериальной гипертензией и сахарным диабетом 2–го типа. Средний возраст пациентов составил 56,5±3,4 года (от 41 года до 68 лет). Длительность стенокардии достигала 64,3±24,3 мес. Диагноз ИБС был верифицирован методом коронаровентрикулографии (сужение одной и/или более коронарных артерий более 70%), наличием в анамнезе перенесенного инфаркта миокарда давностью 6 и более месяцев, наличием клинических проявлений коронарной недостаточности. Добавление Кардионата (250 мг 4 раза/сут.) к стандартной антиангинальной терапии привело к достоверному уменьшению количества ангинальных приступов на 55,6%, при этом суточная потребность в нитроглицерине достоверно снизилась на 55,1%. Также у больных отмечено снижение функционального класса стенокардии. Данные велоэргометрии выявили достоверное увеличение толерантности к физической нагрузке на 28,7%, примерно на такую же величину улучшилось качество жизни 27,8%. Только у 2 больных (6,6%) на фоне приема препарата отмечено сердцебиение, которое купировалось самостоятельно и не требовало отмены препарата.
С большой долей уверенности можно говорить о необходимости более широкого применения препаратов группы кардиопротекторов в курсовой терапии ИБС.