катализатор ускоряет химическую реакцию а что ее замедляет
Скорость химической реакции
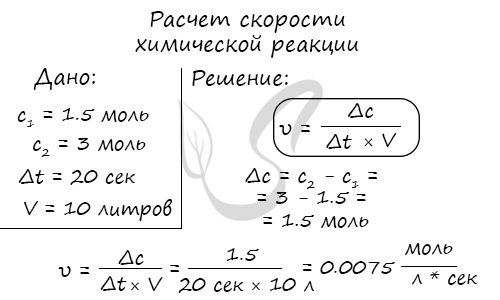
Скорость реакции отражает изменение концентраций реагирующих веществ за единицу времени. Единицы измерения для гомогенной реакции: моль/л * сек. Физический смысл в том, что каждую секунду какое-то количество одного вещества превращается в другое в единице объема.
Мне встречались задачи, где была дана молярная концентрация вещества до реакции и после, время и объем. Требовалось посчитать скорость реакции. Давайте решим подобное несложное задание для примера:
Влияние природы реагирующих веществ
При изучении агрегатных состояний веществ возникает вопрос: где же быстрее всего идут реакции: между газами, растворами или твердыми веществами?
Запомните, что самая высокая скорость реакции между растворами, в жидкостях. В газах она несколько ниже.
Если реакция гетерогенная: жидкость + твердое вещество, газ + твердое вещество, жидкость + газ, то большую роль играет площадь соприкосновения реагирующих веществ.
Химическая активность также играет важную роль. Например, отвечая на вопрос: какой из металлов Li или K быстрее прореагирует с водой? Мы отдадим предпочтение литию, так как в ряду активности металлов он стоит левее калия, а значит литий активнее калия.
Иногда для верного ответа на вопрос о скорости реакции требуется знание активности кислот. Мы подробнее обсудим эту тему в гидролизе, однако сейчас я замечу: чем сильнее (активнее) кислота, тем быстрее идет реакция.
Например, реакцию магния с серной кислотой протекает гораздо быстрее реакции магния с уксусной кислотой. Причиной этому служит то, что серная кислота относится к сильным (активным) кислотам, а активность уксусной кислоты меньше, она является слабой кислотой.
Как я уже упомянул, слабые и сильные кислоты и основания изучаются в теме гидролиз.
Влияние изменения концентрации
Замечу деталь, которая может оказаться важной, если в реакции участвуют газы: при увеличении давления концентрация вещества на единицу объема возрастает (представьте, как газ сжимается). Поэтому увеличение давление, если среди исходных веществ есть газ, увеличивает скорость реакции.
Закон действующих масс устанавливает соотношение между концентрациями реагирующих веществ и их продуктами. Скорость простой реакции aA + bB → cC определяют по уравнению:
Записанное выше следствие закона действующих масс нужно не только «зазубрить», но и понять. Поэтому мы решим пару задач, где потребуется написать подобную формулу.
Окисление диоксида серы протекает по уравнению: 2SO2(г) + O2 = 2SO3(г). Как изменится скорость этой реакции, если объемы системы уменьшить в три раза?
По итогу решения становится ясно, что скорость реакции в таком случае возрастет в 27 раз.
Решим еще одну задачу. Дана реакция синтеза аммиака: N2 + ЗН2 = 2NH3. Как изменится скорость прямой реакции образования аммиака, если уменьшить концентрацию водорода в два раза?
В результате решения мы видим, что при уменьшении концентрации водорода в два раза скорость реакции замедлится в 8 раз.
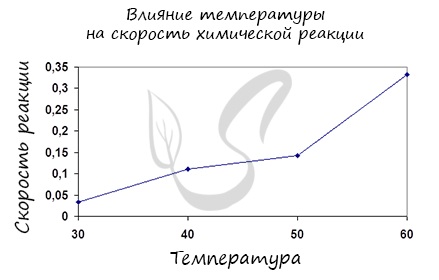
Влияние изменения температуры на скорость реакции
Постулат, который рекомендую временно взять на вооружение: «Увеличение температуры увеличивает скорость абсолютно любой химической реакции: как экзотермической, так и эндотермической. Исключений нет!»
Правило Вант-Гоффа, голландского химика, позволяет точно оценить влияние температуры на скорость химической реакции. Оно звучит так: «При повышении температуры на каждые 10 градусов константа скорости гомогенной элементарной реакции увеличивается в два — четыре раза»
Если по итогам решения задач у вас получится температурный коэффициент меньше 2 или больше 4, то, скорее всего, где-то вы допустили ошибку. Используйте этот факт для самопроверки.
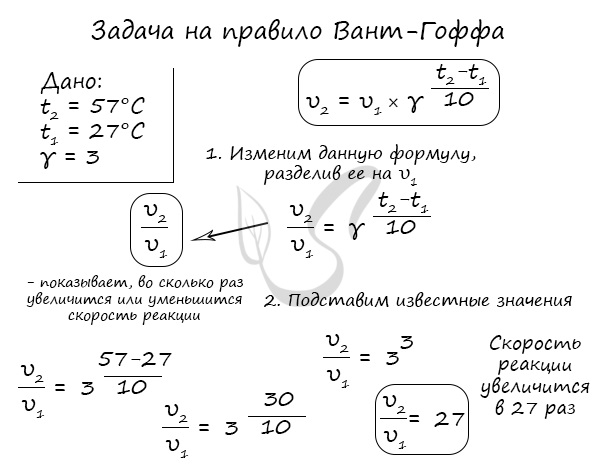
Для тренировки решим пару задач, в которых потребуется использование правило Вант-Гоффа.
Как изменится скорость гомогенной реакции при повышении температуры от 27°C до 57°C при температурном коэффициенте, равном трем?
Иногда в задачах требуется рассчитать температурный коэффициент, как, например, здесь: «Рассчитайте, чему равен температурный коэффициент скорости, если известно, что при понижении температуры от 250°C до 220°C скорость реакции уменьшилась в 8 раз».
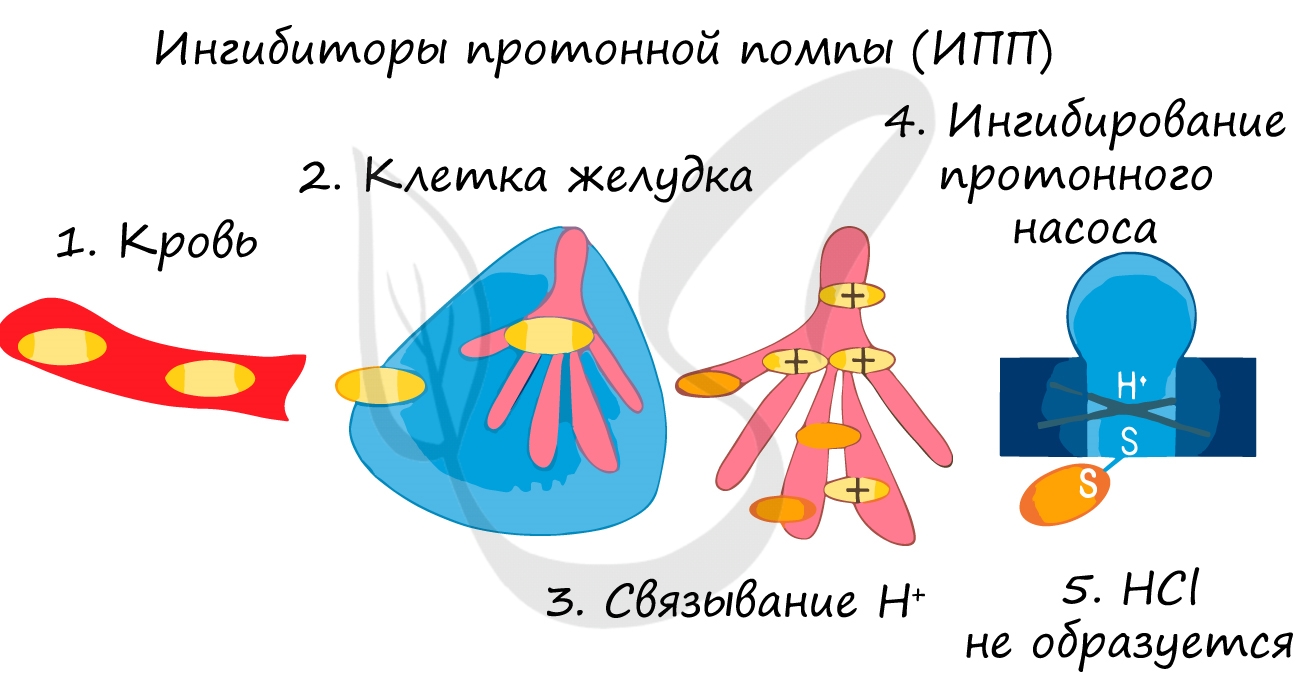
Катализаторы и ингибиторы
Ингибиторы применяют для замедления коррозии металла, окисления топлива, старения полимеров. Многие лекарственные вещества являются ингибиторами.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Скорость химической реакции
Катализ и катализаторы
Катализ – это процесс изменения скорости химической реакции при помощи катализаторов – веществ, принимающих участие в химической реакции, но в состав конечных продуктов не входящих и в результате реакции не расходующихся.
Одни катализаторы ускоряют реакцию (положительный катализ), другие – замедляют (отрицательный катализ). Отрицательный катализ называют ингибированием, а катализаторы, понижающие скорость химической реакции – ингибиторами.
Различают гомогенный и гетерогенный катализ.
Гомогенный катализ.
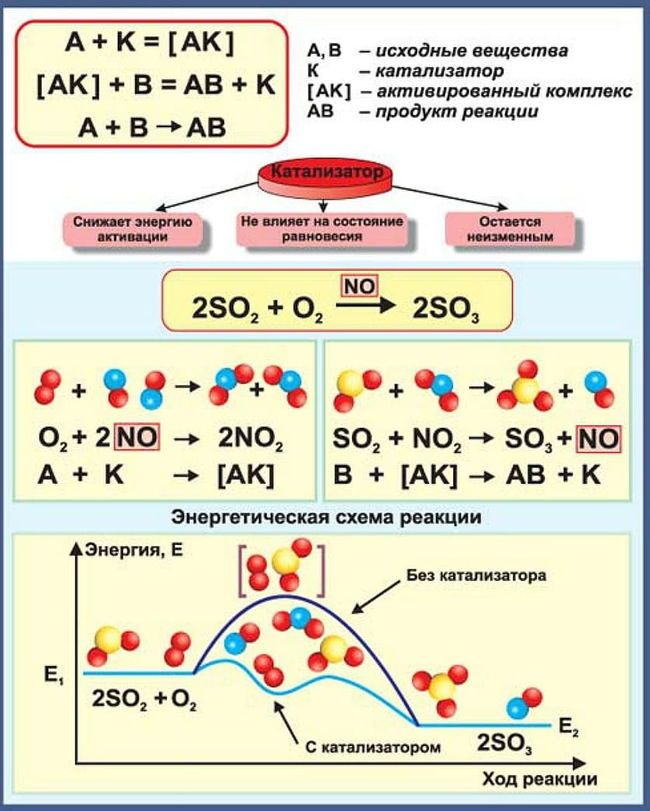
При гомогенном (однородном) катализе реагирующие вещества и катализатор находятся в одинаковом агрегатном состоянии и между ними отсутствует поверхность раздела. Пример гомогенного катализа – реакция окисления SO2 и SO3 в присутствии катализатора NO (реагирующие вещества и катализатор являются газами).
Гетерогенный катализ.
В случае гетерогенного (неоднородного) катализа реагирующие вещества и катализатор находятся в различных агрегатных состояниях и между ними существует поверхность (граница) раздела. Обычно катализатор – твердое вещество, а реагирующие вещества – жидкости или газы. Пример гетерогенного катализа – окисление NN3 до NO в присутствии Pt (катализатор – твердое вещество).
Механизм действия катализаторов
Действие положительных катализаторов сводится к понижению энергии активации реакции Еа(исх), действие ингибиторов – противоположное.
Так, для реакции 2HI = H2+I2 Еа(исх)=184 кДж/моль. Когда же эта реакция протекает в присутствии катализатора Au или Pt, то Еа(исх)=104 кДж/моль, соответственно.
Механизм действия катализатора при гомогенном катализе объясняется образованием промежуточных соединений между катализатором и одним из реагирующих веществ. Далее промежуточное соединение реагирует со вторым исходным веществом, в результате чего образуется продукт реакции и катализатор в первоначальном виде. Так как скорость обоих промежуточных процессов значительно больше скорости прямого процесса, то реакция с участием катализатора протекает значительно быстрее, чем без него.
SO2 +1/2 O2 = SO3 протекает очень медленно, а если использовать катализатор NO
то реакции NO +1/2О2 = NO2 и NO2 +SO2 = SO3 +NO протекают быстро.
Механизм действия катализатора при гетерогенном катализе иной. В этом случае реакция протекает вследствие адсорбции молекул реагирующих веществ поверхностью катализатора (поверхность катализатора неоднородна: на ней имеются так называемые активные центры, на которых и адсорбируются частицы реагирующих веществ.). Увеличение скорости химической реакции достигается, в основном, за счет понижения энергии активации адсорбированных молекул, а также, отчасти, за счет увеличения концентрации реагирующих веществ в местах, где произошла адсорбция.
Каталитические яды и промоторы.
Некоторые вещества снижают или полностью уничтожают активность катализатора, такие вещества называют каталитическими ядами. Например, небольшие примеси серы (0,1%) полностью прекращает каталитическое действие металлического катализатора (губчатого железа), использующегося при синтезе аммиака. Вещества, повышающие активность катализатора, называют промоторами. Например, каталитическая активность губчатого железа значительно возрастает при добавлении примерно 2% метаалюмината калия KAlO2.
Применение катализаторов
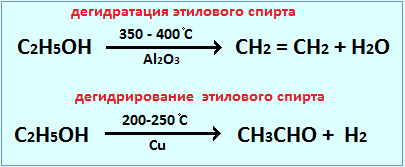
Действие катализатора избирательно и специфично. Это означает, что, применяя различные катализаторы, из одних и тех же веществ можно получить различные продукты. Это особенно характерно для реакций органических веществ. Например, в присутствии катализатора AlO3 происходит дегидратация этилового спирта, в присутствии Cu – дегидрирование:
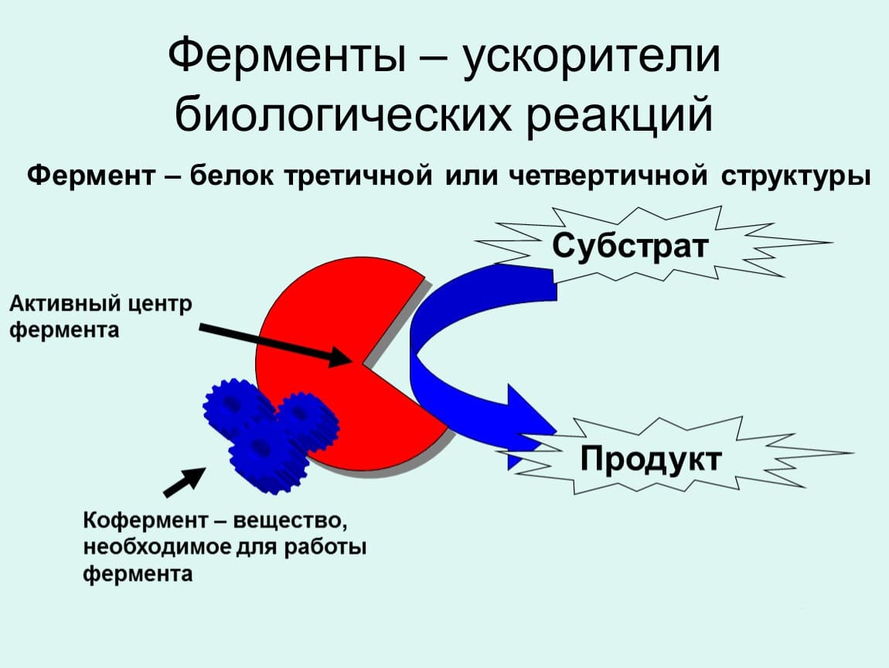
Биологические катализаторы, принимающие участие в сложных химических превращениях, протекающих в организме, называются ферментами.
Катализаторы широко используются в производстве серной кислоты, аммиака, каучука, пластмасс и др. веществ.
Скорость химических реакций. Действие катализаторов.
Скорость химической реакции определяется количеством вещества, прореагировавшего в единицу времени в единице объема.
Если при постоянных объеме и температуре концентрация одного из реагирующих веществ уменьшилась от с1 до с2 за определенный промежуток времени от t1 до t2, то скорость химической реакции равна:
где k — коэффициент, не зависящий от концентрации, называется константой скорости реакции,
vA и vB – постоянные числа – показатели порядка скорости реакции по реагентам А и В.
Следует отметить, что показатели порядка скорости реакции vA и vB о реагентам никогда не равны стехиометрическим коэффициентам a и b (исключение может быть только в одном случае – если реакция представляет собой элементарный акт).
Для сложных реакций показатели порядка реакции не равны стехиометрическим коэффициентам и определяются только экспериментально.
Такая зависимость справедлива для газов и жидкостей (гомогенные системы). Для гетерогенной реакции (с участием твердых веществ) скорость реакции зависит еще и от величины поверхности соприкосновения между реагирующими веществами. Любое увеличение площади поверхности приводит к увеличению скорости реакции.
Влияние катализаторов на скорость химической реакции.
Механизм действия катализаторов (упрощенный).
В ходе катализируемой химической реакции происходит образование промежуточных продуктов (образование связи между катализатором и реагирующим веществом).
Реакция без катализатора идет очень медленно, а при добавлении катализатора К, о реагирует с одним из исходных веществ (например, с А), образуя очень непрочное и реакционноспособное промежуточное соединение АК:
Это промежуточное соединение реагирует с другим исходным веществом В, образуя конечный продукт АВ и катализатор выходит в первоначальном виде:
Катализатор может участвовать в реакции бесконечное число раз. Но следует учесть, что в реакциях могут присутствовать соединения, понижающие активность катализатора. Такие вещества называется каталитическими ядами, а сам процесс – отравлением.
Гомогенный катализ.
Гетерогенный катализ.
При гетерогенном катализе происходит адсорбция реагирующих веществ поверхностью катализатора (она неоднородна, и здесь расположены активные центры, под действием которых связь между атомами реагентов ослабляется, молекула деформируется, а иногда даже распадается).
Для катализатора характерна избирательность действия (определенный катализатор для определенной реакции). Подбор оптимальных катализаторов является насущной проблемой многих производств: переработка газов, крекинг углеводородов, нефтяная промышленность, получение полимеров, каучука и т. д.
В живой природе катализаторы также играют большую роль, только называются они ферментами.
Виды и особенности катализаторов химических реакций
Химическая реакция – это процесс превращения реагентов в продукты реакции. Многие превращения в химии имеют очень долгий срок протекания, что абсолютно недопустимо для промышленности или для организма человека. Колоссальное ускорение превращений как в промышленности, так и в живых организмах, обеспечивают катализаторы химических реакций. Рассмотрим этот вопрос подробнее.
Что такое катализатор реакции?
Речь идет о веществе, которое способно ускорять протекание превращения многократно. Процесс в химии, протекающий в присутствии ускорителей превращений, называется катализом. Катализ характеризуется тем, что вещество, ускоряющее химический процесс, не расходует в ходе протекания последнего, а также не входит в состав конечных продуктов.
Катализ по своему результату может быть двух видов: положительный и отрицательный. Положительный катализ приводит к увеличению скорости превращения. Отрицательный катализ приводит к замедлению или прекращению протекания химического превращения. Вещества, реализующие, отрицательный катализ называются ингибиторами.
Разновидности веществ, ускоряющих химические реакции
Существуют две общепризнанных классификации веществ, которые ускоряют протекания превращений в химии. Первая основывается на агрегатном состоянии катализатора, вторая – на происхождении.
Классификация по агрегатному состоянию
По агрегатному состоянию вещества каталитические соединения можно подразделить на гомогенные и гетерогенные. Гомогенные вещества, ускоряющие химическую реакцию, находятся в одной фазе с реагентами. Гетерогенные вещества, ускоряющие химическое превращение, находятся в разных фаза с реагентами (например, катализатор представлен жидкость, а реагенты – газами).
Свойства гомогенных ускорителей реакции
К данной группе соединений относятся кислоты и основания. Например, серная кислота ускоряет протекание превращение органических субстратов. Основными свойствами гомогенных соединений являются:
Свойства гетерогенных ускорителей реакции
К данной группе соединений относятся оксиды большинства металлов (Al2O3, CaO, BaO, MgO, TiO2), а также алюмосиликаты и цеолиты. Обозначим основные свойства гетерогенных каталитических веществ:
Классификация по происхождению
По происхождению вещества, ускоряющие процесс протекания превращений в химии, подразделяются на органические и неорганические. Неорганические соединения в основном представлены тяжелыми металлами (свинец, палладий), спектр органический соединений намного шире. Основными представителями органических ускорителей превращений являются энзимы (соединения биологического происхождения). Энзимы – это катализаторы, увеличивающие скорость химических реакций в живых организмах. Ферменты (энзимы) имеют следующие особенности:
Свойства катализаторов
Каталитические вещества, ускоряющие протекание реакций в химии, имеют определенные свойства. Обозначим их:
Другие свойства каталитические соединений связаны с их строением и физическими параметрами:
Каталитические системы на основе катализаторов
Современные промышленные каталитические смеси состоят из нескольких компонентов:
Промотор
Добавление промоторов к каталитическому соединению улучшает следующие свойства последних: активность, избирательность и стабильность в системе. Сам по себе промотор может являться соединением, которое не участвует в протекающем процессе. По своему назначению активаторы подразделяются на две большие группы:
Также промоторы подразделены на две большие группы структурообразующие (инертные соединения, предотвращающие слипание частиц) и активирующие (изменяют электронную конфигурацию каталитического соединения в активную фазу катализа).
Носитель
Носитель представляет собой материю, на которую различными методами укладывают катализатор. При использовании носителя увеличивается площадь поверхности действия каталитического соединения, повышается его термостойкость. Благодаря использованию носителей возможна экономия в промышленных условиях достаточно дорогих каталитических элементов (палладий, никель, платина, серебро). Однако стоит отметь, что носитель также может положительно влиять на активность каталитического соединения, поэтому нельзя провести четкую границу между этими двумя понятиями. Носителями могут быть оксид алюминия, силикагель, пемза, каолин, асбест, алюмосиликаты и другие вещества.