клопидогрел или аспирин что лучше
Некоторые аспекты применения ацетилсалициловой кислоты и клопидогрела у кардиологических больных
Рассмотрены возможности использования ацетилсалициловой кислоты и клопидогрела у больных со стабильными проявлениями атеротромбоза для первичной профилактики сердечно-сосудистых заболеваний и вопросы безопасности антитромбоцитарной терапии.
Possibilities of use of acetylsalicylic acid and clopidogrel in patients with stable implications of atherothrombosis, for primary prevention of cardiovascular diseases and safety questions of antithrombocytic therapy are surveyed.
Признание атеротромбоза основой патогенеза большинства сердечно-сосудистых заболеваний (ССЗ), успехи в изучении молекулярных механизмов тромбообразования оказали влияние на развитие антитромбоцитарной терапии и способствовали появлению новых препаратов [1]. Наиболее изученными и широко применяемыми в клинической практике антитромбоцитарными препаратами в настоящее время являются ацетилсалициловая кислота (АСК) и клопидогрел.
В качестве лекарственного средства АСК известна с 1899 г. Несмотря на более чем 100-летний опыт использования и появление в последние годы новых антиагрегантов, АСК удалось сохранить за собой позиции «золотого» стандарта антитромбоцитарной терапии. В основе антитромбоцитарного действия АСК лежит ее способность необратимо ингибировать фермент циклооксигеназу (ЦОГ) тромбоцитов, вследствие чего снижается образование тромбоксана А2 — мощного стимулятора агрегации тромбоцитов и вазоконстриктора. Циклооксигеназа имеет две изоформы: ЦОГ-1 и ЦОГ-2. Притом, что АСК блокирует обе изоформы, ее активность в отношении ЦОГ-1 в тромбоцитах в 50–100 раз выше, чем влияние на ЦОГ-2 в моноцитах и других клетках воспаления. Поскольку тромбоциты не имеют ядра и поэтому не способны синтезировать белки, необратимое ингибирование ЦОГ-1 приводит к тому, что блокада синтеза тромбоксана А2 под действием АСК сохраняется на протяжении всего периода жизни тромбоцитов (в течение 7–10 дней). Именно способность необратимо блокировать ЦОГ-1 обусловливает стабильный и длительный антитромбоцитарный эффект АСК [2].
Клопидогрел по химической структуре относится к тиенопиридинам. Механизм антитромбоцитарного действия клопидогрела отличается от такового АСК и заключается в селективном и необратимом ингибировании P2Y12-рецепторов тромбоцитов, что, в свою очередь, приводит к угнетению стимуляции аденилатциклазного механизма и блокированию связанного с ним сигнала, направленного на усиление агрегации тромбоцитов [3]. Клопидогрел является пролекарством и метаболизируется в печени в активный метаболит с помощью нескольких изоферментов цитохрома Р450 (CYP). Исследования последних лет показали, что существуют полиморфизмы генов, носительство которых ассоциируется со снижением активности ферментов, участвующих в превращении клопидогрела в активный метаболит [4]. Так, носительство аллеля CYP2C19*1 обеспечивает полностью функционирующий метаболизм, тогда как носительство аллелей CYP2C19*2 и CYP2C19*3 уменьшает функциональную активность ферментов, метаболизирующих клопидогрел. Установлено, что носительство различных аллелей CYP2C19 определяет не только фармакокинетику активного метаболита клопидогрела, но и антитромбоцитарный эффект. По данным ряда исследований [5–10], носительство аллелей CYP2C19*2 и CYP2C19*3 соотносится с меньшим подавлением агрегации тромбоцитов и более высокой частотой неблагоприятных сердечно-сосудистых событий (включая тромбозы внутрикоронарных стентов) у больных, получающих клопидогрел в стандартной дозировке (75 мг/сут).
Важно отметить, что при одновременном применении АСК и клопидогрела антитромбоцитарный эффект усиливается. Предполагают, что это обусловлено синергизмом между двумя препаратами в подавлении агрегации тромбоцитов, индуцированной коллагеном [3, 11].
Ацетилсалициловая кислота, безусловно, является более изученным препаратом, чем клопидогрел, поэтому неудивительно, что спектр ее применения в кардиологии значительно шире. Назначение АСК позволяет уменьшить частоту неблагоприятных исходов у больных стабильной и нестабильной стенокардией, инфарктом миокарда с наличием зубца Q на ЭКГ и без такового, после чрескожных коронарных вмешательств и операции аортокоронарного шунтирования, при цереброваскулярной болезни, а также у пациентов с перемежающейся хромотой атеросклеротического происхождения. Согласно рекомендациям европейских, американских и российских медицинских сообществ при всех вышеперечисленных заболеваниях и состояниях рекомендован неограниченно долгий (пожизненный) прием АСК. В разных рекомендациях при одном и том же заболевании предписано использовать различные дозы АСК (так, например, в Европе поддерживающая доза АСК обычно составляет 75–100 мг/сут, а в США — 81 мг/сут), но предпочтительны все-таки низкие дозы АСК как минимально эффективные.
Клопидогрел рекомендуется использовать в основном в комбинации с АСК (так называемая двойная антитромбоцитарная терапия) при инфаркте миокарда и нестабильной стенокардии, а также у больных, подвергнутых чрескожным коронарным вмешательствам, поскольку, как было показано в многочисленных крупных исследованиях, добавление клопидогрела к АСК в этих ситуациях превосходит по эффективности монотерапию АСК. Монотерапия клопидогрелом как альтернатива монотерапии АСК может быть рекомендована только при атеросклеротическом поражении артерий нижних конечностей [12–14] и в качестве средства вторичной профилактики у больных, перенесших острое нарушение мозгового кровообращения [15–17]. Во всех остальных случаях монотерапия клопидогрелом возможна лишь при непереносимости АСК.
Рассмотрим более подробно некоторые аспекты применения АСК и клопидогрела в кардиологической практике.
Первичная профилактика ССЗ
Н. М. Воробьёва, доктор медицинских наук
ФГБУ РКНПК МЗ РФ, Москва
Роль клопидогреля в лечении и профилактике сердечно-сосудистых заболеваний
Г.А.Барышникова
Кафедра семейной медицины
ФГХ Учебно-научный медицинский центр, Москва
Ведущая роль в профилактике осложнений атеросклероза принадлежит антитромбоцитарным препаратам (антиагрегантам), ингибирующим функцию тромбоцитов. Классификация антитромбоцитарных средств (антиагрегантов) представлена в табл. 1. Перечисленные антиагреганты блокируют агрегацию тромбоцитов посредством разных механизмов действия. Аспирин блокирует циклооксигеназу, предотвращая образование тромбоксана А2; дипиридамол увеличивает концентрацию циклических нуклеотидов и влияет на концентрацию АДФ, тромбина, арахидоновой кислоты; производные тиенопиридина (тиклопидин, клопидогрель) необратимо ингибируют АДФ-индуцированную агрегацию тромбоцитов, блокируя аденозиновые рецепторы тромбоцитов; антагонисты ГП рецепторов тромбоцитов GP IIb/IIIa предотвращают образование межтромбоцитарных фибриногеновых мостиков.
Таблица 1.
Основные классы антиагрегантных препаратов
Поскольку в первую очередь, вызывается и усиливается агрегация тромбоцитов тромбоксан А2 и АДФ, неудивительно, что с целью профилактики атеротромботических осложнений стали широко применять антиагреганты, влияющие на образование ТхА2 (аспирин) или блокирующие АДФ-рецепторы тромбоцитов (тиенопиридины). Дипиридамол используется преимущественно после перенесенного ишемического инсульта в комбинации с аспирином. Ингибиторы IIβ/IIIα ГП-рецепторов (прежде всего абсиксимаб) с успехом применяются (парентерально!) при проведении ангиопластики, однако попытка использовать эти препараты длительно перорально не увенчалась успехом.
Таблица 2.
Расширение показаний к применению антитромбоцитарных препаратов по итогам метаанализа 2002 г. [5]
| Показания к применению антитромбоцитарных препаратов | 1994 г. | 2002 г. |
| Острый ИМ | + | + |
| Нестабильная стенокардия | + | + |
| Перенесенный ИМ | + | + |
| Перенесенный ишемический инсульт | + | + |
| Острый ишемический инсульт | + | |
| Перемежающаяся хромота | + | |
| Стабильная стенокардия | + |
Но при всех его достоинствах аспирин не лишен ряда недостатков. Хорошо известны его побочные эффекты: диспепсия (в 20-30% случаев при длительном применении), эрозивно-язвенные поражения желудочно-кишечного тракта (ЖКТ), бронхоспазм, острый приступ подагры (из-за нарушения экскреции мочевой кислоты); аллергические реакции. Развитие аспирининдуцированных осложнений со стороны слизистой оболочки ЖКТ требует отмены аспирина и назначения наиболее эффективных в данной ситуации ингибиторов протонной помпы. Снизить риск неблагоприятного воздействия аспирина на ЖКТ можно, используя таблетки с кишечнорастворимой оболочкой, например Аспирин Кардио [6]. При непереносимости аспирина альтернативой ему согласно большинству европейских и отечественных рекомендаций является клопидогрель.
Рис. 1. Сравнительная эффективность аспирина и клопидогреля в исследовании CAPRIE [11].
Рис. 2. Риск осложнений со стороны ЖКТ в исследовании CAPRIE [12].
Клопидогрель по сравнению с аспирином вызывает меньше осложнений со стороны ЖКТ
Ацетилсалициловая кислота vs клопидогрел во вторичной профилактике сердечно-сосудистых событий

Сравнение основных характеристик АСК и клопидогрела: показания и побочные эффекты
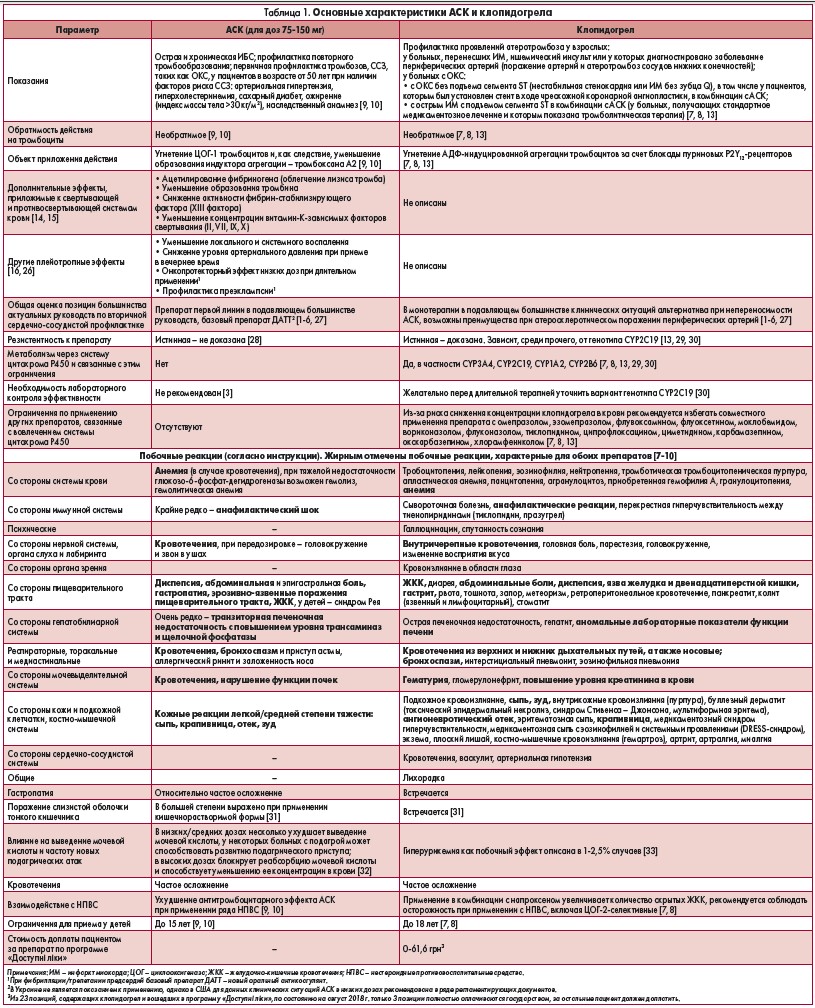
Основные характеристики АСК и клопидогрела приведены в таблице 1. Даже при рассмотрении показаний к их назначению, которые представлены в актуальных инструкциях, одобренных Министерством здравоохранения Украины, заметна разница 8. Для АСК очевидна ориентация на ишемическую болезнь сердца – ИБС (как хронические, так и острые ее формы). Представлено в инструкциях и показание использовать АСК для первичной профилактики сердечно-сосудистых заболеваний (ССЗ), что ближе к североамериканской позиции в отношении антитромбоцитарной терапии (АТТ). Большая часть показаний клопидогрела направлена на пациентов с острыми сердечно-сосудистыми состояниями, включая острый коронарный синдром (ОКС), а также на клинические ситуации, связанные с атеросклеротическим поражением периферических артерий (инсульт, атеротромбоз сосудов нижних конечностей). В официальных украинских инструкциях к препаратам клопидогрела, утвержденных в 2013-2018 гг., есть показание к его применению в сочетании с АСК для профилактики атеротромбоза и тромбоэмболических событий при фибрилляции предсердий (ФП), что, вероятно, обусловлено предыдущей редакцией национального руководства по ФП [11], однако противоречит современной мировой практике. Так, в рекомендациях Европейского общества кардиологов по тромбопрофилактике при ФП (2016) [12] применение клопидогрела (и АСК, в том числе в комбинации) для АТТ при ФП (кроме двойной/тройной АТТ (ДАТТ/ТАТТ) на фоне ОКС/стентирования) не показано.
В рекомендациях Европейского общества кардиологов по ведению пациентов с ФП (2016) [12] отмечено, что доказательства в поддержку антитромбоцитарной монотерапии для профилактики инсульта при ФП чрезвычайно ограничены, а терапия витамин-К‑зависимым оральным антикоагулянтом (ОАК) лучше предотвращает инсульт, системные эмболии, ИМ, а также случаи смерти вследствие сосудистых причин, чем моно- или комбинированная АТТ (АСК + клопидогрел). Ежегодный риск указанных событий при применении комбинации АСК + клопидогрел составил 5,6% в сравнении с 3,9% в случае терапии витамин-К‑зависимым ОАК [48], причем разница была даже большей у пациентов с высоким риском тромбоэмболий [49]. В руководстве отмечено, что АТТ, особенно ДАТТ, увеличивает риск кровотечений (2,0 против 1,3% на монотерапии антитромбоцитарным препаратом; р 1 года), реваскуляризация (>1 года), стеноз коронарных артерий (50%). У пациентов, которым для АТТ был назначен клопидогрел, чаще отмечали артериальную гипертензию, сахарный диабет, инсульт в анамнезе, многососудистое поражение коронарных артерий, поражение периферических артерий и более длительный анамнез ИБС. По мнению исследователей, именно результаты CAPRIE явились причиной выбора клопидогрела для применения у пациентов с более тяжелым сосудистым поражением и течением заболевания.
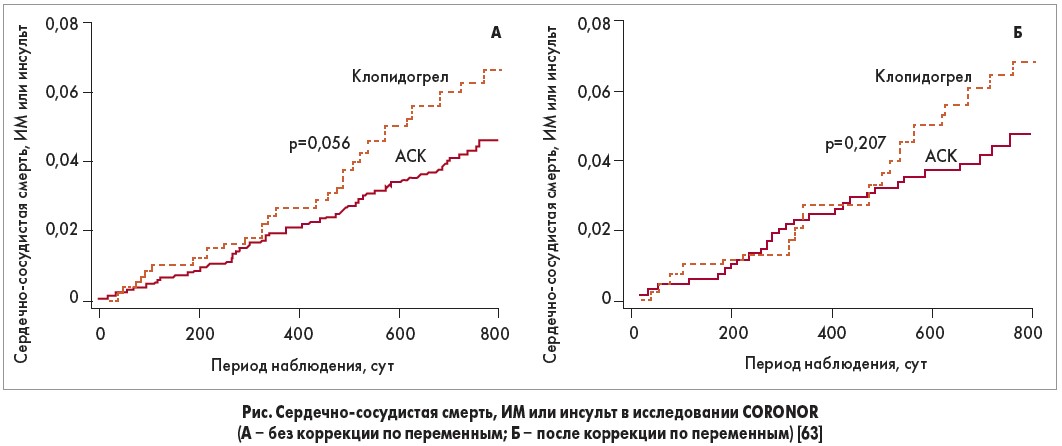
В противоположность результатам, полученным в исследовании CAPRIE, двухлетнее наблюдение за пациентами в более позднем и основанном на реальной практике исследовании CORONOR не подтвердило преимуществ монотерапии клопидогрелом перед АСК в дозе 100 мг/сут в отношении риска развития сердечно-сосудистых событий, что было особенно наглядно продемонстрировано в общей популяции без коррекции по переменным. Тем не менее в обоих анализах не было выявлено достоверных различий между группами лечения (рис.). По частоте возникновения кровотечений группы также не отличались: кровотечения с показателем BARC ≥3 отмечены у 16 (0,8%) пациентов группы АСК и у 5 (0,7%) – группы клопидогрела (95% доверительный интервал 0,82 (0,30-2,24); р=0,698).
Результаты исследования CORONOR свидетельствуют, что в современной клинической практике ведения пациентов со стабильным течением ИБС в качестве препарата для моно-АТТ часто используют клопидогрел, однако такую стратегию нельзя назвать лучшей по сравнению с моно-АТТ с применением АСК в том, что касается частоты развития ишемических событий или кровотечений.
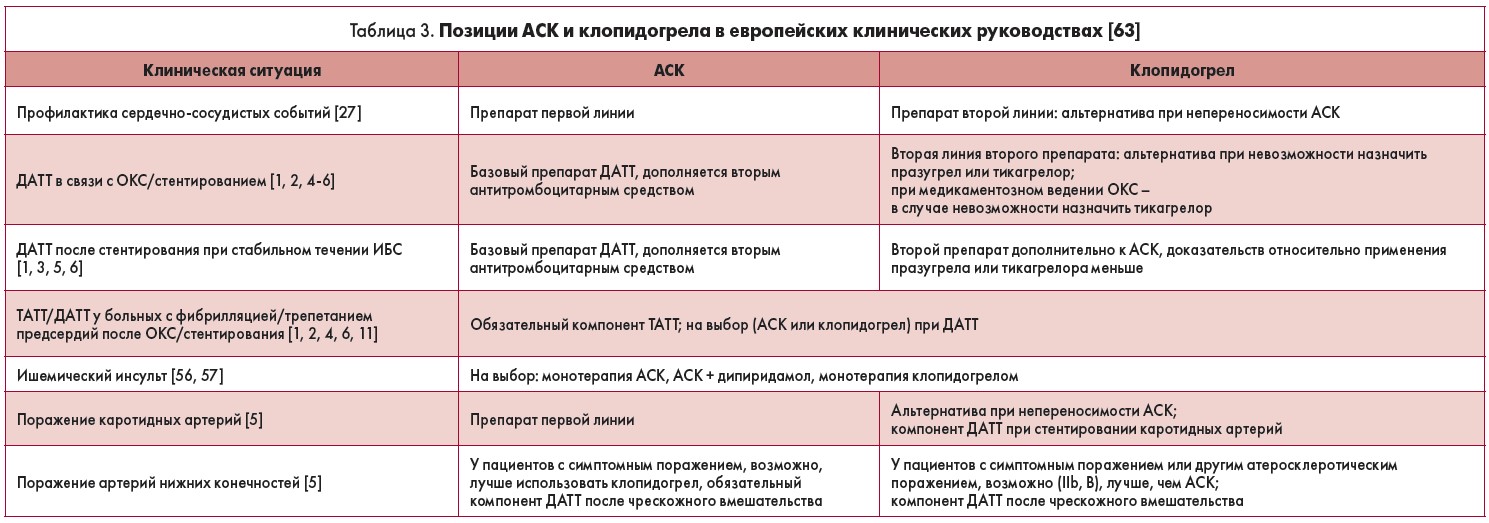
Таким образом, для клопидогрела сегодня сформировалось четкое терапевтическое окно (табл. 3).
Истинная резистентность и метаболизм клопидогрела через систему цитохрома P450 как причины ослабления его позиций в современных руководствах
Как видно из представленных в таблице 3 данных, в некоторых клинических ситуациях клопидогрел, ранее считавшийся одним из оптимальных препаратов, отходит на второй план. С чем связано это отступление клопидогрела с поля антитромбоцитарного боя? В первую очередь подвела истинная резистентность к препарату. Именно из-за этого феномена нагрузочная доза клопидогрела при ОКС в течение многих лет постепенно повышалась, поскольку это самый простой способ преодоления фармакологической резистентности. Специалисты Управления по контролю качества продуктов питания и лекарственных средств США (FDA) уже давно говорят о нагрузочной дозе 600 мг и поддерживающей 150 мг/сут для «плохих метаболизаторов» клопидогрела, однако отмечают, что для такой категории пациентов не был разработан и апробирован оптимальный режим [30]. Кроме того, в случае оценки пациента как «плохого метаболизатора» клопидогрела FDA рекомендует рассматривать другие варианты АТТ: поскольку с повышением дозы меняется профиль безопасности, сложно сказать, выиграет ли пациент с резистентностью к клопидогрелу от повышения дозы, когда существует более дешевая альтернатива в виде АСК (наверняка более безопасная в дозе 75-100 мг/сут) или более дорогая в виде празугрела и тикагрелора.
Новые представители группы блокаторов P2Y12-рецепторов имеют более скромные нагрузочные дозы и при ОКС в симбиозе с АСК убедительно «переиграли» клопидогрел [58, 59]. За ними не замечены огрехи в виде истинной резистентности (по крайней мере, пока). Что же касается резистентности к антитромбоцитарному эффекту АСК, то этой теме уже было посвящено много публикаций и исследований, в которых показано, что так называемая истинная резистентность к АСК маловероятна [28], а основной причиной снижения антитромбоцитарного эффекта АСК является псевдорезистентность как результат нарушения комплаенса, недостаточной дозы / кратности применения (активно обсуждается для лиц с повышенной массой тела, пациентов с сахарным диабетом и ускоренным восстановлением пула функционально полноценных тромбоцитов, например, при эссенциальной тромбоцитемии) и в не последнюю очередь как результат снижения биодоступности при применении кишечнорастворимой формы АСК; имеют значение и лекарственные взаимодействия с НПВС [28, 60-62].
Не добавляет популярности клопидогрелу и его метаболизм через систему цитохрома P450, что приводит к массе неудачных лекарственных взаимодействий, причем со многими средствами именно кардиологической группы, в частности статинами, о чем пишут в основном в американских источниках [29, 30]. И даже такая побочная реакция, как гиперурикемия, которая в первую очередь ассоциирована с приемом АСК, встречается и при применении клопидогрела [29, 33].
Заключение
Какова же позиция новых рутинных антитромбоцитарных/антитромботических стратегий? Пока что это соподчинение АСК. То есть при ОКС следует однозначно назначать ДАТТ с базовым компонентом в виде АСК. В подавляющем большинстве клинических ситуаций АСК остается приоритетным препаратом первой линии. И дело тут не только в недостижимой по масштабам для других антитромбоцитарных препаратов доказательной базе, существенное влияние на решение клиницистов и экспертов оказывают плейотропные эффекты АСК, несвойственные другим антитромбоцитарным средствам. Недавнее обнаружение онкопротекторных свойств низких доз АСК привело к повышению интереса к этому препарату в мире и, скорее всего, будет способствовать расширению его профилактических показаний. Уникальность АСК, дешевизна и доступность при впечатляющей и доказанной эффективности делают ее на сегодня непобедимым антитромбоцитарным средством, в то время как будущее клопидогрела несколько менее очевидно в свете появления новых конкурентов, которые по мере накопления доказательной базы при стабильном течении ИБС и поражении периферических артерий, появления их генерических форм и последующего снижения цены однажды могут оказаться лучшим выбором для пациентов не только при ОКС.
Список литературы находится в редакции.
Статья печатается в сокращении.
При поддержке ООО «Такеда Украина».
UA/MAGNH/0119/0001
Медична газета «Здоров’я України 21 сторіччя» № 1 (446), січень 2019 р.
СТАТТІ ЗА ТЕМОЮ Кардіологія
Призначення статинів з метою первинної та вторинної профілактики доведено зменшує ризики несприятливих серцево-судинних подій шляхом зниження холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ). Однак у деяких випадках, незважаючи на високодозову терапію статинами, в пацієнтів зберігаються залишкові серцево-судинні ризики через недостатню ефективніть терапії. Альтернативою для таких пацієнтів може бути езетиміб, який при додаванні до тепапії статином значно підвищує ефективніть гіполіпідемічної терапії.
Пандемія коронавірусної хвороби (COVID‑19) внесла свої корективи в перебіг серцево-судинних захворювань (ССЗ), оскільки вірус SARS‑CoV‑2 чинить надзвичайно широкий вплив на організм людини та здатен виступати додатковим до інших чинником серцево-судинного ризику. Ще однією проблемою сучасної медицини став післяковідний синдром. Багатогранність симптоматики, зниження працездатності, різноманітні психологічні та серцево-судинні прояви цього стану значно погіршують якість життя й потребують уваги сімейного лікаря та кардіолога. У цій ситуації β-адреноблокатори є одними з небагатьох препаратів для лікування ССЗ, що послідовно підтверджують високу безпечність й асоціацію з кращим прогнозом у хворих на COVID‑19, які за кардіальними показаннями їх отримують, залишаючись базовою групою препаратів для лікування серцево-судинної патології. Їхня роль у впливі на серцево-судинний континуум, у тому числі серед хворих на COVID‑19, важко переоцінити.
Антитромботическая терапия у пациентов, перенесших ишемический инсульт: место ацетилсалициловой кислоты и клопидогрела
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Сердечно-сосудистые заболевания (ССЗ) являются основной причиной заболеваемости и смертности населения во всем мире.
Сердечно-сосудистые заболевания (ССЗ) являются основной причиной заболеваемости и смертности населения во всем мире. Если в 1900 г. на долю ССЗ приходилось менее 10% смертельных исходов, то в 2000 г., по данным ВОЗ, ССЗ стали основной причиной смертности. В 1996 г. от ССЗ в мире умерли 15 млн человек, по прогнозам экспертов, к 2020 г. эта цифра может достичь 25 млн [1]. В структуре сердечно-сосудистой патологии лидируют ишемическая болезнь сердца и инсульт. Инсульт не только занимает второе место среди причин смерти от ССЗ, но и считается ведущей причиной инвалидизации у лиц пожилого возраста. В нашей стране ежегодно регистрируется более 400 тыс. инсультов, среди которых преобладают ишемические (70–85%) [2], возникающие вследствие атеросклеротического поражения церебральных артерий.
Атеросклероз – это заболевание, поражающее артерии эластического типа (аорту и подвздошные сосуды), а также крупные и средние артерии мышечного типа (коронарные, сонные, внутримозговые, артерии нижних конечностей), проявляющееся уплотнением сосудистой стенки и образованием атеросклеротических бляшек. Это динамичный процесс, для которого характерно как прогрессирование, так и обратное развитие изменений в стенке артерии. Однако со временем атеросклероз прогрессирует, приводя, в конечном итоге, к клиническим проявлениям заболевания [1]. Образующиеся в церебральных артериях атеросклеротические бляшки уменьшают их просвет и ограничивают приток крови к головному мозгу, следствием чего является хроническая ишемия мозга с последующим развитием атеросклеротической энцефалопатии. При появлении трещины или разрыве покрышки бляшки на ее поверхности образуется тромб, состоящий из тромбоцитов и сети фибрина, заполненной эритроцитами. Появление на поверхности бляшки тромба, размеры которого могут то увеличиваться, то уменьшаться, создает условия для нестабильности кровоснабжения мозга и может привести к транзиторной ишемической атаке (ТИА). Дистанционное образование. При драматичном нарастании размеров тромба развивается окклюзия церебральной артерии и возникает ишемический инсульт (ИИ).
Установлено, что тромбообразование на поверхности поврежденной атеросклеротической бляшки происходит за счет активации тромбоцитов и каскада коагуляции и является причиной не только острых состояний, но и прогрессирования заболевания. Активация обоих процессов происходит одновременно, а мембрана тромбоцитов служит фосфолипидной поверхностью, на которой происходит активация каскада коагуляции. По современным представлениям, активация тромбоцитов начинается с их адгезии (приклеивания) к поврежденному деэндотелизированному участку сосуда, затем происходит их агрегация (склеивание) с формированием так называемых первичных тромбоцитарных «пробок». Тромбоцитарные тромбы непрочные, легко «размываются» потоком крови и могут быть причиной микрососудистой обструкции. Активация каскада коагуляции связана с экспозицией на поверхности бляшки тканевого фактора, содержащегося, наряду с холестерином и его эфирами, в макрофагах бляшки. Вследствие активации каскада коагуляции образуется тромбин – ключевой фермент свертывания крови. В связи с вышесказанным, препараты, ингибирующие функцию тромбоцитов и каскад коагуляции, представляются теоретически обоснованными для профилактики и лечения всех проявлений атеротромбоза [3].
Антитромботическая терапия является одним из ведущих направлений в лечении и профилактике инсульта и обязательна к назначению всем больным, перенесшим ИИ или ТИА. С этой целью в клинических исследованиях были изучены следующие препараты: ацетилсалициловая кислота (АСК), клопидогрел, тиклопидин, дипиридамол, а также новые антиагреганты (цилостазол, трифлузал и терутробан) и пероральные антикоагулянты. С позиций доказательной медицины у больных, перенесших ИИ, была установлена эффективность АСК, клопидогрела, тиклопидина и дипиридамола медленного высвобождения (МВ), из них наиболее изученными и широко применяемыми являются АСК и клопидогрел.
В качестве лекарственного средства АСК известна с 1899 г. Несмотря на более чем 100-летний опыт использования и появление в последние годы новых антиагрегантов, АСК удалось сохранить за собой позиции «золотого стандарта» антитромбоцитарной терапии. В основе антитромбоцитарного действия АСК лежит ее способность необратимо ингибировать фермент циклооксигеназу (ЦОГ) тромбоцитов, вследствие чего снижается образование тромбоксана А2 – мощного стимулятора агрегации тромбоцитов и вазоконстриктора. Циклооксигеназа имеет две изоформы: ЦОГ-1 и ЦОГ-2. При том, что АСК блокирует обе изоформы, ее активность в отношении ЦОГ-1 в тромбоцитах в 50–100 раз выше, чем влияние на ЦОГ-2 в моноцитах и других клетках воспаления. Поскольку тромбоциты не имеют ядра и поэтому не способны синтезировать белки, необратимое ингибирование ЦОГ-1 приводит к тому, что блокада синтеза тромбоксана А2 под действием АСК сохраняется на протяжении всего периода жизни тромбоцитов (в течение 7–10 дней). Именно способность необратимо блокировать ЦОГ-1 обусловливает стабильный и длительный антитромбоцитарный эффект АСК [4].
Клопидогрел по химической структуре относится к тиенопиридинам. Механизм антитромбоцитарного действия клопидогрела отличается от такового АСК и заключается в селективном и необратимом ингибировании P2Y12-рецепторов тромбоцитов, что, в свою очередь, приводит к угнетению стимуляции аденилатциклазного механизма и блокированию связанного с ним сигнала, направленного на усиление агрегации тромбоцитов [5]. Клопидогрел является пролекарством и метаболизируется в печени в активный метаболит с помощью нескольких изоферментов цитохрома Р450 (CYP). Исследования последних лет показали, что существуют полиморфизмы генов, носительство которых ассоциируется со снижением активности ферментов, участвующих в превращении клопидогрела в активный метаболит [6]. Так, носительство аллеля CYP2C19*1 обеспечивает полностью функционирующий метаболизм, тогда как носительство аллелей CYP2C19*2 и CYP2C19*3 уменьшает функциональную активность ферментов, метаболизирующих клопидогрел. Установлено, что носительство различных аллелей CYP2C19 определяет не только фармакокинетику активного метаболита клопидогрела, но и его антитромбоцитарный эффект. По данным ряда исследований [7–12], носительство аллелей CYP2C19*2 и CYP2C19*3 соотносится с меньшим подавлением агрегации тромбоцитов и более высокой частотой неблагоприятных сердечно-сосудистых событий (включая тромбозы внутрикоронарных стентов) у больных, получающих клопидогрел в стандартной дозировке (75 мг/сут).
Антитромботическая терапия в остром периоде ишемического инсульта АСК в остром периоде ИИ
В 2014 г. опубликованы результаты систематического обзора, объединившего 8 исследований и 41 183 пациента, при этом почти 98% больных были участниками двух крупных рандомизированных плацебо-контролируемых исследований – IST (1997) и CAST (1997) [13]. Дозы АСК в этих работах варьировали от 160 до 325 мг/сут, а длительность приема АСК/плацебо составила 4–24 нед.
Метаанализ этих исследований показал, что в сравнении с плацебо терапия АСК дополнительно предотвращает 9 смертельных исходов от любых причин на 1000 пролеченных и способствует полному восстановлению неврологического статуса в течение 30 дней после ИИ дополнительно у 7 человек на 1000 пролеченных. Подобный эффект достигается за счет небольшого увеличения риска нефатального большого внечерепного кровотечения (дополнительно 4 случая кровотечения на 1000 пролеченных). Кроме этого, польза АСК у больных ИИ проявляется в снижении частоты венозных тромбоэмболических осложнений [14].
Нужно отметить, что в этих работах специально не изучали ни оптимальную дозу начальной терапии АСК, ни оптимальное время для начала ее приема. Диапазон доз был достаточно широким – от 160 до 325 мг/сут. Последующий метаанализ подтвердил, что клиническая эффективность АСК не зависит от дозы препарата – увеличение дозы не приводит к еще большему снижению риска повторного инсульта. Прием АСК целесообразно начинать как можно раньше от момента появления симптомов инсульта, но только после исключения внутричерепного кровоизлияния. Кроме того, не следует использовать АСК в первые 24 ч после тромболитической терапии. С учетом этого, время начала приема АСК в данных исследованиях варьировало от 19 до 24 ч. Полученные результаты позволили рекомендовать назначение АСК в стартовой дозе 160–325 мг/сут в течение первых 48 ч после начала симптомов инсульта. Для снижения риска геморрагических осложнений через 1–2 нед. от начала лечения доза АСК для длительного приема может быть уменьшена до 75–100 мг/сут.
Эффективность монотерапии клопидогрелом и другими антиагрегантами в остром периоде инсульта окончательно не подтверждена.
Комбинированная антитромботическая терапия в остром периоде ИИ
Лишь в единичных исследованиях сравнили комбинацию АСК с другими антиагрегантами в остром периоде ИИ. В самом крупном из них – пилотном исследовании FASTER [15] – участвовали 392 пациента. Исследование имело интересный дизайн: в течение 24 ч после начала симптомов ИИ или ТИА назначали клопидогрел (нагрузочная доза 300 мг, далее 75 мг/сут) или плацебо; при этом все больные обязательно получали АСК. Длительность лечения составила 90 дней. Комбинация клопидогрела с АСК не показала значимых преимуществ по эффективности перед монотерапией АСК. Частота повторного инсульта была 7,1% в группе комбинированной терапии и 10,8% – в группе АСК (относительный риск (ОР) 0,7; 95% доверительный интервал (ДИ) 0,3–1,2); абсолютное снижение риска составило 3,8% (р=0,19). Частота геморрагических осложнений оказалась несколько выше в группе комбинированной терапии, в которой было отмечено 2 случая внутричерепных кровотечений (против 0 – в группе АСК); абсолютное увеличение риска – 1% (р=0,5). Исследователи сделали вывод, что польза комбинации АСК с клопидогрелом незначительна и не превышает риск геморрагических осложнений, поэтому применение комбинированной антитромботической терапии в остром периоде ИИ неоправданно.
Таким образом, на сегодняшний день АСК – единственный антиагрегант, эффективность и безопасность которого в остром периоде ИИ доказаны в крупных рандомизированных клинических исследованиях. Согласно рекомендациям [16–18], больным с острым ИИ следует проводить раннюю (в течение 48 ч) терапию АСК в дозе 160–325 мг/сут.
Вторичная профилактика после ишемического инсульта
Необходимость назначения антиагрегантов с целью вторичной профилактики ИИ сомнений не вызывает. Опубликованные в 2009 г. результаты крупного метаанализа [19], включившего 287 исследований по изучению роли антитромбоцитарных препаратов во вторичной профилактике сердечно-сосудистых осложнений у более чем 200 тыс. пациентов высокого риска, продемонстрировали значительную эффективность антиагрегантов по сравнению с плацебо. В этих исследованиях использовали 4 антиагреганта: АСК, клопидогрел, дипиридамол МВ и антагонисты гликопротеиновых рецепторов IIb/IIIa. Объединенный эффект различных антитромбоцитарных препаратов проявлялся в снижении риска развития нефатального инсульта на 25%, нефатального инфаркта миокарда – на 34%, сердечно-сосудистой смерти – на 15%, а также комбинированной конечной точки (инсульт, инфаркт миокарда, сердечно-сосудистая смерть) – на 25%.
АСК по сравнению с отсутствием терапии
Доступны результаты 11 исследований, в которых длительную терапию АСК сравнили с плацебо. Метаанализ этих исследований показал, что применение АСК в течение 2 лет у 1000 пациентов с ИИ или ТИА дополнительно предотвращает 5 случаев смерти, 25 повторных нефатальных инсультов и 6 нефатальных инфарктов миокарда ценой 7 нефатальных больших внечерепных кровотечений [19]. Дополнительное преимущество АСК заключается в снижении на 1/3 смертности от онкологических заболеваний, которое отмечено при длительном (свыше 5 лет) приеме АСК [20, 21], что эквивалентно предупреждению 20 смертей от рака у 1000 больных, перенесших ИИ и леченных АСК в течение 10 лет.
Доказательства эффективности и безопасности различных доз АСК в предупреждении сердечно-сосудистых осложнений получены в нескольких метаанализах, итоги которых суммированы в статье О. Vandvik и соавт. [22]. Было показано, что увеличение дозы АСК более 100 мг/сут сопровождается повышением риска геморрагических осложнений, а прием АСК в дозах менее 75 мг/сут недостаточно эффективно предотвращает инфаркты миокарда и инсульты. Поэтому в настоящее время большинством экспертов доза АСК 75–100 мг/сут признана оптимальной для вторичной профилактики ИИ и других сердечно-сосудистых осложнений.
Клопидогрел по сравнению с АСК
В исследовании CAPRIE [23] выполнили прямое сопоставление монотерапии АСК (325 мг/сут) с монотерапией клопидогрелом (75 мг/сут) у 19 185 пациентов высокого риска, недавно перенесших инфаркт миокарда, ИИ или имеющих клинические проявления атеросклероза артерий нижних конечностей. Наличие одного из данных заболеваний являлось основным критерием для включения в исследование, в соответствии с которым пациентов распределили на 3 подгруппы. Однако у многих больных проявления атеросклероза не ограничивались одним сосудистым бассейном, нередко имело место сочетанное поражение (например, часть пациентов с ИИ ранее перенесли инфаркт миокарда или имели сопутствующую перемежающуюся хромоту), поэтому распределение на подгруппы по основному критерию включения достаточно условно. Длительность приема антиагрегантов составила 1–3 (в среднем 1,9) года.
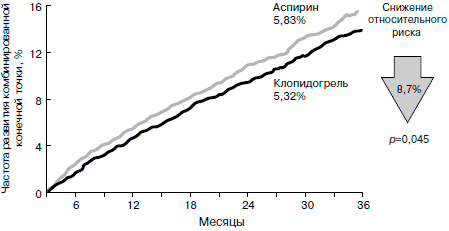
Исследование CAPRIE продемонстрировало несколько большую эффективность клопидогрела в отношении снижения частоты сердечно-сосудистых осложнений у больных высокого риска. В группе клопидогрела суммарная частота неблагоприятных событий (инфаркт миокарда, ИИ и сердечно-сосудистая смерть) оказалась несколько ниже, чем в группе АСК (5,3% в год для клопидогрела против 5,8% в год для АСК), что соответствовало снижению ОР на 8,7% (95% ДИ 0,3–16,5; р=0,043). В целом использование клопидогрела позволяло дополнительно предотвратить 5 неблагоприятных исходов на каждую 1000 пролеченных больных в год.
Однако в подгруппе пациентов, перенесших ИИ (n=6432), преимущества клопидогрела не были столь очевидными: так, частота комбинированной конечной точки составила 7,2% против 7,7% в группе АСК (p=0,26). Эффективность АСК и клопидогрела в предупреждении различных неблагоприятных событий оказалась практически одинаковой. Дальнейший ретроспективный анализ базы данных исследования CAPRIE обнаружил, что эффективность клопидогрела была выше у больных, ранее перенесших операцию аортокоронарного шунтирования, имевших несколько осложнений атеросклероза в анамнезе и страдающих сахарным диабетом, особенно инсулинозависимым.
Таким образом, результаты исследования CAPRIE свидетельствуют о том, что в целом монотерапия клопидогрелом, как минимум, не уступает по эффективности монотерапии АСК в профилактике сердечно-сосудистых осложнений у больных с клинически выраженными проявлениями атеросклероза. При этом в подгруппе больных, перенесших ИИ, эффективность АСК и клопидогрела оказалась практически одинаковой.
Комбинация дипиридамола и АСК по сравнению с монотерапией АСК
Дипиридамол представляет собой производное пиримидопиримидина с вазодилатирующими и антитромбоцитарными свойствами. Известно 2 механизма его антитромбоцитарного действия: первый связан с повышением содержания циклического аденозинмонофосфата в тромбоцитах за счет ингибирования фосфодиэстеразы, второй – с блокадой захвата аденозина и стимуляцией аденилатциклазного механизма агрегации тромбоцитов [3]. В связи с коротким (около 10 ч) периодом полужизни дипиридамол принимают 2 р./сут. Дипиридамол обладает низкой системной биодоступностью, поэтому в последние годы был создан препарат дипиридамола с замедленным высвобождением и улучшенной биодоступностью в комбинации с низкими (50 мг) дозами АСК.
Результаты исследований ESPS-2 [24] и ESPRIT [25] свидетельствуют о том, что эффективность комбинации низких доз АСК с дипиридамолом МВ превосходит таковую монотерапии АСК. В исследовании ESPS-2 [24] участвовали 6602 пациента с ИИ или ТИА, которых рандомизировали к монотерапии АСК (50 мг/сут), монотерапии дипиридамолом МВ (400 мг/сут), комбинации АСК (50 мг/сут) с дипиридамолом МВ (400 мг/сут) или к приему плацебо. Монотерапия АСК оказалась столь же эффективной, как и монотерапия дипиридамолом. В сравнении с плацебо в группе АСК риск повторного инсульта был ниже на 18% (р=0,013), в группе дипиридамола – на 16% (р=0,039); риск повторного инсульта или сердечно-сосудистой смерти – на 13% (р=0,016) и 15% (р=0,015) соответственно. В группе комбинированной терапии снижение риска неблагоприятных событий оказалось более выраженным – на 37% был ниже риск повторного инсульта (р A polymorphism and high on clopidogrel platelet reactivity associated with adverse 1-year clinical outcome of elective percutaneous coronary intervention with drug- eluting or bare-metal stents // J. Am. Coll. Cardiol. 2008. Vol. 51. P.1925–1934.
8. Mega J.L., Close S.L., Wiviott S.D. et al. Cytochrome P-450 Polymorphisms and Response to Clopidogrel // N. Engl. J. Med. 2009. Vol. 360. P. 354–362.
9. Collet J.P., Hulot J.S., Pena A. et al. Cytochrome P450 2C19 polymorphism in young patients treated with clopidogrel after myocardial infarction: a cohort study // Lancet. 2009. Vol. 373. P. 309–317.
10. Sibbing D., Stegherr J., Latz W. et al. Cytochrome P450 2C19 loss-of-function polymorphism and stent thrombosis following percutaneous coronary intervention // Eur. Heart J. 2009. Vol. 30. P. 916–922.
11. Giusti B., Gori A. M., Marcucci R. et al. Relation of cytochrome P450 2C19 loss-of-function polymorphism to occurrence of drug-eluting coronary stent thrombosis // Am. J. Cardiol. 2009. Vol. 103. P. 806–811.
12. Shuldiner A.R., O’Connell J.R., Bliden K.P. et al. Association of cytochrome P450 2C19 genotype with the antiplatelet effect and clinical efficacy of clopidogrel therapy // JAMA. 2009. Vol. 302. P. 849–857.
13. Sandercock P.A.G., Counsell C., Tseng M.C., Cecconi E. Oral antiplatelet therapy for acute ischaemic stroke // Cochrane Database Syst. Rev. 2014. Vol. 3. CD000029.
14. Kahn S.R., Lim W., Dunn A.S. et al. Prevention of VTE in nonsurgical patients: antithrombotic therapy and prevention of thrombosis, 9th ed.: American College of Chest Physicians evidence-based clinical practice guidelines // Chest. 2012. Vol. 141 (2) (Suppl.). P. e195S-e226S.
15. Kennedy J., Hill M.D., Ryckborst K.J. et al. FASTER Investigators. Fast assessment of stroke and transient ischaemic attack to prevent early recurrence (FASTER): a randomised controlled pilot trial // Lancet Neurol. 2007. Vol. 6 (11). P. 961–969.
16. The European Stroke Organization (ESO) Executive Committee and the ESO Writing Committee: Guidelines for management of ischaemic stroke and transient ischaemic attacks 2008 // Cerebrovasc. Dis. 2008. Vol. 25. P. 457–507.
17. Sacco R.L., Adams R., Albert G. et al. Guidelines for prevention of stroke in patients with ischemic stroke or transient ischemic attack: a statement for healthcare professionals from the American Heart Association/American Stroke Association Council on Stroke: co-sponsored by the Council on Cardiovascular Radiology and Intervention: the American Academy of Neurology affirms the value of this guideline // Stroke. 2006. Vol. 37 (2). P. 577–617.
18. Lansberg M.G., O’Donnell M.J., Khatri P. et al. Antithrombotic and Thrombolytic Therapy for Ischemic Stroke: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed.: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines // Chest. 2012. Vol. 141 (2) (Suppl.). e601S-e636S.
19. Baigent C., Blackwell L., Collins R. et al. Antithrombotic Trialists’ (ATT) Collaboration. Aspirin in the primary and secondary prevention of vascular disease: collaborative meta-analysis of individual participant data from randomised trials // Lancet. 2009. Vol. 373 (9678). P. 1849–1860.
20. Rothwell P.M., Fowkes F.G.R., Belch J.F.F. et al. Effect of daily aspirin on long-term risk of death due to cancer: analysis of individual patient data from randomised trials // Lancet. 2011. Vol. 377 (9759). P. 31–41.
21. Rothwell P.M., Wilson M., Elwin C.-E. et al. Long-term effect of aspirin on colorectal cancer incidence and mortality: 20-year follow-up of five randomised trials // Lancet. 2010. Vol. 376 (9754). P. 1741–1750.
22. Vandvik P.O., Lincoff A.M., Gore J.M. et al. Primary and secondary prevention of cardiovascular disease: antithrombotic therapy and prevention of thrombosis, 9th ed.: American College of Chest Physicians evidence-based clinical practice guidelines // Chest. 2012. Vol. 141 (2) (Suppl.). e637S-e668S.
23. CAPRIE Steering Committee. A randomised, blinded, trial of clopidogrel versus aspirin in patients at risk of ischaemic events (CAPRIE) // Lancet. 1996. Vol. 348. P. 1329–1339.
24. Diener H.C., Cunha L., Forbes C. et al. European Stroke Prevention Study. 2. Dipyridamole and acetylsalicylic acid in the secondary prevention of stroke // J. Neurol. Sci. 1996. Vol. 143 (1–2). P. 1–13.
25. Halkes P.H., van Gijn J., Kappelle L.J. et al. ESPRIT Study Group. Aspirin plus dipyridamole versus aspirin alone after cerebral ischaemia of arterial origin (ESPRIT): randomised controlled trial // Lancet. 2006. Vol. 367 (9523). P.1665–1673 [erratum appears in Lancet. 2007. Vol. 369 (9558). P. 274].
26. Sacco R.L., Diener H.-C., Yusuf S. et al. PRoFESS Study Group. Aspirin and extended-release dipyridamole versus clopidogrel for recurrent stroke // N. Engl. J. Med. 2008. Vol. 359 (12). P. 1238–1251.
27. Diener H.-C., Bogousslavsky J., Brass L. M. et al. MATCH investigators. Aspirin and clopidogrel compared with clopidogrel alone after recent ischaemic stroke or transient ischaemic attack in high-risk patients (MATCH): randomised, double-blind, placebo-controlled trial // Lancet. 2004. Vol. 364 (9431). P. 331–337.
28. Chen D.K., Kim J.S., Sutton D.M. Thrombotic thrombocytopenic purpura associated with ticlopidine use: a report of 3 cases and review of the literature // Arch. Intern. Med. 1999. Vol. 159 (3). P. 311–314.
29. Sudlow C.L., Mason G., Maurice J.B. et al. Thienopyridine derivatives versus aspirin for preventing stroke and other serious vascular events in high vascular risk patients // Cochrane Database Syst. Rev. 2009. Vol. 4. CD001246.
30. Huang Y., Cheng Y., Wu J. et al. Cilostazol versus Aspirin for Secondary Ischaemic Stroke Prevention cooperation investigators. Cilostazol as an alternative to aspirin after ischaemic stroke: a randomised, double-blind, pilot study // Lancet Neurol. 2008. Vol. 7 (6). P. 494–499 [erratum appears in Lancet Neurol. 2008. Vol. 7 (8). P. 675].
31. Shinohara Y., Katayama Y., Uchiyama S. et al. CSPS 2 group. Cilostazol for prevention of secondary stroke (CSPS 2): an aspirin-controlled, double-blind, randomised non-inferiority trial // Lancet Neurol. 2010. Vol. 9 (10). P. 959–968.
32. Kamal A.K., Naqvi I., Husain M.R., Khealani B.A. Cilostazol versus aspirin for secondary prevention of vascular events after stroke of arterial origin // Cochrane Database Syst. Rev. 2011. Vol. 1. CD008076.
33. Costa J., Ferro J. M., Matias-Guiu J. et al. Triflusal for preventing serious vascular events in people at high risk // Cochrane Database Syst. Rev. 2005. Vol. 3. CD004296.
34. Bousser M.G., Amarenco P., Chamorro A. et al. PERFORM Study Investigators. Terutroban versus aspirin in patients with cerebral ischaemic events (PERFORM): a randomised, double-blind, parallel-group trial // Lancet. 2011. Vol. 377 (9782). P. 2013–2022.
35. Algra A., De Schryver E.L.L.M., van Gijn J. et al. Oral anticoagulants versus antiplatelet therapy for preventing further vascular events after transient ischaemic attack or minor stroke of presumed arterial origin // Cochrane Database Syst. Rev. 2006.Vol. (3). P. CD001342.
36. Баркаган З.С., Котовщикова Е.Ф. Сравнительный анализ основных и побочных эффектов различных форм ацетилсалициловой кислоты // Клиническая фармакология и терапия. 2004. № 13 (3). С. 1–4.
37. Верткин А.Л., Аристархова О.Ю., Адонина Е.В. и др. Безопасность и фармакоэкономическая эффективность применения различных препаратов ацетилсалициловой кислоты у пациентов с ИБС // РМЖ. 2009. № 17 (9). С. 570–575.
Только для зарегистрированных пользователей