клостридиоз у собак чем лечить
Клостридиоз
Клостридиоз – широко распространенное заболевание животных и людей, вызываемое различными видами и типами клостридий. В большинстве случаев люди заражаются через инфицированное мясо и мясные продукты. Животные заражаются через корма, повреждения на коже и слизистых.
Наиболее распространенные возбудители:
Другие виды клостридий вызывают ботулизм (C. botulinum), столбняк (С. teteni), газовую гангрену (C. sordellii), эмфизематозный карбункул (C. chauvoei). Различные типы C. novyi вызывают некротический гепатит и злокачественный отёк у овец, бациллярную гемоглобинурию и злокачественный отёк у КРС, хронический остеомиелит буйволов.
Болеют КРС, буйволы, МРС, свиньи, лошади. Встречается зараженная клостридиями рыба и цыплята.
Повсеместно распространенное заболевание. Чаще всего встречается в развивающихся странах и стоит в первой пятерке причин пищевых отравлений, в одном ряду с сальмонеллой и стафилококковыми инфекциями.
Клостридии входят в состав нормальной микрофлоры ЖКТ и представлены множеством типов от А до Е. Среди всех клостридий, наиболее опасным видом являются clostridium perfringens. Эти бактерии широко распространены в окружающей среде: в воздухе, почве, на растениях.
Сами по себе клостридии безобидны, не заразны и не опасны. Проблемы начинаются при снижении иммунитета, нарушениях в кормлении и содержании животных. Избыток крахмалов и других углеводов в рационе, порезы, внутренние или внешние абсцессы, всё что приводит к снижению кислорода в тканях и органах животного и провоцирует развитие клостридиоза.
Заражение происходит через пищу и воду или через ранки, порезы и воспаления на коже и слизистых.
Наибольшей опасности подвергаются молодые животные, у которых еще не полностью сформировался желудочно-кишечный тракт и кишечная микрофлора. Сlostridium perfringens питается крахмалом и сахарами, поэтому, когда в рационе идет избыток углеводов это провоцирует развитие заболевания. Особенно опасно включать в рацион много углеводов (рекомендуем ознакомиться со статьей «Углеводы в рационе скота»), когда животные испытывают стресс или у них снижена резистентность на фоне других заболеваний. Ослабленный иммунитет и стресс могут быть и самостоятельными причинами клостридиоза.
Триггер-фактором для развития клостридиоза может стать заражение печеночными двуустками.
Заболевание проявляется, когда в крови резко повышается уровень токсинов, выделяемых клостридиями. Особенно опасен альфа – токсин. От него животные могут испытывать шок, остановку сердца и даже умереть.
Вопрос окончательно не изучен, но есть предположение, что Сlostridiumperfringens типа А могут вызвать геморрагический кишечный синдром (HBS). Это острое, быстротекущее заболевание КРС, в основном, дойных коров, с летальностью 80 – 100%. Сlostridiumperfringens тип А, так же, является возбудителем некротизирующего мастита коров.
Заражение C. tetani может проявляться как гиперестезия (повышенная реакция на прикосновения), выпадением третьего века, ограниченным движением челюстей, ригидностью мышц и судорогами.
🔴Картина при вскрытии
Клинические патологические исследования и вскрытия редко помогают поставить точный диагноз. Картина может быть самая различная, в зависимости от вида и типа клостридий, путей заражения, количества бактерий. Типичными признаками можно считать геморрагический энтерит, изъязвления слизистой оболочки кишечника и признаки дизентерии. Но могут встречаться отеки, газы или эмфиземы, разложение почек, асфиксия, быстрое разложение туши. Сопутствующим признаком служит заражение печеночной двуусткой.
У овец с «черной ножкой» пораженная ткань будет иметь характерный темно – фиолетовый цвет и прогорклый запах.
Для каждого вида и типа клостридий есть патологоанатомическое описание, которое используется при диагностике.
Клостридии отличаются способностью быстро размножаться в тушах после забоя, что может помешать точному анализу. Посмертное исследование возможно исключительно на только что умерших животных.
Диагноз ставится на основе клинического течения болезни, истории заболеваний на ферме и данных о наиболее распространенных заболеваниях в регионе и лабораторных исследованиях.
При лабораторных исследованиях применяют иммуноферментный анализ, посев и ПЦР метод.
При первых признаках клостридиоза хорошо работают антибиотики пенициллинового ряда. Обычно, их комбинируют с обезболивающими.
В случае, когда заболевание уже несколько запущено, применяют сильные антибиотики в сочетании с внутривенным капельным введением большого количества жидкости.
Для усиления перистальтики кишечника используют касторовое масло.
При болях в кишечнике и слабой диарее, чтобы не уничтожать естественную микрофлору антибиотиками, применяют каолин + пектин, пептобисамол или минеральное масло. Но если заболевание прогрессирует, необходимо немедленно сделать инъекцию сильного антибиотика.
Вакцинация. Используется инактивированная вакцина, соответствующая наиболее опасному типу клостридий или комбинированные вакцины. При выборе вакцины необходимо проконсультироваться с государственным ветврачом.
Для молодняка рекомендуется двукратная вакцинация с перерывом 4 – 6 недель. Возраст вакцинируемых животных и дозировка зависят от иммунного статуса матери и степени риска заражения. Рекомендуем ознакомиться со статьей «Схема вакцинации телят». Чтобы мать с молозивом передала антитела пассивного иммунитета потомству, её необходимо своевременно провакцинировать.
К мерам профилактики можно отнести запрет на выпас животных на зараженных пастбищах. Необходимо максимально очистить пастбище от острых и колющих предметов. Изолировать животных с ранами, абсцессами и другими повреждениями кожи.
Clostridium difficile
Разговор о клостридиях был бы неполным без самого внутрибольничного представителя оных — Clostridium difficile.
Автор: Трубачева Е.С., врач – клинический фармаколог
Разговор о клостридиях был бы неполным без самого внутрибольничного представителя оных — Clostridium difficile. К тому же сейчас самый подходящий случай о нем вспомнить, так как всевозможные схемы, в том числе и антибактериальной терапии, в лечении вирусных пневмоний, вызванных SARS-CoV-2, в перепрофилированных больницах могли еще сильнее натренировать внутрибольничную микрофлору, в состав которой и входит вышеупомянутая клостридия.
В настоящее время токсигенные штаммы C.difficile рассматриваются как однозначные возбудители внутрибольничных инфекций. То есть вызываемый ими псевдомембранозный колит является заболеванием, связанным с оказанием медицинской помощи, то есть ятрогенным. А все мы знаем, как Следственный Комитет к этому относится и, что самое главное, останавливаться не собирается (согласно последнему интервью председателя СК А. Бастрыкина). Поэтому необходимо максимально подробно разораться, как данное заболевание вызывается, что его провоцирует и как этого если не избежать, то максимально эффективно пролечить. Об этом и будет нынешний разговор.
Микробиологические аспекты
C.difficile, как и остальные клинически значимые клостридии, является строгим анаэробом. Основным поражающим фактором для нее, так же как и для остальных клостридий, являются токсины, и так же, как и другие клостридии, C.difficile умеет образовывать споры. Заболевание, вызываемое токсигенной C.difficile, именуется псевдомембранозным колитом.
Теперь отметим частности:
Эпидемиологические аспекты
Основным источником токсигенных C.difficile является либо больной, либо здоровый носитель. Путь распространения — фекально-оральный либо контактный. Так как споры C.difficile благополучно сохраняются до 180 суток, то некоторые вспышки могут происходить без видимо определяемого источника — достаточно плохо убранных туалетных помещений стационаров, а также давно или неправильно обработанных матрасов. Кроме того, если вдруг в отделении оказался бессимптомный носитель C.difficile из числа медицинского персонала, а остальные не особенно привыкли мыть руки, то эти самые споры будет разносить каждый второй сотрудник уже не отделения, а всей больницы — на руках, халатах, смартфонах, рассаживая ее по столам, перилам и клавиатурам, совершенно бессимптомно для себя, но с катастрофическими последствиями для больных.
Почему именно стационары? Потому что именно здесь используется самое большое количество антибактериальных препаратов, в том числе не всегда обоснованно, и C.difficile может получить селективное преимущество ввиду уменьшения количества бактерий-антагонистов, ранее сдерживавших ее размножение и токсиновыделение.
В каких отделениях чаще всего возможны случаи (или даже целые вспышки) псевдомебранозных колитов?
Поэтому если ваш пациент в течение недавнего прошлого оказывался по какой-либо причине в одном из таких отделений, то надо иметь в виду риск возможного носительства токсигенных C.difficile и развития ПМК в случае назначения антибиотиков.
Какие антибиотики чаще всего провоцируют рост количества тоскигенных C.difficile и развитие псевдомембранозного колита?
Проще говоря, то, что выбивает из толстой кишки основных конкурентов C.difficile, то и обеспечивает высокие риски развития ПМК. Но, помимо антибиотиков, ПМК провоцируют и цитостатические препараты, такие, как, например, препараты платины и метотрексат.
Какие пациенты подвергаются риску заражения токсигенной C.difficile и развитию ПМК? Чаще всего это изначально тяжелые пациенты с ожогами, после операций на толстом кишечнике, пациенты с почечной недостаточностью и любые пациенты, находящиеся в отделениях реанимации и интенсивной терапии. А пациенты с ВИЧ почему-то показывают статистику, аналогичную основной популяции — не больше и не меньше.
Исходя из всего сказанного, главным в деле сдерживания C.difficile является профилактика, краеугольным камнем которой стоит эпидемиологический надзор. Только тотальная чистота рук, туалетных комнат, как у пациентов, так и персонала, а также строжайшее выполнение требований СанПина, особенно в лечебных учреждениях, уже столкнувшихся с этим зверем, способна предотвратить новые случаи. Напомню, что летальность при псевдомембранозном колите — более 50%, а при развившемся токсическом мегаколоне — 100%.
Клинические аспекты
Основная проблема, связанная с C.difficile, — это ее диагностика. С одной стороны, все просто — давно есть коммерческие тест-системы, позволяющие проведение экспресс-тестов для обнаружения токсинов, с другой — ну и кто, положа руку на сердце, хоть раз в живую их видел? Автор за 15 лет работы не видела ни разу. Микробиологическая же диагностика требует наличия в лаборатории не только анаэробного анализатора, но еще и специально обученного бактериолога. И где всю эту роскошь взять? Вот и приходится практическому врачу ставить диагноз исходя из клинических проявлений, не забывая о дифдиагностике с другими возможными инфекционными заболевания толстого и тонкого кишечника (про которые мы уже написали в более ранних статьях: см. здесь, здесь и здесь). Кроме того необходимо думать о внутрибольничных кишечных инфекциях, которые тоже никто не отменял (хотя и давно не видел).
При этом нужно помнить и об антибиотик-ассоциированных диареях, ничего общего с ПМК и C.difficile не имеющими и объясняющимися исключительно фармакодинамикой назначенных препаратов. Например, диарея, связанная с приемом амоксициллина/клавуланата вызвана тем, что метаболиты оного стимулируют моторику толстой кишки, или макролиды, действующие на мотилиновые рецепторы и вызывающие точно такую же диарею. А уж когда эти два препарата назначены в комбинации, как любят делать в амбулаторной практике, то антибиотик-ассоциированная диарея не прилетит только к самым стойким пациентам. Кстати, если до сих пор не предупреждаете пациентов об этом чрезвычайно слабительном эффекте — то начинайте. Но, повторимся, к C.difficile это все не имеет совершенно никакого отношения. Почти всегда амбулаторные состояния решаются заменой препарата на что-то менее агрессивное в отношении кишечника и пересмотром сопутствующей терапии (например, там могут оказаться еще и НПВС, которые тоже способны провоцировать диарею).
Чем же диарея при инфицировании C.difficile отличается от всего остального? Четкой связью с госпитализацией и началом приема антибиотиков, особенно если пациент за пару месяцев до попадания к нам в руки побывал на госпитализации в ранее указанных отделениях. Если на третий день после назначения, например, цефтриаксона у такого пациента развилась диарея, тут же должен прозвучать тревожный звоночек. Если есть доступ к экспресс-тестам — определить наличие токсинов, если нет, то сразу отменять антибиотик. Если необходимость в антибактериальной терапии все еще существует, менять его на препарат из безопасного перечня. Бета-лактамы не назначать! Никакие! До выяснения происходящего с пациентом. За самим пациентом в это время (сутки, максимум двое) необходимо очень внимательно наблюдать и ни в коем случае не назначать никаких препаратов, снижающих моторику кишечника.
Если смена антибактериального препарата ничего в состоянии пациента не изменила, количество эпизодов диареи тоже нарастает или начинает пальпироваться напряженная толстая кишка, то речь может идти уже о псевдомембранозном колите, подтвердить который можно эндоскопическими методами, где в заключении будет указано наличие характерных псевдомембран на отдельных участках или всем протяжении толстой кишки, доступной к осмотру.
Чем и как лечить?
В чем преимущество метронидазола? Он не вызывает селекции резистентных штаммов энтерококков (об энтерококках мы рассуждали здесь), более доступен и в разы дешевле даже самого дешевого ванкомицина. При этом в связи с бесконтрольным его использованием на любой случай диареи образовал уже довольно приличный пул штаммов C.difficile, к нему устойчивых, поэтому метронидазол не стоит назначать пациентам, у которых уже наблюдались эпизоды внутрибольничных диарей, им же леченные, так как не факт, что перед вами не окажется пациент с уже перенесенным эпизодом ПМК, которому вегетативные C.difficile выбили, а споры устойчивых форм именно сейчас дождались своего часа.
Клостридии. Всегда рядом, всегда начеку
Ботулизм, столбняк, газовая гангрена… Об этих заболеваниях наслышаны если не все, то очень многие люди. Но если от столбняка существуют вакцины, например АКДС (адсорбированная коклюшно-дифтерийно-столбнячная сыворотка), то от псевдомембранозного колита, некротического энтерита, ботулизма или газовой гангрены таких вакцин нет. А вызываются все эти заболевания бактериями рода Clostridium.
Одним из наиболее распространенных видов клостридий является Clostridium difficile. Ее высевают из почвы, воды (в том числе и морской). Благодаря возможности образовывать эндоспоры (покрываться оболочкой и переживать неблагоприятный период в состоянии своеобразной «спячки») этот вид может длительно, до двух месяцев, сохраняться во внешней среде. Более того, в состоянии эндоспоры клостридия диффициле выдерживает даже кипячение. Чувствительность к антибиотикам у Clostridium difficile от природы очень низкая, поэтому лечение посредством антибиотикотерапии зачастую терпит фиаско.
Clostridium difficile входит в нормофлору (является представителем нормального микробного состава) желудочно-кишечного тракта, обитая преимущественно в толстом кишечнике. Хотя отдельные его представители встречаются и во рту, и в тонком отделе кишечника, и во влагалище у женщин. Чаще всего Clostridium difficile обнаруживается в кишечнике новорожденных (около половины младенцев), а из детей старше 2 лет и взрослых каждый 10 является обладателем этой бактерии.
Clostridium difficile вызывает такие заболевания как псевдомембранозный колит и антибиотикоассоциированные диареи. Патогенные (болезнетворные) свойства этой клостридии обусловлены выделением токсинов А и В, а также белка, угнетающего перистальтику (сократительную функцию) кишечника.
Антибиотикодиссоциированные диареи (сокращенно – ААД) могут вызываться не только клостридией дифициле, а и множеством других микроорганизмов (сальмонеллами, кандидами, клостридией перфрингенс, золотистым стафилококком, клебсиеллой). Этот вид диарей является наиболее частой внутрибольничной инфекцией и связана такая тенденция с тем, что в больницах, во-первых, концентрируется большая масса больных и здоровых людей. А во-вторых, здесь используется множество антибиотиков и дезинфицирующих средств, которые способствуют образованию генераций (поколений) микроорганизмов, устойчивых к антибиотикам. Поэтому в мире ежегодно регистрируется около миллиона случаев ААД. Возникновение антибиотикоассоциированных диарей связано с тем, что антимикробные препараты подавляют как патогенную, так и нормальную микрофлору. Даже однократный прием антибиотиков широкого спектра действия может послужить причиной развития ААД.

Несмотря на это, дети младенческого возраста практически не болеют антибиотикоассоциированными диареями, вызываемыми клостридией диффициле. Связано это с тем, что дети получают с материнским молоком достаточно иммунных факторов, которые могут сдерживать размножение Clostridium difficile. Более того, в младенческом организме нет такого количества сопутствующей условно-патогенной микрофлоры, которая ослабляет иммунитет.
Антибиотикозависимые диареи могут иметь разную симптоматику и течение: от легкой диареи до тяжелейшего псевдомембранозного энтероколита (ПМК). Последний чаще всего вызывается именно клостридией диффициле.
В процессе течения заболевания отмечаются следующие симптомы:
При отсутствии лечения количество смертельных случаев составляет до 30 %.
Характерная особенность болезней, вызванных Clostridium difficile, является то, что около четверти случаев через время повторяются (рецидив заболевания). Причиной этого явления становятся споры клостридий, которые переживают период лечения, либо повторное заражение. Как правило, после лечения больные выздоравливают, или чувствуют себя значительно лучше, но спустя несколько дней (от 3 до 7) развивается рецидив.
Еще одна клостридия, которая может вызывать такие болезни желудочно-кишечного тракта, как пищевые токсикоинфекции и некротический энтерит, — Clostridium perfringens.
Некротический энтерит характеризуется формированием язв и эрозий и деструктивными (разрушающими) изменениями в слизистой оболочке. Первым симптомом заболевания является возникновение участков геморрагического некроза в начальных отделах тощей кишки. Эти участки имеют красный цвет. Наблюдается также сужение просвета кишечника в месте воспаления, за счет отечности стенки. Происходит тромбоз (закупорка) мелких кровеносных сосудов (артериол). У больного отмечаются озноб и лихорадка, рвота и кровавый пенистый понос.
Clostridium perfringens производит ферменты, расщепляющие белки (протеиназа), коллаген (коллагеназа), гиалуроновую кислоту (гиалуронидаза).

Профилактика заболеваний, причиной которых являются клостридии, в первую очередь заключается в соблюдении санитарно-гигиенических норм и правил: мытье и ошпаривание овощей и фруктов; длительная термическая обработка. Но немаловажным является также нормализация микрофлоры и укрепление иммунитета. Причем, как в процессе лечения, так и в процессе предупреждения этих болезней. Ограниченное и строго подконтрольное врачам применение антибиотиков, отказ от самолечения также очень важны для профилактики возникновения АДД и других болезней, связанных с клостридиями.
Клостридиозы (гангренозный дерматит, некротический и язвенный энтерит)
Клостридии – это грамположительные анаэробные бактерии, относящиеся к семейству Bacillaceae, роду Clostridium. Являются возбудителями антропозоонозной инфекции, характеризующейся клиническими проявлениями разной степени выраженности.
Гангренозный дерматит
Синонимы: клостридиальный дерматит, некротический дерматит, гангренозный целлюлит, гангренозный дерматомиозит, злокачественный отек птиц, газовый отек.
К данному заболеванию в основном восприимчивы птицы мясных и мясояичных пород 4–8-недельного возраста, реже – 16–20-недельного.
Передача осуществляется горизонтальным (преимущественно алиментарным) и контактным (через поврежденные кожные покровы и слизистые оболочки) путями.
Первое звено – возбудитель заболевания. Возбудителями гангренозного (от греч. ганграйно – пожар) дерматита являются бактерии Clostridium perfringens и Clostridium septicum. Возможна также комбинация клостридий с золотистым стрептококком, при этом тяжесть протекания гангренозного дерматита усиливается.
Источником и распространителем инфекции служат больные и переболевшие птицы, а также корм, вода, подстилочный материал, частички пыли, помет.
Второе звено – ворота инфекции. Представляют собой место проникновения возбудителя через слизистые оболочки пищеварительного тракта и поврежденную кожу.
Третье звено – патогенное воздействие возбудителя гангренозного дерматита.
Развитию данного заболевания могут способствовать инфекционная бурсальная болезнь (исследователи считают, что отсутствие антител к ИББ у цыплят-бройлеров напрямую связано с чувствительностью их потомков к дерматитам), вирусная анемия цыплят, аденовирусы, реовирусы, кокцидии и др.
Гангренозный дерматит относится к тем немногим заболеваниям, постановка предварительного диагноза которых основывается на наличии клинических признаков, поскольку патологические изменения выражены незначительно и не являются патогномоничными.
У заболевших особей развивается депрессия, нарушается координация движений, снижается аппетит, возникает слабость ног.
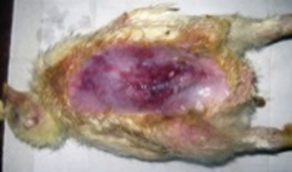
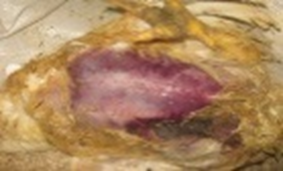
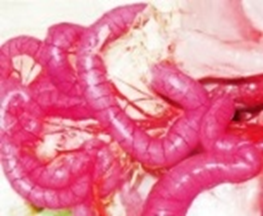
Вследствие гнилостного воспаления пораженные участки кожи (преимущественный тропизм выражен именно к тканям кожи и подкожной клетчатке) выглядят темными вследствие изменения кровяного пигмента, что придает омертвевшему участку фиолетово-синеватую или черную окраску (рис. 1), и влажными – по причине разложения ткани гнилостными организмами. В отечных участках кожа собрана в складки из-за оказываемого на нее кровянистой жидкостью давления (рис. 2).
Рис. 1. Гангренозный дерматит. Омертвевшая кожа имеет фиолетово-синеватую окраску
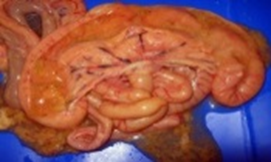
Рис. 2. Гангренозный дерматит. В отечных участках кожа собирается в складки
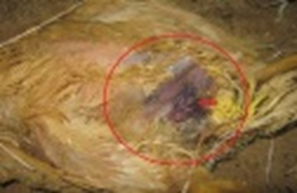
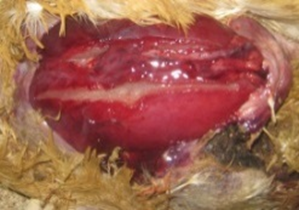
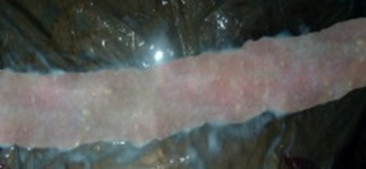
Под поврежденной кожей обнаруживаются обширные отеки кровянистого цвета, при этом глубокие слои мышц не затрагиваются (рис. 3).
Рис. 3. Гангренозный дерматит. Наличие обширных отеков кровянистого цвета под поврежденной кожей
В некоторых случаях в подкожной клетчатке может отмечаться наличие газа или серозно-геморрагической жидкости.
Четвертое звено – выделение бактерий из организма птиц во внешнюю среду. В основном осуществляется с пометом.
Некротический энтерит
Синонимы: анаэробная энтеротоксемия, клостридиозный энтерит.
Первое звено – возбудитель заболевания. Возбудителями некротического энтерита являются спорообразующие бактерии Clostridium perfringens (грамположительные анаэробы), вырабатывающие энтеробактериальные токсины, которые обуславливают патогенность данных микроорганизмов.
К данному заболеванию чаще всего восприимчив молодняк кур мясных пород, реже – индюшата.
У цыплят-бройлеров основным видом клостридий, вызывающих заболевание, является Clostridium perfringens типа А (продуцирует ɑ-токсины) и – в редких случаях – типа С (продуцирует ɑ- и β-токсины). ɑ-Токсин представляет собой фосфолипазу, которая гидрализует фосфолипиды и сфингомиелин, вызывающий дезорганизацию мембраны и геморрагический энтерит.
Источником и распространителем инфекции служат больные и переболевшие птицы.
Передача осуществляется через корма, воду, подстилку, инвентарь, обслуживающий персонал, помет.
Второе звено – ворота инфекции. Желудочно-кишечный тракт (алиментарный путь).
Третье звено – патогенное воздействие возбудителя некротического энтерита.
У здоровых цыплят клостридии локализуются в основном в толстом отделе кишечника (к которому относятся слепые отростки и прямая кишка), не вызывая каких-либо патологических изменений. Но данная ситуация будет сохраняться только до тех пор, пока имеются необходимые для этого условия: присутствие в кишечнике кислорода, предотвращающего размножение анаэробов, нормальная перистальтика, низкие значения рН в железистом желудке и тонком отделе кишечника. Отметим, что бокаловидные клетки, секретирующие муцин, при колонизации кишечника цыплят Clostridium perfringes начинают производить вместо нейтральных молекул – кислые, что указывает на попытку организма выровнять оптимальное значение рН.
Из всего изложенного выше можно сделать вывод, что одного лишь присутствия клостридий для возникновения некротического энтерита недостаточно, обязательно требуется наличие каких-либо сопутствующих факторов*, приводящих к созданию благоприятных условий для интенсивного роста, размножения Clostridium perfringes и последующего токсинообразования. Токсины клостридий разрушают слизистую оболочку кишечника и эритроциты крови, в некоторых случаях затрудняют передачу нервных импульсов к сердцу и легким, что выражается внезапной гибелью птицы без предварительных клинических признаков.
* К сопутствующим факторам относятся:
Также при визуальном осмотре молодняка у некоторых особей отмечаются депрессивное состояние (птицы ложатся на подстилку и вытягивают шею), взъерошенность оперения, диарея (в помете отмечается присутствие крови), сменяющаяся запором. Смертность при некротическом энтерите составляет от 5 до 20 %.
У взрослых несушек снижается продуктивность, по причине чего они не в состоянии выйти на пик яйценоскости, но процент падежа может оставаться в пределах нормы.
В зависимости от стадии патологического процесса характер повреждений может варьироваться.
1. В кишечнике появляются небольшие покраснения возле кровеносных сосудов и некротизированные (синеватого цвета) участки (от небольших, в виде точек, до обширных, на всем протяжении кишечного тракта). Данные поражения можно рассмотреть со стороны серозной оболочки кишечника (со стороны слизистой оболочки обнаруживаются кровоизлияния различной степени интенсивности).
Некротический энтерит всегда протекает в ассоциации с субклиническим или клиническим кокцидиозом (рис. 4).
Рис. 4. Ассоциативное протекание некротического энтерита и кокцидиоза
2. В просвете кишечника обнаруживаются водянистые массы, смешанные с пузырьками газа, отрубевидный налет (рис. 5).
3. В просвете кишечника могут находиться фибрин и клеточная ткань (рис. 6) либо его слизистая оболочка может быть покрыта свободно или плотно прилегающей коричнево-оранжевой, желтой или зеленой псевдомембраной, по виду напоминающей махровое полотенце или кору дерева (рис. 7).
Рис. 5. В просвете кишечника отмечается отрубевидный налет, приводящий к прекращению пищеварительной функции кишечника. Некроз слизистой оболочки кишечника в дальнейшем переходит в фибринонекротический энтерит
Рис. 6. Фибринонекротический энтерит (в просвете кишечника находятся фибрин и клеточная ткань)
Рис. 7. Фибринонекротический энтерит. Слизистая оболочка кишечника покрыта свободно или плотно прилегающей желтой или зеленой псевдомембраной (дифтерической мембраной «махровое полотенце»)
В толстом отделе кишечника отмечается вздутие слепых отростков вследствие сильного газообразования и скопление непереваренных частичек корма в прямой кишке.
Печень увеличенная, от темно-красного до черного цвета, иногда в ней обнаруживаются множественные некротические очажки.
Четвертое звено – выделение бактерий из организма птиц во внешнюю среду. Осуществляется с пометом
Язвенный энтерит
Синонимы: анаэробный энтерит, некротизирующий энтерит.
Первое звено – возбудитель заболевания. Возбудителем язвенного энтерита является бактерия Clostridium colinum (грамположительный анаэроб).
К данному заболеванию наиболее восприимчивы перепела, а также цыплята (в возрасте 21–56 дней), индюшата (в возрасте 28–84 дней), взрослые куры и индейки.
Источником и распространителем инфекции служат больные птицы, зараженный корм, вода, подстилка, помет, предметы ухода и оборудование, обслуживающий персонал.
Второе звено – ворота инфекции. Желудочно-кишечный тракт.
Третье звено – патогенное воздействие возбудителя язвенного энтерита. Исследователями отмечено, что данное заболевание чаще всего регистрируется после возникновения кокцидиоза, вирусной анемии цыплят, инфекционной бурсальной болезни, реовирусной инфекции, после воздействия различных стресс-факторов, приводящих к снижению естественной резистентности организма птиц и как следствие – к обширному язвенному некрозу слизистой оболочки кишечника.
Клинические признаки, отмечаемые при язвенном энтерите, включают в себя: скучивание птицы (признак, указывающий на возникновение в стаде любого заболевания), угнетенное состояние, отказ от корма при повышенном потреблении воды, диарею (помет жидкий, светло-шоколадного цвета, с примесью уратов).
Патолого-анатомические изменения: при вскрытии птиц наиболее характерным изменением, которое и послужило основанием для названия данной болезни, является наличие язв в кишечнике (в основном располагающихся в его тонком отделе), в железистом желудке (язвы эллипсоидной или круглой формы) и в слепых отростках (язвы могут быть кратерообразной формы).
В самом начале заболевания данные поражения представлены небольшими желтыми очажками (иногда они сливаются между собой в большие некротическо-дифтерические очаги) с геморрагическим ободком, который по мере разрастания язвы исчезает. Язвы могут как глубоко внедряться в слизистую оболочку, так и быть поверхностными, т. е. выступать над слизистой оболочкой. При прободении (перфорации) кишечной стенки возникает перитонит.
В печени тоже встречаются рассеянные очажки некрозов, иногда окруженные бледно-желтым ореолом.
Четвертое звено – выделение бактерий из организма птиц во внешнюю среду. Осуществляется с пометом.
Диагностика, лечение и профилактика клостридиозов
Пятое звено – постановка диагноза. Диагноз основывается на результатах эпизоотологических, клинических, патолого-морфологических, серологических и бактериологических исследований.
Для диагностики клостридиозов в ветеринарную лабораторию направляется следующий материал:
Шестое звено – лечение и профилактика. При подозрении на клостридиоз, а также на смешанные инфекции целесообразно проводить антибиотикотерапию теми лекарственными формами препаратов, к которым предварительно определена чувствительность у выделенных возбудителей заболеваний.
| Действующее вещество | Группа | Спектр действия | Доза |
|---|---|---|---|
| Цинк бацитрацин (продуцируется Bacillus licheniformis) | Относится к группе полипептидных антибиотиков | Clostridium spp.(активен в отношении грамположительных микроорганизмов, на грамотрицательные практически не действует) | 0,5–1 кг на 1 т корма. При содержании в 1 г препарата 100 мг действующего вещества (10 %). 0,33–0,66 кг на 1 т корма. При содержании в 1 г препарата 150 мг действующего вещества (15 %) |
| Цефалексин (бактерицид) Трудно растворим в воде, практически нерастворим в спирте | Цефалоспориновый антибиотик I поколения | Clostridium spp., Salmonella spp., Escherichia coli, Staphylococcus spp., Streptococcus spp., Klebsiella spp. | 0,2–0,4 г на 1 л воды; в течение 3–5 дней; 0,4–0,8 г на 1 кг корма. При содержании в 1 г препарата 500 мг действующего вещества (50 %) |
| Окситетрациклина гидрохлорид (бактериостатик) водорастворимый | Природный антибиотик I поколения тетрациклиновой группы | Clostridia spp., Staphylococcus spp., Streptococcus spp., Еsсherichia coli, Salmonella spp., Mycoplasma spp. Klebsiella spp., Haemophilus spp., Rickettsia spp., Chlamydia spp., | 5 г на 1 л воды в течение 3–5 дней. При содержании в 1 г препарата 200 мг действующего вещества (20 %) |
| Доксициклина гиглат (бактериостатик) водорастворимый | Полусинтетический антибиотик тетрациклиновой группы | Clostridium perfringens, Staphylococcus spp., Streptococcus spp., Еsсherichia coli, Salmonella spp., Haemophilus spp., Pasteurella spp., Chlamydia spp., Mycoplasma spp., | 1 мл на 1 л воды в течение 3–5 дней. При содержании в 1 мл раствора 100 мг действующего вещества (10 %). 1 г на 2 л воды, в течение 3–5 дней. При содержании в 1 г препарата 200 мг действующего вещества (20 %). 1 г на 5 л воды, в течение 3–5 дней. При содержании в 1 г препарата 500 мг действующего вещества (50 %) |
| Ципрофлоксацина гидрохлорид (бактерицид) водорастворимый | Фторхинолон II поколения | Clostridium spp. Haemophilus spp., Mycoplasma spp., Pasteurella sp., Proteus spp., Klebsiella spp., Salmonella sp., Campylobacter spp., Staphylococcus sp. (St. aureus), Streptococcus sp., Pseudomonas aeruginosa, Еsсherichia coli | 0,5–1 мл на 1 л воды в течение 3–5 дней. При содержании в 1 мл препарата 100 мг действующего вещества (10 %) |
| Флумеквин (бактерицид)водорастворимый | Фторхинолон II поколения | Clostridia spp., Haemophilus spp., Salmonella spp., Еsсherichia coli, Pasteurella spp., Staphylococcus spp., Pseudomonas spp., Proteus spp., Klebsiella spp., Yersinia spp. | 0,45–0,9 мл на 1 л воды в течение 3–5 дней. При содержании в 1 мл препарата 200 мг действующего вещества (20 %) |
| Левофлоксацин (бактерицид) водорастворимый | Фторхинолон III поколения | Clostridium perfringens, Salmonella spp., Pasteurella spp., Еsсherichia coli, Staphylococcus spp., Streptococcus spp., Pseudomonas aeruginosa, Mycoplasma spp. | 0,5 мл на 1 л воды в течение 3–5 дней. При содержании в 1 мл препарата 100–150 мг действующего вещества (10–15 %) |
| Энрофлоксацина гидрохлорид (бактерицид) водорастворимый | Фторхинолон III поколения | Clostridium spp., Staphylococcus spp., Streptococcus spp., Еsсherichia coli, Pasteurella spp., Klebsiella spp., Haemophilus spp., Proteus spp., Mycoplasma spp., Chlamydia spp. | 0,5–1 мл на 1 л воды в течение 3–5 дней. При содержании в 1 мл препарата 100 мг действующего вещества (10 %) |
| Ацетилизовалерил – тилозин бактериостатик) водорастворимый | Макролидный антибиотик из группы тилозина | Clostridia perfringens, Mycoplasma spp., Ornithobacterium rhinotracheale | 25 г препарата на 400 л питьевой воды в течение 3–5 дней. При содержании в 1 г препарата 1 г действующего вещества |
| Тилмикозина фосфат (бактериостатик) водорастворимый | Модифицированный макролидный антибиотик пролонгированного действия | Clostridia spp., Mycoplasma spp., Ornithobacterium rhinotracheale, Haemophilus spp., Staphylococcus spp., Streptococcus spp., Pasteurella spp., Spirochaeta spp., Chlamydia spp. | 0,3 мл на 1 л воды в течение 3–5 дней. При содержании в 1 мл препарата 250 мг действующего вещества (25 %) |
| Тилозин тартрат (бактериостатик) водорастворимый | Макролидный антибиотик | Clostridia spp., Mycoplasma spp., Ornithobacterium rhinotracheale, Haemophilus spp., Staphylococcus spp., Streptococcus spp., Pasteurella spp., Spirochaeta spp., Chlamydia spp., Klebsiella spp., Rickettsia spp. | 0,5 г препарата на 1 л воды в течение 3–5 дней; 0,3–0,5 г на 1 кг корма в течение 3–5 дней; аэрозольно 75–150 г на 1 000 м3 с добавлением 10 % глюкозы (от объема раствора) в течение 30 мин., 2–3 дня |
| Спирамицина адипат (бактериостатик) Трудно растворим в воде и легко – в большинстве органических растворителей | Макролидный антибиотик II поколения, короткого действия | Clostridium spp., Staphylococcus spp., Streptococcus spp., Pasteurella spp., Mycoplasma spp., Haemophilus spp., Rickettsia spp. | 1 г на 10 кг массы тела в течение 3–5 дней. При содержании в 100 г препарата 150 млн МЕ действующего вещества При использовании в высоких дозах может действовать бактерицидно в отношении более чувствительных штаммов. |
| Тиамулина гидроген фумарат (бактериостатик) водорастворимы | Полусинтетический антибиотик группы плевромутилинов | Clostridia spp., Mycoplasma spp., Ornithobacterium rhinotracheale, Haemophilus spp., Staphylococcus spp., Streptococcus spp., Pasteurella spp., Klebsiella spp. | 0,55 г на 1 литр воды, в течение 3–5 дней. При содержании в 1 г препарата 450 мг действующего вещества (45 %) |
Автор Д. Н. Хлып, независимый ветеринарный врач-консультант по птицеводству, г. Прохладный, Кабардино-Балкарская Республика