комедокарцинома молочной железы что это такое у женщин
Карцинома молочных желез – это злокачественное новообразование, отличающееся быстрым ростом и метастазированием.
Карцинома молочных желез – это злокачественное новообразование, по-другому рак груди, образующееся из эпителиальных клеток железистой ткани. Опухоль отличается быстрым ростом и метастазированием, высоким уровнем агрессивности, образованием токсичных веществ, которые отрицательно сказываются на общем состоянии всего организма.
Заболевание чаще всего встречается после 50-ти лет, но в последние десятилетия растет среди более молодых женщин (30-40 лет).
Как развивается рак молочных желез?
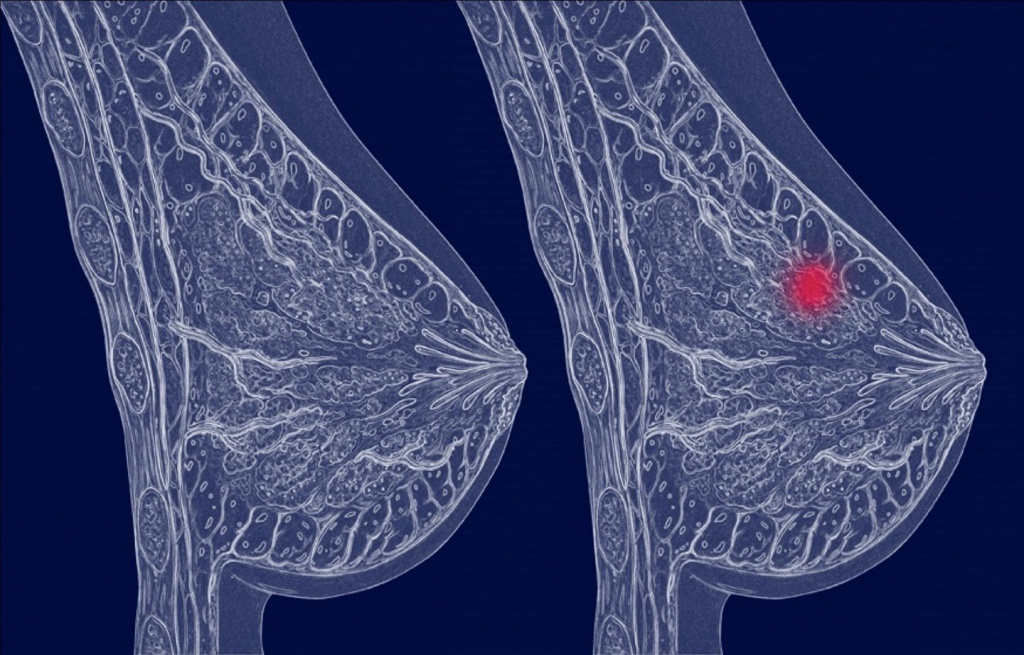
Клетки, из которых состоит грудь, в норме упорядоченно обновляются – на смену отмершим появляются новые. При озлокачествлении клеток этот процесс теряет контроль – устаревшие клетки не отмирают, а накапливаются в молочной железе. Раковые клетки начинают метастазировать в другие органы, где образуются новые очаги рака. Местом начала развития карциномы обычно становится молочная долька или проток – путь вывода молока (внутрипротоковая карцинома молочной железы).
Факторы риска развития карциномы
Точные причины развития карциномы молочной железы не выяснены, как и других типов рака. Однако существуют статистические данные о факторах риска возникновения данной патологии:
Симптомы рака груди
Первым симптомом обнаружения карциномы молочной железы является уплотнение в груди. Поэтому для своевременного обнаружения онкологии груди каждой женщине необходимо проводить самообследование – прощупывать ткани молочных желез на предмет уплотнений и узелков, оценивать симметричность, размер груди, состояние сосков и кожи.
Насторожить также должны:
При переходе карциномы на более поздние стадии (2-3) отмечаются общеспецифические симптомы рака: повышенная температура, слабость, усталость, одышка, снижение иммунитета, боли в костях и других органах, связанные с метастазированием.
Стадии карциномы молочной железы
Выделяют 4 стадии протекания заболевания:
Диагностика
Первое диагностическое действие врача – это пальпация, после чего при обнаружении уплотнения назначаются инструментальные и лабораторные обследования:
Лечение карциномы молочной железы
Лечение рака груди всегда комплексное – хирургическое вмешательство плюс химио- и радиотерапия в до- и послеоперационный периоды.
Операция
Самым эффективным при карциноме является хирургическое лечение. Наиболее щадящая операция – лампэктомия (удаление пораженных тканей груди). В результате молочная железа сохраняется, удаляется сама опухоль с близлежащими структурами. Мастэктомия – это радикальная операция, полное удаление одной или обоих молочных желез. В некоторых случаях возможно ее сочетание с пластической хирургией (реконструкция форм груди имплантами).
Химиотерапия
Назначается до и часто после операции, чтобы уменьшить вероятность образования метастазов и замедлить рост опухоли. Суть – приостановка деления клеток в организме, как раковых, так и здоровых. Показанием для химиотерапии также является неоперабельная карцинома. Химиотерапия всегда сопровождается неприятными побочными эффектами (выпадение волос, тошнота и рвота, угнетение иммунитета, депрессивные состояния), однако она необходима. Все побочные эффекты – лишь временны.
Лучевая терапия
Лучевая терапия представляет собой облучение высокоэнергетическими радиоактивными частицами. Ее цель – устранение злокачественных клеток, которые могли остаться в организме, путем уничтожения сосудов, подпитывающих опухоль. Чаще применяется спустя месяц после операции, однако может назначаться и до. Среди побочных эффектов – раздражение кожи в месте облучения, гиперпигментация кожи, застой лимфы.
Врачи Университетской клиники МГУ им. М.В. Ломоносова в работе
Карцинома молочных желез – прогноз
Выживаемость при онкологии молочной железы зависит от стадии заболевания, индивидуальных особенностей больного (возраст, наличие других болезней, общее состояние) и вида рака груди – существует карцинома молочной железы неспецифического типа, лечение и прогноз для которой немного отличаются.
Онкологи пользуются понятием «5-летней выживаемости» при разных стадиях рака, сформированным благодаря статистике. Оно означает, что в течение 5-ти лет с постановки диагноза (не развития самой болезни) рака пациент не умер. После истечения этого периода вступает в действие следующий показатель – 10-летняя выживаемость. Если на протяжении 10-ти лет пациент остается в полной ремиссии, и признаки рака никак не проявляются, врачи обычно говорят о полном излечении.
Каждый человек и протекание его болезни индивидуально, и данные цифры дают лишь примерную картину:
Карцинома молочной железы
Рак молочной железы – самая распространенная онкологическая патология у женщин, а в общей структуре злокачественных заболеваний – занимает второе место после рака легких. Более того, заболевание обладает еще и высоким уровнем летальности. Мужчины хоть и болеют на порядок реже, но рак протекает у них более агрессивно, к тому же они долгое время откладывают обращение к специалисту, увеличивая риски неблагоприятного исхода.
Причинами рака груди выступают длительные воспалительные заболевания половых органов, вредные привычки, тяжелая сопутствующая патология, злокачественные новообразования половых органов, стресс, гормональный дисбаланс и др. Весомый вклад в развитие рака молочной железы делает еще тенденция женщин в отказе от грудного вскармливания и рождения детей в принципе.
Проблема еще состоит в том, что большинство людей очень халатно относятся к своему здоровью. Клинические признаки очень часто появляются только на второй стадии рака, а начальные проходят бессимптомно. Но пациенты увиливают от профилактических осмотров, не делают самоосмотров, откладывают визиты к врачу и обращаются уже на поздних стадиях.
Диагностика рака включает смотр, сбор анамнестических данных и дополнительные методы исследования.
В зависимости от локализации новообразования рак молочной железы условно разделяют на:
Юсуповская больница – круглосуточное медицинское учреждение высокого уровня, специалисты которого занимаются не только диагностикой и лечением онкологических заболеваний, но и рассказывают, что такое карцинома молочной железы, какие ее симптомы, как правильно проводить самоосмотр желез. Врачи считают, что мало только лечить, важно – заниматься профилактикой онкологических заболеваний.
Симптомы карциномы молочной железы
Ранние стадии онкологического процесса молочной железы характеризуются скудной клинической картиной, или вовсе проходят бессимптомно.
В процессе развития появляются симптомы общей раковой интоксикации:
Специфические симптомы карциномы груди:
Наличие даже одной из вышеперечисленных жалоб – причина, чтобы обратится к специалисту. Чем раньше установлен диагноз – тем благоприятней прогноз.
Диагностика и лечение карциномы молочной железы
Диагностика включает сбор жалоб, анамнеза, осмотр, пальпацию, лабораторные и инструментальные исследования.
После консультации назначается маммография, ультразвуковое исследование железы, а для окончательной установки диагноза карциномы молочной железы проводится биопсия с гистологическим исследованием биоптата. Для исключения или обнаружения метастазов карциномы груди проводят магниторезонансную томографию, компьютерную томографию, позитронно-эмиссионную компьютерную томографию и др.
Лечение может быть радикальным на ранних стадиях, симптоматическим и паллиативным. Методы лечения при карциноме молочной железы следующие:
Лечение карциномы молочной железы чаще всего направлено еще и на профилактику рецидивов. Терапия зависит от стадии, гистологического строения, степени дифференцировки клеток, гормоночувствительности, распространенности и др.
Таргетная терапия карциномы молочной железы – один из медикаментозных методов, который направленный на блокировку роста клеток новообразования, путем вмешательства таргетных клеток в канцерогенез.
Гормональная и химиотерапия широко используется в лечении карцином. Подбор препаратов выполняется в зависимости от чувствительности, которая определяется гистологически.
Хирургическое лечение карциномы молочной железы может быть, как радикальной мерой, так и паллиативной – все зависит от стадии процесса. Если возникла необходимость полного удаления молочной железы, дефект можно исправить посредством косметической операции и использованием имплантов.
Прогноз при карциноме молочной железы
Прогноз для жизни при карциноме молочной железы зависит от многих факторов. Ранняя диагностика – один из главных признаков благоприятного прогноза.
Гистологическая структура карциномы груди так же имеет важное значение. Так, например, суррогатный молекулярно-биологический подтип карциномы молочной железы чаще имеет неблагоприятный прогноз.
Отказ от лечения очень быстро приводит к терминальной стадии рака молочной железы с многочисленными метастазами.
В Юсуповской больнице диагностика и лечение карциномы молочной железы проходит в комфортных условиях за очень короткое время. Специалисты высокого уровня со всей должной ответственностью подбирают индивидуальный подход и помогаю каждому пациенту. Персонал обучен правильному уходу и обучает родственников и пациентов для наилучшего результата.
РМЖ: морфологическая характеристика
В настоящее время рак молочной железы (РМЖ) является самым распространенным заболеванием у женщин. Ежегодно в мире выявляется более 1,7 миллионов случаев этого заболевания. Существует несколько патогенетических разновидностей РМЖ, которые принципиально отличаются друг от друга по эпидемиологии, факторам риска, ответу на лечение и прогнозам.
Наиболее частой категорией злокачественных образований молочной железы является ER/PgR-позитивный РМЖ. Риск возникновения таких опухолей напрямую зависит от современного образа жизни женщин, важными составляющими которого являются контроль рождаемости и ожирение. Непривычные условия функционирования молочной железы, заключающиеся в отсутствии постоянных беременностей и лактаций, избыточном питании и ведущие к ожирению, нарушают физиологические циклы колебаний уровня стероидных гормонов и обновления клеток.
Кроме того, вероятность заболевания раком молочной железы увеличивается с возрастом: опухоли, имеющие большее количество рецепторов к эстрогену и прогестерону, возникают в организме с большим количеством сопутствующих развитию РМЖ факторов и избыточным процентом жировой ткани, которая является значимым «производителем» женских половых гормонов, особенно после менопаузы.
Факторы риска других разновидностей РМЖ (HER2-позитивных или трижды негативных карцином) изучены в значительно меньшей степени, но их существование напрямую сказывается на результатах скрининга и лечения данного заболевания. Несомненным с точки зрения эпидемиологии является феноменальное улучшение отдаленных результатов лечения рака молочной железы. Смертность от РМЖ с 1990 по 2014 гг. в США упала на целых 34 % — беспрецедентная динамика за период, охватывающий всего лишь четверть века.
Этот колоссальный прогресс связывают с появлением тамоксифена и других препаратов для лечения гормон-чувствительных карцином, внедрением трастузумаба и иных антагонистов рецептора HER2, появлением тестирования генов наследственного рака BRCA1 и BRCA2, совершенствованием химиотерапии и т. д.
К сожалению, столь очевидный прогресс не затрагивает страны с ограниченными ресурсами, которые не имеют полного доступа ко всем разновидностям системного лечения РМЖ. Для лучшего понимания биологии рака молочной железы необходимы знания о факторах риска его развития. К таким относятся:
1. Генетические мутации
В некоторых случаях РМЖ передается в соответствии с классической Менделевской моделью наследования. Самые распространенные гены предрасположенности — BRCA1 и BRCA2, чей вклад в частоту наследственных заболеваний раком молочной железы составляет около 20 %. Исследования на семьях с таким типом карцином продемонстрировали фатальный риск развития рака у носительниц мутаций BRCA. Кроме того, в качестве генов предрасположенности к развитию РМЖ могут быть рассмотрены гены ATM, PTEN, p53 и др., поскольку было отмечено значительное увеличение частоты РМЖ среди их гетерозиготных носительниц.
2. Соматические изменения
Взаимодействие между различными факторами, предрасполагающими к возникновению РМЖ, приводит к аккумуляции соматических мутаций в эпителиальных клетках. Хромосомная нестабильность, проявляющаяся в патологическом количестве крупных хромосомных перестроек, отдельные изменения в генах, ассоциированных с РМЖ — все это служит пусковым механизмом для возникновения соматических изменений. Различные комбинации мутаций и эпигенетических событий являются причиной появления совокупности свойств, характерных для раковых клеток, таких как способность противостоять процессу апоптоза, неограниченное деление и самодостаточность в отношении ростовых факторов, возможность инвазии и метастазирования, непрерывный ангиогенез и т. д.
3. Образ жизни и влияние окружающей среды
Ожирение, сопровождающееся наличием висцерального жира, и постоянный набор веса неразрывно связаны с увеличением риска возникновения РМЖ как до наступления менопаузы, так и после. В тоже время было замечено, что у женщин, ведущих активный образ жизни с регулярными физическими нагрузками, риск возникновения РМЖ после менопаузы меньше. Кроме того, риск возрастает вместе с увеличением потребления алкоголя.
4. Воздействие облучения
Кроме того, опухоли, ограниченные базальной мембраной протока или дольки, получили название неинвазивных (карциномы in situ), а образования, обладающие способностью к проникновению через базальную мембрану в строму, назвали инвазивными (опухолевые клетки в строме могут инвазировать сосуды, что является причиной поражения лимфатических узлов и развития отдаленных метастазов).
Неинвазивная протоковая карцинома (DCIS — ductal carcinoma in situ)
Среди всех опухолей молочной железы примерно 20 % составляют неинвазивные протоковые карциномы. Их выявление в большинстве случаев происходит благодаря обнаружению микрокальцификатов. Однако клинически DCIS может проявляться в виде:
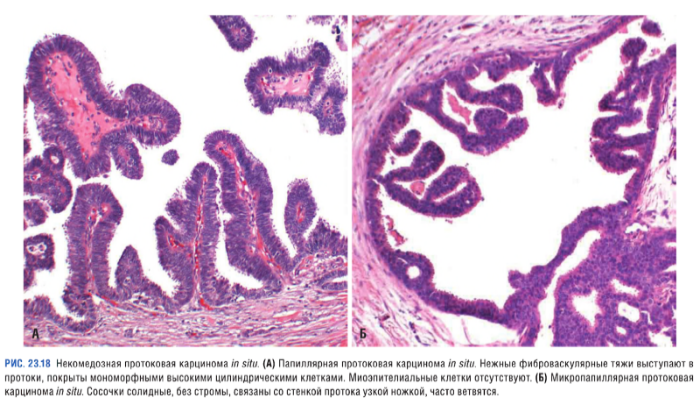
Неинвазивная протоковая карцинома представляет собой скопление злокачественных клеток, окруженных базальной мембраной протоков. Тем не менее DCIS может распространяться за пределы протока и инфильтрировать прилежащие ткани молочной железы. В зависимости от гистологического строения протоковый РМЖ in situ подразделяется на следующие типы:
Комедокарцинома
Опухоль, характеризующаяся наличием очагов некроза, солидных полей плеоморфных клеток с ярко выраженной гиперхроматией ядер и кальцификацией мембран, которые можно выявить при маммографии (линейные и/или ветвящиеся микрокальцификаты). Вследствие обтурации протоков возникает перидуктальный фиброз, сопровождающийся хроническим воспалением.
Некомедозные карциномы
Опухоли, отличающиеся отсутствием выраженной атипии у злокачественных клеток:
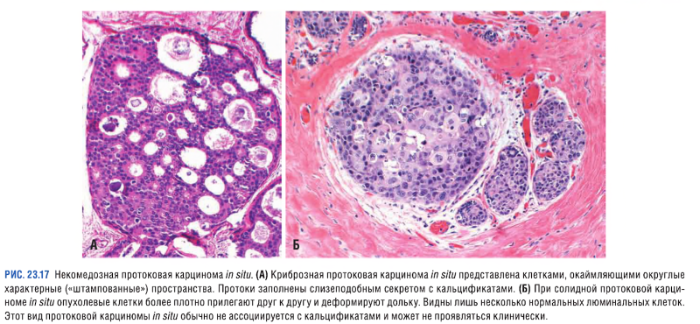
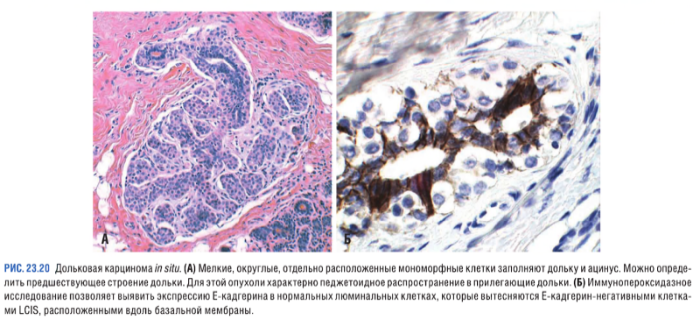
Неинвазивная дольковая карцинома (LCIS — lobular carcinoma in situ)
Такие опухоли клинически никак не не проявляются (микрокальцификаты и уплотнения отсутствуют), поэтому даже после внедрения скрининга распространенность LCIS не изменилась — 1–6 % от общего числа карцином. LCIS характеризуются наличием идентичных атипичных клеток с измененными круглыми ядрами. Клетки достаточно слабо связаны между собой вследствие нарушения экспрессии E-кадгерина, участвующего в образовании межклеточных контактов. Кроме того, клетки неинвазивных дольковых карцином характеризуются негативной экспрессией рецепторов к факторам роста и наличием гиперэкспрессии рецепторов к эстрогенам и прогестероны (ER+/Pgr+, HER2-).
Инвазивные карциномы
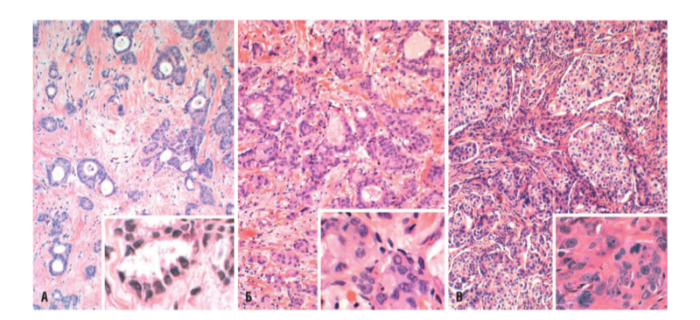
Инвазивная протоковая карцинома является самым распространенным типом карциномы и представляет 80 % всех РМЖ. Макроскопически такие опухоли отличаются плотной, твердой консистенцией (объясняется наличием очагов и некроза и скоплениями кальцификатов), разрезание или скобление сопровождается характерным звуком. Карциномы могут содержать клетки различной степени дифференцировки:
Инвазивная дольковая карцинома (ILC — invasive lobular carcinoma) состоит из клеток, которые утратили способность образовывать межклеточные контакты и поэтому либо «разбросаны» в строме молочной железы, либо расположены в одну линию. На основании морфологических различий ILC можно поделить на несколько гистологических типов, однако все они будут характеризоваться нарушениями контактов между клетками.
Источник:
Devita Jr V. T., Lawrence T. S., Rosenberg S. A. DeVita, Hellman, and Rosenberg’s cancer: principles & practice of oncology. – Lippincott Williams & Wilkins, 2015.
Комедокарцинома молочной железы что это такое у женщин
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена; Кафедра онкологии и радиотерапии ФПП ОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Современные подходы к лечению больных с карциномой in situ молочной железы
Журнал: Онкология. Журнал им. П.А. Герцена. 2013;2(4): 30-33
Пак Д. Д., Усов Ф. Н., Фетисова Е. Ю., Волченко А. А., Ефанов В. В. Современные подходы к лечению больных с карциномой in situ молочной железы. Онкология. Журнал им. П.А. Герцена. 2013;2(4):30-33.
Pak D D, Usov F N, Fetisova E Iu, Volchenko A A, Efanov V V. Current treatment options for breast carcinoma in situ. P.A. Herzen Journal of Oncology. 2013;2(4):30-33.
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздравсоцразвития России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
Московский научно-исследовательский онкологический институт им. П.А. Герцена; Кафедра онкологии и радиотерапии ФПП ОВ Первого Московского государственного медицинского университета им. И.М. Сеченова
ФГБУ «Московский научно-исследовательский онкологический институт им. П.А. Герцена» Минздрава России
По оценкам экспертов ВОЗ, в мире ежегодно выявляется от 800 000 до 1 млн новых случаев рака молочной железы (РМЖ). В структуре заболеваемости злокачественными новообразованиями (ЗНО) женского населения России РМЖ в 2010 г. занимал 1-е место (20,5%), как и в структуре смертности от РМЖ (1-е место — 17,2%). При этом число впервые выявленных случаев ЗНО молочной железы увеличилось с 49 548 случаев в 2005 г. до 57 241 в 2010 г. [1].
Благодаря развитию диагностических методов и внедрению скрининговых программ частота выявления карциномы in situ (CIS) молочной железы в некоторых странах составляет 15—25% от всех случаев впервые выявленного РМЖ [2, 3].
Согласно международной классификации по системе TNM, CIS относится к стадии 0, а первичная опухоль кодируется как Тis.
По данным исследований, CIS может достигать 5—10 см, а иногда и более без признаков инвазии [4].
Для диагностики CIS молочной железы применяются маммография, ультразвуковое исследование (УЗИ). Магнитно-резонансную томографию (МРТ) следует применять для диагностики в сочетании с другими методами [5], особенно при планировании органосохраняющего лечения. При маммографическом исследовании протоковая CIS (DCIS) в 72% случаев проявляется только очагами микрокальцификации, чаще сгруппированными (реже рассеянные), в 12% случаев микрокальцификация сочетается с очагом уплотнения и в 6% DCIS протекает рентгенологически бессимптомно. Микрокальцификация при дольковой CIS (LCIS) наблюдается намного реже и в 60% случаев кальцификации подвергается не сама опухоль, а окружающие ткани, иногда на большом протяжении [4].
В план обследования больных с узловой патологией молочных желез обязательно должна входить пункционная биопсия. При подозрении на CIS необходимо проводить трепанобиопсию, позволяющую получить столбик ткани, достаточный как для гистологического, так и для иммуногистохимического исследования. В настоящее время наиболее информативный материал можно получить путем вакуумной биопсии аппаратом Маммотом. Этот метод позволяет при однократном введении инструмента в зону очага (узловое образование, скопление микрокальцинатов) многократно получать биопсийный материал.
После биопсии обязательно выполняют маркировку зоны, где находились непальпируемые образования и микрокальцинаты, титановой клипсой, что облегчат работу хирурга в случае последующего оперативного вмешательства. При невозможности проведения толстоигольного или вакуумного забора тканей выполняют ножевую биопсию со срочным гистологическим исследованием.
К сожалению, во многих регионах Российской Федерации практически остается нерешенной проблема диагностики непальпируемых форм РМЖ, в том числе и CIS. У большинства больных неинвазивные формы РМЖ являются случайной находкой, поэтому очень важно правильно выбрать стратегию при подозрении на клинически скрыто протекающую карциному. При этом необходим четкий алгоритм диагностических мероприятий для выявления потенциально излечимых форм РМЖ. На основании полученных нами данных разработан алгоритм обследования больных (см. рисунок). 
Диагноз DCIS требует немедленного лечения, так как выживаемость при DCIS может составлять до 100% [2, 6], а при отсутствии лечения частота развития инвазивного заболевания достигает 30% [2].
Наиболее эффективным методом лечения CIS остается хирургическое вмешательство. При этом объем оперативного вмешательства различен. В последние десятилетия подходы к хирургическому этапу лечения изменились в сторону уменьшения объема удаляемых тканей без нарушения радикализма. Все чаще при данном заболевании применяется органосохраняющее лечение, чему в немалой степени способствует использование адъювантной лучевой терапии (ЛТ) [7], снижающей риск локорегионарных рецидивов на 50% [8, 9]. Органосохраняющее лечение в сочетании с адъювантной ЛТ дает результаты, эквивалентные мастэктомии, в то время как отказ от адъювантной ЛТ значительно повышает риск местного рецидива [10, 11].
Однако, по данным некоторых исследований, можно отказаться от проведения адъювантной ЛТ при органосохраняющем лечении у пациентов с DCIS при отсутствии комедонекроза в опухоли (или его наличии и размере менее 1,5 см при условии широкого иссечения), размере очага менее 2 см в диаметре и расстоянии от края опухоли более 2 см [12]. Для проверки этих данных нужны рандомизированные исследования.
Проведены многочисленные исследования, направленные на выявление достоверных факторов возможного рецидива после первичного лечения DCIS По данным мировой литературы (мультивариантный анализ), молодой возраст (менее 40 лет), размер DCIS более 1,5 см и отказ от адъювантной ЛТ — факторы плохого прогноза в отношении развития локорегионарных рецидивов [7, 13]. При этом молодой возраст и положительный край резекции рассматриваются как важные факторы риска для развития местного рецидива даже при органосохраняющем лечении в сочетании с ЛТ [9]. Микропапиллярный гистологический тип опухоли, наличие комедонекроза и мультифокального и мультицентрического роста являются факторами неблагоприятного прогноза для развития ипсилатерального рецидива и, в ряде случаев, развития рака в контралатеральной молочной железе [13—15]. При этом выделение комедокарциномы в отдельный гистологический тип является неверным, в настоящее время рассматривается наличие или отсутствие комедонекроза в опухоли [16]. Такие факторы, как гиперэкспрессия HER2/neu и высокая пролиферативная активность опухоли (Ki-67+) DCIS, также ассоциируются с более высоким риском развития рецидива при органосохраняющем лечении DCIS [11]. Ожирение может быть связано с неблагоприятными биологическими особенностями и худшим прогнозом при инвазивном РМЖ. По данным исследований, для пациенток с DCIS такой связи не прослежено, ИМТ более 30 никак не влияет на прогноз [17].
В качестве оценки лучшего подхода к комплексному лечению при DCIS университетом Южной Калифорнии в 1996 г. был разработан и введен в практику прогностический индекс Van Nuys (VNPI) [18]. В 2003 г. он был дополнен [19] (табл. 1).
При расчете риска возможного рецидива учитываются следующие признаки: размер опухоли, ширина краев резекции, степень гистологической злокачественности, возраст. По данным исследований M.J. Silverstein и соавт. [18, 19], у пациенток при индексе 4—6 баллов лечение можно ограничивать только удалением опухоли. При индексе 7—9 баллов органосохраняющее лечение должно быть дополнено адъювантной ЛТ или рекомендуется повторная операция в случае отступа от края опухоли менее 10 мм. При индексе 10—12 баллов отмечен чрезвычайно высокий риск рецидива при органосохраняющем лечении даже в сочетании с ЛТ. В этом случае должна быть выполнена мастэктомия, по возможности с реконструкцией [19]. По результатам последних исследований, у больных с DCIS после мастэктомии при индексе 4—9 баллов рецидивов не отмечалось в течение 12 лет, в то время как при 10—12 баллах за то же время рецидивы были отмечены в 9,6% случаев. В группе риска по развитию локального рецидива находятся пациентки молодого возраста, мультифокальный и мультицентрический рост опухоли [13].
В настоящее время не выявлены четкие показания к биопсии сторожевого лимфатического узла у пациенток с DCIS в связи с крайне редким поражением регионарных лимфатических узлов при данном заболевании. Некоторые исследования показывают, что биопсия сторожевого лимфатического узла представляется целесообразной при опухолях более 2,5 см с гиперэкспрессией HER2/neu (как часть первичной хирургической процедуры) [20].
У больных с DCIS следует применять системную терапию. В настоящее время известно, что применение тамоксифена для ЭР + DCIS снижает риск рецидива [10]. Пациентки с ЭР + DCIS должны получать тамоксифен в адъювантном режиме [21].
При выявлении LCIS рекомендуется наблюдение в течение всей жизни либо хирургическое лечение. Наиболее приемлемым объемом оперативного вмешательства является тотальная мастэктомия с последующей реконструкцией молочной железы [4].
Материал и методы
В отделении общей онкологии МНИОИ им. П.А. Герцена в 1994—2011 гг. проведено лечение 108 больным с CIS молочной железы. Средний возраст больных составил 48,3 года. Частота выявления CIS составила 1,5%.
Чаще неинвазивный рак поражал левую молочную железу — в 55,6% случаев, правую — в 44,4% наблюдений. На этапе обследования диагноз CIS установлен только в 1,9% случаев по результатам гистологического исследования материала, полученного при вакуумной биопсии аппаратом Маммотом.
Результаты
При морфологическом исследовании у 93 (86,1%) больных выявлен протоковый рак, у 8 (7,4%) — дольковый и у 7 (6,5%) — сочетание протокового и долькового рака. Монофокальный рост опухоли выявлен у 58 (54%) больных, мультифокальный — у 35 (31,7%), мультицентрический — у 15 (14,3%). При протоковом раке чаще встречался монофокальный и мультифокальный рост опухоли, а при дольковом — мультицентрический. Метастазы в подмышечных лимфатических узлах обнаружены у 4,6% больных. Местный рецидив выявлен в 4 (3,7%) случаях. Пятилетняя выживаемость в первой группе составила 100%, безрецидивная выживаемость — 96,3%. Данные об объеме хирургических вмешательств представлены в табл. 2.
Заключение
Прогнозируя результаты органосохраняющего лечения при CIS следует помнить, что характерной особенностью протоковой формы заболевания является мультифокальное распространение опухолевого роста, т.е. в пределах одного сегмента поражается 1—2 протока. При дольковой CIS чаще встречаются множественные зачатки опухоли в разных отделах молочной железы (нередко в противоположной молочной железе). Органосохраняющие операции в объеме субтотальной резекции или подкожной мастэктомии с одномоментной реконструкцией являются адекватными для хирургического лечения больных с неинвазивными формами РМЖ, а также важными этапами социальной и психологической реабилитации женщин.
В данном случае полное или почти полное удаление тканей молочной железы является очень важным этапом органосохраняющего комбинированного лечения больных РМЖ.