концентрированная серная кислота реагирует с чем реагирует
Серная кислота
Обладает выраженным дегидратационным (водоотнимающим) действием. При попадании на кожу или слизистые оболочки приводит к тяжелым ожогам.
Получение
Известны несколько способов получения серной кислоты. Применяется промышленный (контактный) способ, основанный на сжигании пирита, окислении образовавшегося SO2 до SO3 и последующим взаимодействием с водой.
Нитрозный способ получения основан на взаимодействии сернистого газа с диоксидом азота IV в присутствии воды. Он состоит из нескольких этапов:
В окислительной башне смешивают оксиды азота (II) и (IV) с воздухом:
Смесь газов подается в башни, орошаемые 75-ной% серной кислотой, здесь смесь оксидов азота поглощается с образованием нитрозилсерной кислоты:
В ходе гидролиза нитрозилсерной кислоты получают азотистую кислоту и серную:
В упрощенном виде нитрозный способ можно записать так:
Химические свойства
В водном растворе диссоциирует ступенчато.
С солями реакция идет, если в результате выпадает осадок, образуется газ или слабый электролит (вода). Серная кислота, как и многие другие кислоты, способна растворять осадки.
Подчеркну, что реакции разбавленной серной кислоты с железом и хромом не сопровождаются переходом этих элементов в максимальную степень окисления. Они окисляются до +2.
Cu + H2SO4(разб.) ⇸ (реакция не идет, медь не может вытеснить водород из кислоты)
Холодная концентрированная серная кислота пассивирует Al, Cr, Fe, Ni, Be, Co. При нагревании или амальгамировании данных металлов реакция идет.
Обратите особое внимание, что при реакции железа, хрома с концентрированной серной кислотой достигается степень окисления +3. В подобных реакциях с разбавленной серной кислотой (написаны выше) достигается степень окисления +2.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Урок №14. Серный ангидрид и серная кислота
Повторите темы уроков 9 класса:
Оксид серы (VI)
Оксид серы (VI) – это кислотный оксид. При обычных условиях – бесцветная ядовитая жидкость, «дымит» на воздухе, поглощая пары воды.
Способы получения
Оксид серы (VI) получают в реакциях окисления:
SO 2 + NO 2 = SO 3 + NO
Разложением сульфата железа (III):
Химические свойства оксида серы (VI)
1. Оксид серы (VI) активно поглощает влагу и реагирует с водой с образованием серной кислоты:
2. Серный ангидрид – типичным кислотный оксид, взаимодействует с щелочами и основными оксидами.
SO 3 + 2NaOH ( избыток) = Na 2 SO 4 + H 2 O
SO 3 + NaOH ( избыток) = NaHSO 4
SO 3 + MgO = t = MgSO 4
3. Серный ангидрид – очень сильный окислитель:
SO 3 + 2KI = I 2 + K 2 SO 3
3SO 3 + H 2 S = 4SO 2 + H 2 O
5SO 3 + 2P = P 2 O 5 + 5SO 2
4. Растворяется в концентрированной серной кислоте, образуя олеум – раствор SO 3 в H 2 SO 4
РЕАКЦИИ СЕРНОЙ КИСЛОТЫ
Химические свойства разбавленной серной кислоты
1) Диссоциация протекает ступенчато:
(первая ступень, образуется гидросульфат – ион)
(вторая ступень, образуется сульфат – ион)
2) Взаимодействие с металлами:
Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений левее водорода:
Zn 0 + H 2 +1 SO 4 (разб) → Zn +2 SO 4 + H 2 0 ↑
Zn 0 + 2H + → Zn 2+ + H 2 0 ↑
3) Взаимодействие с основными и амфотерными оксидами:
CuO + H 2 SO 4 → CuSO 4 + H 2 O
CuO + 2H + → Cu 2+ + H 2 O
4) Взаимодействие с основаниями:
H 2 SO 4 + 2NaOH → Na 2 SO 4 + 2H 2 O
Если кислота в избытке, то образуется кислая соль:
H 2 SO 4 + NaOH → NaНSO 4 + H 2 O
H 2 SO 4 + Cu(OH) 2 → CuSO 4 + 2H 2 O
2H + + Cu(OH) 2 → Cu 2+ + 2H 2 O
5) Обменные реакции с солями:
Серная кислота – сильная нелетучая кислота, вытесняет из солей другие менее сильные кислоты:
MgCO 3 + H 2 SO 4 → MgSO 4 + H 2 O + CO 2 ↑
MgCO 3 + 2H + → Mg 2+ + H 2 O + CO 2 ↑
Н 2 SO 4 + 2NaHCO 3 = Na 2 SO 4 + CO 2 ↑ + H 2 O
H 2 SO 4 + Na 2 SiO 3 = Na 2 SO 4 + H 2 SiO 3 ↓
Качественная реакция на сульфат-ион
BaCl 2 + H 2 SO 4 → BaSO 4 ↓ + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 ↓
Образование белого осадка BaSO 4 (нерастворимого в кислотах) используется для идентификации серной кислоты и растворимых сульфатов.
6) Реагирует с аммиаком
Химические свойства концентрированной серной кислоты
1. С водой образуются гидраты:
H 2 SO 4 + nH 2 O = H 2 SO 4 ·nH 2 O + Q
Органические вещества обугливаются!
2H 2 SO 4 + C = CO 2 + 2SO 2 + 2H 2 O
2. Серная кислота окисляет неметаллы
неМе + H 2 SO 4 (конц.) = H 2 O + SO 2 + Кислотный гидроксид
, где степень окисления неметалла – высшая
C + 2H 2 SO 4 = 2H 2 O + CO 2 + 2SO 2
S + 2H 2 SO 4 = 3SO 2 + 2H 2 O
2P + 5H 2 SO 4 = 2H 3 PO 4 + 5SO 2 + 2H 2 O
3. Взаимодействие серной кислоты с металлами
H 2 SO 4 (конц.) + Me = t = соль + H 2 O + Х
Железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании образуется газа SO 2 :
6H 2 SO 4 (конц.) + 2Fe = t = Fe 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
6H 2 SO 4(конц.) + 2Al = t = Al 2 (SO 4 ) 3 + 3SO 2 + 6H 2 O
При взаимодействии с неактивными металлами концентрированная серная кислота восстанавливается до сернистого газа:
2H 2 SO 4 (конц.) + Cu = CuSO 4 + SO 2 ↑ + 2H 2 O
2H 2 SO 4 (конц.) + Hg = HgSO 4 + SO 2 ↑ + 2H 2 O
2H 2 SO 4 (конц.) + 2Ag = Ag 2 SO 4 + SO 2 ↑ + 2H 2 O
При взаимодействии с щелочноземельными металлами и магнием концентрированная серная кислота восстанавливается до серы:
3Mg + 4H 2 SO 4 = 3MgSO 4 + S + 4H 2 O
При взаимодействии со щелочными металлами и цинком концентрированная серная кислота восстанавливается до сероводорода:
5H 2 SO 4 (конц.) + 4Zn = 4ZnSO 4 + H 2 S↑ + 4H 2 O
4. Взаимодействие с восстановителями
Концентрированная серная кислота окисляет галогеноводороды и сероводород при комнатной температуре:
3H 2 SO 4 (конц.) + 2KBr = Br 2 ↓ + SO 2 ↑ + 2KHSO 4 + 2H 2 O
5H 2 SO 4 (конц.) + 8KI = 4I 2 ↓ + H 2 S↑ + K 2 SO 4 + 4H 2 O
H 2 SO 4 (конц.) + 3H 2 S = 4S↓ + 4H 2 O
СОЛИ СЕРНОЙ КИСЛОТЫ
1) Разложение сульфатов
Термически устойчивые сульфаты – сульфаты щелочных металлов (в том числе лития), они плавятся не разлагаясь
Остальные сульфаты при нагревании разлагаются на оксид серы(IV), оксид металла и кислород:
2CuSO 4 = t = 2CuO + SO 2 + O 2 (SO 3 )
2Al 2 (SO 4 ) 3 = t = 2Al 2 O 3 + 6SO 2 + 3O 2
2ZnSO 4 = t = 2ZnO + SO 2 + O 2
2Cr 2 (SO 4 ) 3 = t = 2Cr 2 O 3 + 6SO 2 + 3O 2
4FeSO 4 = t = 2Fe 2 O 3 + 4SO 2 + O 2
Так как оксиды тяжёлых и благородных металлов разлагаются сами, разложение их сульфатов следует записывать до металла:
Ag 2 SO 4 = t = 2Ag + SO 2 + O 2
HgSO 4 = t = Hg + SO 2 + O 2
2) Сульфаты проявляют окислительные свойства и могут взаимодействовать с восстановителями, восстанавливаясь до сульфидов.
CaSO 4 + 4C = CaS + 4CO
3) Многие средние сульфаты образуют устойчивые кристаллогидраты
Na 2 SO 4 ∙ 10H 2 O − глауберова соль
CaSO 4 ∙ 2H 2 O − гипс
CuSO 4 ∙ 5H 2 O − медный купорос
FeSO 4 ∙ 7H 2 O − железный купорос
ZnSO 4 ∙ 7H 2 O − цинковый купорос
Na 2 CO 3 ∙ 10H 2 O − кристаллическая сода
Серная кислота. Свойства серной кислоты.
Серная кислота H2SO4 – нелетучая тяжелая жидкость, хорошо растворима в воде (при нагревании). tпл. = 10,3°C, tкип. = 296°С,
Отлично впитывает влагу, поэтому часто выступает в качестве осушителя.
Производство серной кислоты представляет собой контактный процесс. Его можно разделить на 3 этапа:
1. Получение SO2 путем сжигания серы или обжигом сульфидов.
3. Поглощение SO3 серной кислотой, в результате чего образуется 100% серная кислота (олеум):
Воду использовать нельзя из-за образования тумана.
Химические свойства серной кислоты.
Серная кислота H2SO4 – двухосновная кислота, которая обладает большой силой. В воде она диссоциирует ступенчато:
Разбавленная серная кислота реагирует только с металлами, стоящими в ряду напряжения до водорода:
В реакциях с щелочами или основными оксидами образует сульфаты или гидрофильфаты:
Необходимо отметить, что сульфат бария является нерастворимым сульфатом, поэтому его используют в качестве индикатора на присутствие сульфат-ионов.
Концентрированная H2SO4 окисляет медь, серебро, углерод и фосфор:
Концентрированная H2SO4 при обычных условиях не взаимодействует с Al, Cr, Fe, но при нагревании вступает в реакцию.
Концентрированная H2SO4 быстро вступает в реакцию с водой, выделяя пр этом огромное количество тепла.
Серная кислота — химические свойства и промышленное производство

Тяжелая маслянистая жидкость («купоросное масло»);
плотность 1,84 г/см3; нелетучая, хорошо растворима в воде – с сильным нагревом; t°пл. = 10,3°C, t°кип. = 296°С, очень гигроскопична, обладает водоотнимающими свойствами (обугливание бумаги, дерева, сахара).
Теплота гидратации настолько велика, что смесь может вскипать, разбрызгиваться и вызывать ожоги. Поэтому необходимо добавлять кислоту к воде, а не наоборот, поскольку при добавлении воды к кислоте более легкая вода окажется на поверхности кислоты, где и сосредоточится вся выделяющаяся теплота.
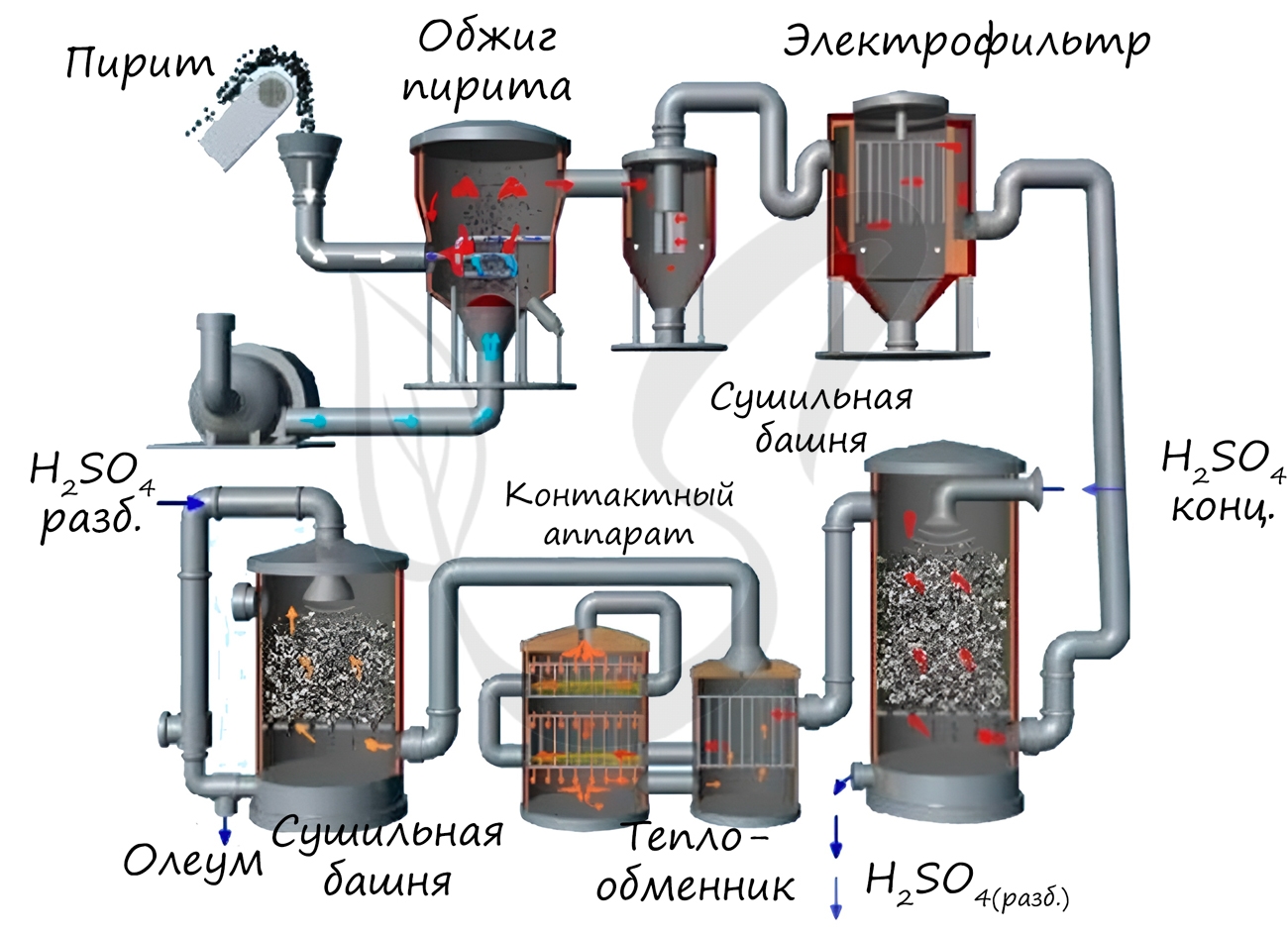
Промышленное производство серной кислоты (контактный способ):

Измельчённый очищенный влажный пирит (серный колчедан) сверху засыпают в печь для обжига в «кипящем слое«. Снизу (принцип противотока) пропускают воздух, обогащённый кислородом.
Из печи выходит печной газ, состав которого: SO2, O2, пары воды (пирит был влажный) и мельчайшие частицы огарка (оксида железа). Газ очищают от примесей твёрдых частиц (в циклоне и электрофильтре) и паров воды (в сушильной башне).
В контактном аппарате происходит окисление сернистого газа с использованием катализатора V 2 O 5 ( пятиокись ванадия) для увеличения скорости реакции. Процесс окисления одного оксида в другой является обратимым. Поэтому подбирают оптимальные условия протекания прямой реакции — повышенное давление (т.к прямая реакция идет с уменьшением общего объема) и температура не выше 500 С ( т.к реакция экзотермическая).
В поглотительной башне происходит поглощение оксида серы (VI) концентрированной серной кислотой.
Поглощение водой не используют, т.к оксид серы растворяется в воде с выделением большого количества теплоты, поэтому образующаяся серная кислота закипает и превращается в пар. Для того, чтобы не образовывалось сернокислотного тумана, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H2SO4·nSO3
Химические свойства серной кислоты:
H2SO4 — сильная двухосновная кислота, одна из самых сильных минеральных кислот, из-за высокой полярности связь Н – О легко разрывается.
2) Взаимодействие серной кислоты с металлами:
Разбавленная серная кислота растворяет только металлы, стоящие в ряду напряжений левее водорода:
Zn 0 + H2 +1 SO4(разб) → Zn +2 SO4 + H2
3) Взаимодействие серной кислоты с основными оксидами:
CuO + H2SO4 → CuSO4 + H2O
5) Обменные реакции с солями:
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Образование белого осадка BaSO4 (нерастворимого в кислотах) используется для обнаружения серной кислоты и растворимых сульфатов (качественная реакция на сульфат ион).
Особые свойства концентрированной H2SO4 :
Активный металл
8 Al + 15 H2SO4(конц.)→4Al2(SO4)3 + 12H2O + 3 H2S
4│2Al 0 – 6e — → 2Al 3+ — окисление
3│ S 6+ + 8e → S 2– восстановление
Металл средней активности
2Cr + 4 H2SO4(конц.)→ Cr2(SO4)3 + 4 H2O + S
1│ 2Cr 0 – 6e →2Cr 3+ — окисление
1│ S 6+ + 6e → S 0 – восстановление
Металл малоактивный
2Bi + 6H2SO4(конц.)→ Bi2(SO4)3 + 6H2O + 3 SO2
1│ 2Bi 0 – 6e → 2Bi 3+ – окисление
3│ S 6+ + 2e →S 4+ — восстановление
2) Концентрированная серная кислота окисляет некоторые неметаллы как правило до максимальной степени окисления, сама восстанавливается до S +4 O2:
3) Окисление сложных веществ:
Серная кислота окисляет HI и НВг до свободных галогенов:
2 КВr + 2Н2SO4 = К2SО4 + SO2 + Вr2 + 2Н2О
2 КI + 2Н2SО4 = К2SO4 + SO2 + I2 + 2Н2О
Концентрированная серная кислота не может окислить хлорид-ионы до свободного хлора, что дает возможность получать НСl по реакции обмена:
NаСl + Н2SO4(конц.) = NаНSO4 + НСl
Серная кислота отнимает химически связанную воду от органических соединений, содержащих гидроксильные группы. Дегидратация этилового спирта в присутствии концентрированной серной кислоты приводит к получению этилена:
С2Н5ОН = С2Н4 + Н2О.
Обугливание сахара, целлюлозы, крахмала и др. углеводов при контакте с серной кислотой объясняется также их обезвоживанием:
C6H12O6 + 12H2SO4 = 18H2O + 12SO2↑ + 6CO2↑.
Химия, Биология, подготовка к ГИА и ЕГЭ
ОВР в статье специально выделены цветом. Обратите на них особое внимание. Эти уравнения могут попасться в ЕГЭ.
Разбавленная серная ведет себя, как и остальные кислоты, окислительные свои возможности прячет:
Zn + H2SO4 → ZnSO4 + H2↑
Автор статьи — Саид Лутфуллин
Окислительные свойства серной кислоты
Концентрированная серная кислота – тяжелая маслянистая жидкость, не летучая, не имеет вкуса и запаха
За счет серы в степени окисления +6(высшей) серная кислота приобретает сильные окислительные свойства.
Правило для задания 24 (по-старому А24) при приготовлении растворов серной кислоты никогда нельзя в нее лить воду. Концентрированую серную кислоту нужно тонкой струйкой вливать в воду, постоянно помешивая.
Взаимодействие концентрированной серной кислоты с металлами
Эти реакции строго стандартизированны и идут по схеме:
H2SO4(конц.) + металл → сульфат металла + H2O + продукт восстановленной серы.
1) Алюминий, железо и хром с H2SO4 (конц) в нормальных условиях не реагируют, из-за пассивации. Нужно нагреть.
2) С платиной и золотом H2SO4 (конц) не реагирует вообще.
Сера в концентрированной серной кислоте – окислитель
Рассмотрим диаграмму степеней окисления серы:
Реакции будут идти вот так:
(обратите внимание, что железо окисляется до +3, до максимально возможной, высшей степени окисления, так как оно имеет дело с сильным окислителем)
Конечно, все относительно. Глубина восстановления будет зависеть от многих факторов: концентрации кислоты (90%, 80%, 60%), температуры и т.д. Поэтому совсем уж точно предсказать продукты нельзя. Приведенная выше таблица тоже имеет свой процент приблизительности, но пользоваться ей можно. Еще необходимо помнить, что в ЕГЭ, когда продукт восстановленной серы не указан, и металл не отличается особой активностью, то, скорее всего, составители имеют в виду SO 2. Нужно смотреть по ситуации и искать зацепки в условиях.
SO 2 – это вообще частый продукт ОВР с участием конц. серной кислоты.
H2SO4 (конц) окисляет некоторые неметаллы (которые проявляют восстановительные свойства), как правило, до максимальной — высшей степени окисления (образуется оксид этого неметалла). Сера при этом тоже восстанавливается до SO 2:
Свежеобразованный оксид фосфора ( V ) реагирует с водой, получается ортофосфорная кислота. Поэтому реакцию записывают сразу:
То же самое с бором, он превращается в ортоборную кислоту:
Очень интересны взаимодействие серы со степенью окисления +6 (в серной кислоте) с «другой» серой (находящейся в другом соединении). В рамках ЕГЭ рассматривается взаимодействиеH2SO4 (конц) с серой (простым веществом) и сероводородом.
Начнем с взаимодействия серы (простого вещества) с концентрированной серной кислотой. В простом веществе степень окисления 0, в кислоте +6. В этой ОВР сера +6 будет окислять серу 0. Посмотрим на диаграмму степеней окисления серы:
Сера 0 будет окисляться, а сера +6 будет восстанавливаться, то есть понижать степень окисления. Будет выделяться сернистый газ:
Но в случае с сероводородом:
Образуется и сера (простое вещество), и сернистый газ:
Этот принцип часто может помочь в определении продукта ОВР, где окислитель и восстановитель – один и тот же элемент, в разных степенях окисления. Окислитель и восстановитель «идут навстречу друг другу» по диаграмме степеней окисления.
А вот галогены в составе бромидов и иодидов (как и в составе соответствующих галогеноводородов) окисляются ей до свободных галогенов. Только вот сера восстанавливается по-разному: иодид является более cильным восстановителем, чем бромид. Поэтому иодид восстанавливает серу до сероводорода, а бромид до сернистого газа:
Хлороводород и фтороводород (как и их соли) устойчивы к окисляющему действию H2SO4 (конц).
Это позволяет использовать концентрированную серную кислоту самым разным образом:
Во-первых, осушение веществ. Концентрированная серная кислота забирает воду от вещества и оно «становится сухим».
Во-вторых, катализатор в реакциях, в которых отщепляется вода (например, дегидратация и этерификация):