кортикостероиды что к ним относится какие препараты
Стероидные противовоспалительные: инструкция для первостольника
Как работают топические глюкокортикостероиды и как грамотно проконсультировать по ним клиента аптеки
Появление местных кортикостероидов (ГКС) в начале 50‑х годов прошлого века считается одним из самых значимых событий в дерматологии. И сегодня препараты этой группы занимают лидирующие позиции среди всех наружных дерматологических ЛС [1]. Широкий спектр показаний, высокая активность, плейотропные эффекты и убедительная доказательная база наряду с благоприятным профилем безопасности — прочный фундамент для стремительного движения к вершинам популярности этих препаратов у врачей и потребителей. Как следствие, первостольникам необходимо держать в голове и уметь использовать в фармконсультировании знания об ЛС этой группы. Особенно с учетом того, что некоторые топические препараты, содержащие ГКС, отпускаются без рецепта. Как работают местные глюкокортикостероиды, когда их можно рекомендовать, и о чем предупредить клиентов — в нашей новой статье.
Говорим плейотропный, подразумеваем множественный
В основе механизма действия местных ГКС лежит их способность взаимодействовать со специфическими для кортикостероидов рецепторами, которые расположены в эпидермисе и фибробластах кожи человека. При этом они проявляют комплекс различных эффектов, оказывая плейотропное (множественное — прим. ред.) действие благодаря реализации целого ряда механизмов [2].
1. Противовоспалительный эффект
Обеспечивает преимущества топических ГКС при воспалительных поражениях кожи.
2. Имунносупрессивное действие
Обеспечивает противовоспалительный эффект топических ГКС.
3. Антипролиферативный эффект, направленный на подавление избыточного размножения некоторых клеток.
Обеспечивает эффективность топических глюкокортикостероидов при состояниях, сопровождаемых аномально высокой пролиферацией кожи, например, при псориазе или экземе.
4. Сосудосуживающий эффект
Обеспечивает высокую активность топических ГКС при дерматологических заболеваниях, сопровождающихся покраснением кожи и отечностью.
Механизм этого эффекта до сих пор остается не до конца изученным. Один из его этапов — ингибирование провоспалительных медиаторов, оказывающих сосудорасширяющее действие (гистамина, брадикинина, простагландина и др.). Вазоконстрикторная активность стала одним из критериев оценки мощности топического ГКС.
Активность топических ГКС
Активность препаратов этой группы зависит, как минимум, от четырех факторов [2, 4].
1. Форма выпуска.
Форма выпуска препарата местного действия — это в своем роде его «транспортное средство», обеспечивающее доставку действующих веществ вглубь кожи. Поэтому от ее свойств во многом зависит «мощность» топического средства.
Мази со стероидами считаются самой эффективной формой топических ГКС. Это эмульсии типа «вода в масле», высокая активность которых обусловлена способностью формировать на поверхности кожи непроницаемую для воздуха и влаги пленку и таким образом обеспечивать «эффект компресса» — окклюзию. В результате увеличивается местная концентрация и эффективность средства. Но у окклюзионных препаратов есть и недостатки: во‑первых, кожа перестает «дышать», что может способствовать развитию мокнутия, а во‑вторых, их неудобно наносить на кожу волосистой части головы, груди и т. д.
Топические ГКС в форме мазей целесообразно рекомендовать для лечения заболеваний сухой кожи.
Кремы, в отличие от мазей, будучи эмульсией «масло в воде», не являются жирными формами. Они не образуют окклюзионную пленку на поверхности кожи и потому лишены как недостатков мазей, так и их преимуществ. Кремы ГКС менее активны, чем стероидные мази.
Топические ГКС в форме крема показаны при остром и подостром воспалении без выраженного мокнутия.
Гели — эмульсия «масло в воде», имеющая спиртовую основу. Разжижаются при контакте с кожей, имеют среднюю степень активности.
Гели целесообразно рекомендовать при лечении участков тела, обильно покрытых волосами
Лосьоны, представляющие собой водные растворы, считаются наименее активной формой ГКС. Они испаряются, обеспечивая эффект охлаждения.
Топические ГКС в форме лосьона целесообразно рекомендовать при необходимости обработки больших участков, а также участков, обильно снабженных волосяными фолликулами.
2. Соль, с которой связан стероид.
Например, бетаметазон существует в виде валерата, дипропионата и бензоата, каждый из которых имеет разную активность.
3. Концентрация активного компонента
Чем выше концентрация действующего вещества, тем выше активность препарата.
Например, один из самых сильных топических ГКС клобетазола пропионат в форме мази примерно в 1000 раз «мощнее», чем самый слабый препарат этой группы, 1 %-гидрокортизон.
Существует две классификации топических ГКС по степени активности — Европейская, выделяющая 4 класса, и Американская, в которой препараты разделяются на 7 классов активности. И в первой, и во второй активность оценивалась на основании вазоконстрикторных тестов и по данным клинических исследований.
Европейская классификация топических глюкокортикостероидов [3]
Американская классификация топических ГКС [3]
| Класс (степень активности) | МНН |
| I – очень сильные | Клобетазол 0,05 % крем, мазь Бетаметазон (дипропионат) 0,1 % крем, мазь; 0,05 % крем, мазь |
| II – сильные | Мометазон (фуроат) 0,1 % мазь, крем, раствор Триамцинолона ацетонид 0,1 % мазь |
| III – умеренно сильные | Бетаметазон (валерат) 0,1 % крем, мазь Флутиказон (пропионат) 0,005 % мазь, 0,05 % крем |
| IV – средней силы | Флуоцинолона ацетонид 0,025 % мазь, крем, гель, линимент Мометазон (фуроат) 0,1 % мазь, крем, раствор Триамцинолона ацетонид 0,025 % мазь Метилпреднизолона ацепонат 0,1 % жирная мазь, мазь, крем, эмульсия |
| V – средней силы | Бетаметазон (валерат) 0,1 % крем Гидрокортизон (бутират) 0,1 % мазь, крем, эмульсия, раствор Флуоцинолона ацетонид 0,025 % крем, гель, линимент |
| VI – средней силы | Алклометазон (дипропионат) 0,05 % мазь, крем |
| VII – слабые | Гидрокортизон (ацетат) 0,5 %, 1 % мазь Преднизолон 0,5 % мазь |
Показания и противопоказания
Перечень показаний, при которых целесообразно применение топических стероидных препаратов (ГКС), довольно обширен. Самыми распространенными показаниями к их назначению являются:
Выбор конкретного препарата зависит, прежде всего, от заболевания и локализации поражения. В зависимости от вида патологии и участка, который необходимо обрабатывать, подбирают и активный компонент, и лекарственную форму, и концентрацию.
Например, топические ГКС высокой силы применяют для лечения обострений очаговой алопеции, резистентного (устойчивого) атопического дерматита, гиперкератотической экземы, красного плоского лишая, тяжелого контактного дерматита и тяжелой экземы кистей [5].
Топические ГКС средней силы применяют при сильном анальном воспалении, сухой экземе, атопической экземе у детей, атопическом дерматите, себорейном дерматите и ряде других заболеваний [5].
Топические ГКС, относящиеся к категории «слабые», показаны при пеленочном дерматите (в тяжелой форме), а также дерматите век и интертриго (дерматите в складках кожи) [5].
Топические стероиды могут назначаться как при обострениях дерматологических заболеваний до наступления периода ремиссии, так и для лечения хронического воспалительного процесса.
Противопоказаниями к применению топических ГКС служат:
Побочные действия топических глюкокортикостероидов
Этот вопрос нередко волнует потребителей. Чтобы первостольники могли быстро и легко развеять сомнения клиентов, мы сформировали несколько убедительных аргументов в формате диалогов с покупателями.
Гормоны, пусть даже наружно, лучше не использовать, у них много побочных эффектов.
Ответ: Большинство препаратов этой группы хорошо переносятся. Побочные эффекты, как правило, развиваются при использовании топических ГКС высокой силы, при обработке больших по площади участков на протяжении длительного времени [2].
Гормональные мази тоже всасываются в кровь, поэтому лучше обходиться без них.
Ответ: Современные топические ГКС имеют крайне низкую абсорбцию и практически не всасываются в кровь, действуя локально в очаге воспаления.
Для лечения детей лучше не использовать гормональные мази — к ним может развиться привыкание.
Ответ: Топические кортикостероиды, которые разрешены для использования в детской практике, например, метилпреднизолона ацепонат, практически не всасываются в кровь, действуя локально в очаге воспаления. При их применении, как правило, очень быстро облегчается состояние и к тому же снижается вероятность рецидивов заболевания. Главное — соблюдать кратность применения и курс лечения.
Возвращаясь к вопросу о побочных эффектах топических ГКС, следует отметить, что самой распространенной неблагоприятной реакцией является атрофия кожи. Она проявляется в виде истончения кожи, блеска, телеангиэктазий, синяков, стрий, покраснения и изменения пигментации. Самой низкой способностью вызывать атрофию кожи обладают гидрокортизона ацепонат, флутиказона пропионат и метилпреднизолона ацепонат. Поэтому их можно использовать для лечения поражений на лице, мошонке, а также на больших участках тела, в том числе, и у детей [2].
Для минимизации вероятности развития побочных эффектов топические ГКС рекомендуют использовать краткими курсами (не более 3–4 недель). С увеличением продолжительности лечения вероятность появления неблагоприятных реакций возрастает.
При использовании топических глюкокортикостероидов у грудных детей следует помнить, что нанесение препаратов в складки кожи и под подгузник может сопровождаться развитием окклюзионного эффекта и локальным повышением концентрации активного компонента. В связи с этим не рекомендуется наносить препараты в местах соприкосновения подгузников и пеленок с кожей [6].
О чем предупредить клиента?
Отпуская препарат, уместно отметить:
Отдельные представители топических ГКС
Перечень применяемых препаратов этой группы довольно велик, поэтому мы отметим особенности только тех средств, которые имеют безрецептурные формы.
Гидрокортизон — слабый синтетический ГКС, уместно использовать при острых и подострых кожных процессах без мокнутия. Для улучшения проникновения рекомендовано наносить легкими массирующими движениями. При появлении положительной динамики кратность применения уменьшают с 1–3 раз в сутки до 2–3 раз в неделю. Разрешен к применению у детей старше 2 лет курсами не дольше 7 дней в минимально эффективных дозах [6].
Алклометазон — ГКС от слабой до умеренной степени активности. Абсорбция через кожу зависит от целостности кожных покровов и вида лекарственной формы. У здоровых людей в течение 8 часов абсорбируется 3 % алклометазона. Может применяться на нежных и чувствительных участках тела — лицо, шея, грудь, область гениталий. Рекомендуют при острых и подострых воспалительных заболеваниях, в том числе и сопровождающихся мокнутием. Возможно применение при беременности (под контролем врача), кормлении грудью, а также у детей старше 6 месяцев. Максимальная длительность лечения у детей — 3 недели.
Бетаметазона дипропионат — сильный ГКС, при использовании на коже лица курс лечения не должен превышать 5 дней во избежание развития розацеа, периорального дерматита или акне. Может применяться у детей с 1 года по строгим показаниям и под врачебным контролем.
Метилпреднизолона ацепонат — ГКС средней силы, может применяться у детей с 4 месяцев жизни курсами до 4 недель. Выпускается в форме эмульсии, крема, мази и жирной мази, что позволяет подобрать препарат индивидуально, в зависимости от поражения.
Кортикостероиды. Кортикостероидные препараты
Содержание
Гормоны коры надпочечников [ править | править код ]
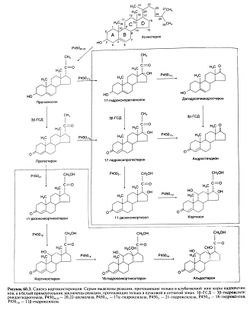
Кора надпочечников синтезирует стероидные гормоны двух классов: кортикостероиды, относящиеся по химической структуре к С21-стероидам, и андрогены, относящиеся к С19-стероидам (рис. 60.3)
. Традиционное деление кортикостероидов на глюкокортикоиды и минералокортикоиды отражает их преобладающее физиологическое действие соответственно на углеводный обмен и водно-электролитный баланс. У человека основной глюкокортикоид — кортизол, а основной минералокортикоид — альдостерон. Величины суточной секреции у человека наиболее важных кортикостероидов — кортизола и альдестерона — и их нормальные сывороточные концентрации указаны в табл. 60.1.
Раньше считали, что в сутки образуется 20 мг кортизола, но, как показали более поздние исследования, эта величина ближе к 10 мг (Esteban et al., 1991).
У женщин кора надпочечников служит также важным источником андрогенов, но при надпочечниковой недостаточности введение одних лишь глюко- и минералокортикоидов увеличивает среднюю продолжительность жизни до нормальной. Иными словами, надпочечниковые андрогены не являются жизненно необходимыми. Однако уровень дегидроэпиандростерона (главного надпочечникового андрогена) изменяется с возрастом, достигая максимума на третьем десятилетии жизни, а затем постепенно снижаясь. Кроме того, при многих хронических заболеваниях концентрация дегидроэпиандростерона в плазме крайне низка. На основании этого было выдвинуто предположение, что прием дегидроэпиандростерона может хотя бы отчасти смягчить симптомы старения. Обсуждалась необходимость применения дегидроэпиандростерона при первичной и вторичной надпочечниковой недостаточности. По данным одного исследования, добавление дегидроэпиандростерона (50 мг внутрь один раз в сутки утром) к стандартной схеме заместительной терапии надпочечниковой недостаточности у женщин улучшает самочувствие и усиливает половое влечение (Arlt et al., 1999).
Физиологическое и фармакологическое действие [ править | править код ]
Эффекты кортикостероидов многочисленны и разнообразны. Они влияют на углеводный, белковый и липидный обмен, поддерживают водно-электролитный баланс и функции сердечно-сосудистой, иммунной, эндокринной и нервной систем, а также почек и скелетных мышц. Кроме того, каким-то не до конца выясненным путем глюкокортикоиды придают организму способность противостоять стрессу (например, при боли или резких изменениях окружающей среды). Без коры надпочечников выживание возможно лишь в специальных условиях: при достаточном и регулярном питании, потреблении относительно больших количеств поваренной соли и поддержании определенной температуры внешней среды.
До недавнего времени действие глюкокортикоидов разделяли на физиологическое (в нормальных физиологических концентрациях) и фармакологическое (в больших концентрациях). Согласно более поздним представлениям, основное фармакологическое действие глюкокортикоидов, а именно противовоспалительное и иммуносупрессивное, имеет место и в физиологических условиях. Многие медиаторы воспаления снижают сосудистый тонус и могли бы вызывать острую сердечно-сосудистую недостаточность, если бы не встречали противодействия со стороны эндогенных глюкокортикоидов. Эту гипотезу подтверждает резкое (по меньшей мере, десятикратное) возрастание суточной секреции глюкокортикоидов при выраженном стрессе. Кроме того, их фармакологические и многие физиологические эффекты опосредуются, по-видимому, одними и теми же рецепторами (см. ниже), поэтому побочное и лечебное действие различных глюкокортикоидов, назначаемых больному, не разделимы.
Действие кортикостероидов сложным образом связано с действием других гормонов. Например, в отсутствие катехоламинов, обладающих липолитическим действием, кортизол почти не влияет на скорость липолиза в липоцитах. И наоборот, в отсутствие глюкокортикоидов адреналин и норадреналин лишь очень слабо влияют на липолиз. Введение малой дозы глюкокортикоидов резко усиливает липолитическое действие катехоламинов. Это, скорее всего, связано с изменением синтеза белка под влиянием глюкокортикоидов. Такой эффект, облегчающий действие других гормонов, называют пермиссивным.
Кортикостероиды различаются по способности задерживать натрий в организме, влиянию на углеводный обмен (например, на отложение гликогена и глюконеогенез в печени) и противовоспалительному действию. В целом, жизнь животных, подвергнутых адреналэктомии, лучше поддерживают те кортикостероиды, которые активнее задерживают натрий (то есть кортикостероиды с высокой минералокортикоидной активностью). Влияние кортикостероидов на углеводный обмен (глюкокортикоидная активность) пропорционально их противовоспалительной активности. В то же время их минералокортикоидная активность не зависит от глюкокортикоидной и противовоспалительной активности. Как уже говорилось, минералокортикоидная и глюкокортикоидная (как и противовоспалительная) активность опосредованы разными рецепторами. Сравнительная активность глюкокортикоидов приведена в табл. 60.2.
Некоторые глюкокортикоиды (например, кортизол и преднизон) проявляют и существенную минералокортикоидную активность. Однако при первичной надпочечниковой недостаточности заместительная терапия этими препаратами (см. ниже) не компенсирует отсутствия альдостерона, поэтому приходится одновременно вводить более активные минералокортикоиды. Напротив, активный минералокортикоид альдостерон слабо влияет на углеводный обмен. При физиологических концентрациях или в дозах, оказывающих максимальное действие на водноэлектролитный баланс, альдостерон почти не обладает глюкокортикоидной активностью, то есть является чистым минералокортикоидом.
Общие механизмы действия кортикостероидов [ править | править код ]
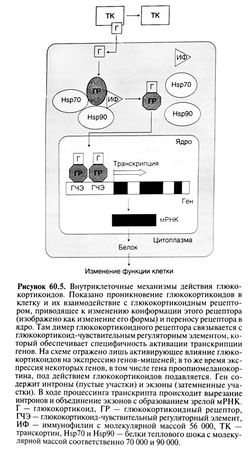
Взаимодействуя с внутриклеточными рецепторами, кортикостероиды регулируют экспрессию генов-мишеней и тем самым изменяют количество и спектр синтезируемых белков (рис. 60.5). Так как изменение в синтезе белка требует времени, большинство эффектов кортикостероидов проявляется не сразу, а лишь через несколько часов. Поэтому нельзя ожидать немедленного эффекта от введения глюкокортикоидов. Хотя под действием кортикостероидов экспрессия большинства генов-мишеней усиливается, описано и подавление экспрессии некоторых генов (см. ниже). В отличие от действия, опосредованного изменением экспрессии генов-мишеней, некоторые эффекты кортикостероидов возникают немедленно и связаны с влиянием этих гормонов на мембранные рецепторы (Christ et al., 1999).
Структура кортикостероидных рецепторов была выяснена с помощью молекулярного клонирования. Эти рецепторы принадлежат к суперсемейству белков, опосредующих эффекты ряда небольших гидрофобных молекул, включая стероидные и тиреоидные гормоны, кальцитриол и ретиноиды (Mangelsdorf et al., 1995). Все эти белки содержат два консервативных домена: один из них, состоящий примерно из 70 аминокислотных остатков, имеет два участка связывания цинка (цинковые пальцы) и необходим для взаимодействия рецептора с определенными последовательностями ДНК, а второй, расположенный на С-конце молекулы, связывает гормон.
Глюкокортикоидный рецептор [ править | править код ]
Регуляция экспрессии генов глюкокортикоидами [ править | править код ]
После связывания гормона глюкокортикоидный рецептор освобождается от других белков, образует димер и перемещается в клеточное ядро, где и взаимодействует с определенными последовательностями ДНК на регуляторных участках генов-мишеней. Короткие последовательности ДНК, распознаваемые активированным рецептором, носят название глюкокортикоид-чувствительных регуляторных элементов и обеспечивают специфичность влияния глюкокортикоидов на экспрессию генов. Основу таких элементов составляет устойчивая последовательность, несовершенный палиндром ГГТАЦАХХХТТТЦТ (X — любой нуклеотид), с которым и связывается димер глюкокортикоидного рецептора. Сложные механизмы активирующего влияния рецептора на транскрипцию генов выяснены не полностью, но, по-видимому, включают его взаимодействие с кофакторами и белками, формирующими основу транскрипционного аппарата. Установлены также гены, транскрипция которых подавляется глюкокортикоидами (Webster and Cidlowski, 1999). Один из них — ген проопиомеланокортина, подавление транскрипции которого в кортикотропных клетках гипофиза — существенное звено в регуляции гипоталамо-гипофизарно-надпочечниковой системы. В этом случае глюкокортикоидные рецепторы взаимодействуют с особым глюкокортикоид-чувствительным регуляторным элементом в промоторе гена проопиомеланокортина.
Без глюкокортикоидов и, вероятно, их рецепторов жизнь невозможна, но взаимодействие рецепторов с глюкокортикоид-чувствительными регуляторными элементами ДНК не столь необходимо. Это подтверждается данными о том, что трансгенные мыши, полностью лишенные глюкокортикоидных рецепторов, погибают сразу же после рождения, тогда как мыши, у которых дефекты рецепторов препятствуют их связыванию с ДНК. выживают (Reichardt et al., 1998). Отсюда следует, что важность глюкокортикоидных рецепторов определяется их взаимодействием с другими белковыми факторами транскрипции (Xu et al., 1999). Действительно, обнаружены белок-белковые взаимодействия этих рецепторов с факторами транскрипции NFkB и АР-1, которые регулируют экспрессию многих белков иммунной системы (McKay and Cidlowski, 1999). В результате подавляется экспрессия генов, кодирующих ряд цитокинов (регуляторных молекул, играющих ведущую роль в иммунных и воспалительных реакциях), и таких ферментов, как коллагеназа и стромелизины (предположительно играющих основную роль в деструкции суставов при артрите). Таким образом, противовоспалительная и иммуносупрессивная активность глюкокортикоидов во многом связана с подавлением экспрессии ряда генов.
Регуляция экспрессии генов минералокортикоидами [ править | править код ]
Минералокортикоидные рецепторы также представляют собой лиганд-чувствительные регуляторы транскрипции, которые связываются с аналогичными (если не теми же) гормон-чувствительными регуляторными элементами ДНК. что и глюкокортикоидные рецепторы. Действие минералокортикоилных рецепторов изучено хуже, чем глюкокортикоидных, но основные принципы, по-видимому, в обоих случаях одинаковы: минералокортикоидные рецепторы также связываются с белком теплового шока Hsp-90 и также активируют транскрипцию определенных генов-мишеней. Различия в ДНК-связывающих доменах глюко-и минералокортикоидных рецепторов, которые могли бы объяснить разницу в активации генов-мишеней, пока не обнаружены. Эти рецепторы различаются по способности подавлять активирующее действие факторов транскрипции АР-1 на экспрессию генов (Pearce and Yamamoto, 1993). Таким образом, причина различного влияния этих рецепторов на клетки может заключаться в их неодинаковом взаимодействии с другими факторами транскрипции. Кроме того, минералокортикоидные рецепторы, в отличие от глюкокортикоидных, имеются лишь в некоторых тканях — в основном в почках (в дистальных извитых канальцах и корковом отделе собирательных трубочек), толстой кишке, слюнных и потовых железах, гиппокампе.
Альдостерон изменяет обмен натрия и калия преимущественно за счет влияния на главные клетки дистальных канальцев и собирательных трубочек, тогда как действие на секрецию Н+ осуществляется в основном через вставочные клетки. Недавние исследования позволили выяснить некоторые механизмы действия альдостерона на транспорт воды и электролитов. Связываясь с минералокортикоидными рецепторами в клетках-мишенях, альдостерон запускает цепь реакций, включающую быструю индукцию киназы, которая регулируется факторами сыворотки и глюкокортикоидами. Эта киназа фосфорилирует и активирует чувствительные к амилориду натриевые каналы в апикальной мембране эпителиальных клеток (Chen et al., 1999). Усиленный вход натрия стимулирует Na+,К+-АТФазу в базолатеральной мембране. Помимо такого быстрого действия альдостерон усиливает и синтез отдельных компонентов этих мембранных белков.
Дальнейшему выяснению роли минералокортикоидных рецепторов и их генов-мишеней в регуляции водно-электролитного баланса способствовало обследование больных с такими редкими генетическими нарушениями, как псевдогипоапьдостеронизм и синдром Лиддла. При псевдогипоальдосгеронизме, несмотря на повышенный уровень минералокортикоидов, наблюдаются симптомы дефицита минералокортикоидов (например, гиповолемия, артериальная гипотония, гиперкалиемия и метаболический ацидоз). Молекулярно-генетические исследования позволили выделить разные группы больных с этим заболеванием. У одних заболевание наследуется аутосомно-рецессивно и обусловлено инактивирующими мутациями генов, кодирующих субъединицы чувствительных к амилориду натриевых каналов эпителиальных клеток. У других имеется аутосомно-доминантная форма псевдогипоальдостеронизма, вызванная инактивирующими мутациями гена минералокортикоидного рецептора (Geller et al., 1998). Синдром Лиддла, наследуемый аутосомно-доминантно, обусловлен активирующими мутациями генов чувствительных к амилориду натриевых каналов (Shimketsetal., 1994). Постоянная активация этих каналов приводит к артериальной гипертонии, гипокалиемии и метаболическому алкалозу, несмотря на низкие уровни ренина и альдостерона в плазме.
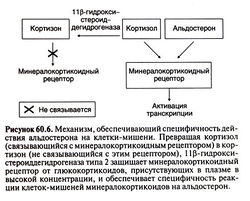
Специфичность действия кортикостероидов, не зависящая от рецепторов. Клонирование генов глюкокортикоидного и минера-локортикоидного рецепторов позволило обнаружить, что альдостерон (классический минералокортикоид) и кортизол (преимущественно глюкокортикоид) связываются с минералокортикоидным рецептором с равным сродством. Почему же минералокортикоидный рецептор взаимодействует именно с альдо-стероном, а не с глюкокортикоидами, уровень которых в крови гораздо выше? По крайней мере частичный ответ на этот вопрос дало открытие фермента 1 ip-гидроксистероиддегидрогеназы типа 2, от которого и зависит специфичность действия кортикостероидов, особенно в почках, толстой кишке и слюнных железах. Этот фермент превращает глюкокортикоиды (например, кортизол) в 11-кето-производные (например, кортизон), не взаимодействующие с минералокортикоидными рецепторами, и тем самым препятствует действию глюкокортикоидов в тканях, чувствительных к минералокортикоидам (рис. 60.6). Альдостерон же, находящийся в организме преимущественно в форме полуацеталя, устойчив к действию 1 ф-гидроксистеро-иддегидрогеназы. В отсутствие этого фермента (что характерно для наследственного заболевания — синдрома мнимого избытка минералокортикоидов) находящийся в избытке кортизол действует на минералокортикоидные рецепторы, что приводит к тяжелой гипокалиемии и артериальной гипертонии. Симптомы избытка минералокортикоидов (в частности, артериальная гипертония) возникают также при ингибировании 11 β-гидро-ксистероиддегидрогеназы глициризиновой кислотой, содержащейся в лакрице.
Углеводный и белковый обмен [ править | править код ]
Глюкокортикоиды оказывают выраженное влияние на углеводный и белковый обмен. Можно считать, что они защищают глюкозозависимые ткани (такие, как головной мозг и сердце) от голодания. В печени глюкокортикоиды стимулируют глюконеогенез и накопление гликогена. В периферических тканях глюкокортикоиды подавляют утилизацию глюкозы, усиливают распад белка и активируют липолиз, что дает аминокислоты и глицерин, используемые для глюконеогенез а. Конечный результат сводится к повышению концентрации глюкозы в крови. Поэтому назначение глюкокортикоидов может усугубить нарушения углеводного обмена у больных сахарным диабетом и вызвать гипергликемию у лиц с предрасположенностью к этому заболеванию.
Механизм подавляющего действия глюкокортикоидов на утилизацию глюкозы периферическими тканями не совсем понятен. глюкокортикоиды снижают поглощение глюкозы жировой тканью, кожей, фибробластами, тимоцитами и нейтрофилами. Считается, что это связано с перемещением переносчиков глюкозы из клеточной мембраны внутрь клеток. Уменьшение поглощения глюкозы периферическими тканями сопровождается усилением катаболизма, что приводит к атрофии лимфоидной ткани, снижению мышечной массы, отрицательному азотистому балансу и истончению кожи.
Механизмы стимулирующего действия глюкокортикоидов на глюконеогенез также не совсем ясны. Аминокислоты, выделяемые рядом тканей под влиянием глюкокортикоидов, поступают в печень, где используются для глюконеогенеза и образования гликогена. В печени глюкокортикоиды усиливают синтез многих ферментов глюконеогенеза и метаболизма аминокислот, включая фосфоенолпируваткарбоксикиназу, глюкозо-6-фосфа-тазу и фруктозо-2,6-дифосфатазу. В регуляции экспрессии гена фосфоенолпируваткарбоксикиназы принимают участие не только глюкокортикоиды, но и инсулин, глюкагон и катехоламины. Влияние всех этих гормонов на экспрессию гена фосфоенолпируваткарбоксикиназы отражает сложность регуляции глюконеогенеза в организме.
Липидный обмен [ править | править код ]
Точно установлены два эффекта глюкокортикоидов на липидный обмен. Один из них — резкое перераспределение жира, наблюдающееся при гиперкортизолемии, характерной для синдрома Кушинга. Другой — усиление липолитического действия других факторов, например СТГ и β-адреностимуляторов, на липоциты (пермиссивное действие), что приводит к повышению уровня свободных жирных кислот. Перераспределение жира проявляется увеличением жировых отложений на шее (жировой горбик), лице (лунообразное лицо) и в надключичной области одновременно с потерей жира в конечностях.
Согласно одной из гипотез, липоциты туловища и конечностей различаются по чувствительности к инсулину и пермис-сивному действию глюкокортикоидов. Липоциты туловища особенно чувствительны к гиперинсулинемии, которая возникает в ответ на вызываемую глюкокортикоидами гипергликемию, тогда как липоциты конечностей менее чувствительны к инсулину, и в них под действием глюкокортикоидов и других гормонов усиливается липолиз.
Водно-электролитный баланс [ править | править код ]
По минералокортикоидной активности альдостерон намного превосходит все (остальные природные кортикостероиды. На это указывает сохранение водно-электролитного баланса у подвергнутых гипофизэктомии животных, у которых надпочечники не секретируют глюкокортикоиды. Минерало-кортикоиды усиливают реабсорбцию натрия, действуя на клетки дистальных канальцев и собирательных трубочек почек, и увеличивают экскрецию калия и Н+ с мочой. Можно считать, что альдостерон стимулирует обмен между ионами Na+ и К+ (или Н+), хотя молекулярный механизм перемещения этих ионов в почечных канальцах отличается от простого обмена одного катиона на другой.
Это действие на транспорт электролитов в почках и в других тканях (толстой кишке, слюнных и потовых железах) определяет физиологические и фармакологические эффекты минералокортикоидов. Поэтому для гипераль-достеронизма характерны задержка натрия, сопровождающаяся увеличением объема внеклеточной жидкости, нормальная или слегка повышенная концентрация натрия в плазме, гипокалиемия и алкалоз. Напротив, дефицит альдостерона сопровождается потерей натрия и уменьшением объема внеклеточной жидкости на фоне гипо-натриемии, гиперкалиемии и ацидоза. При хроническом гиперальдостеронизме наблюдается артериальная гипертония, тогда как дефицит альдостерона обусловливает артериальную гипотонию и может приводить к острой сердечно-сосудистой недостаточности. Из-за выпадения влияния минералокортикоидов на обмен электролитов в потовых железах больные с надпочечниковой недостаточностью в жару особенно предрасположены к потере натрия и воды с потом.
глюкокортикоиды также влияют на водно-электролитный баланс. Они необходимы для поддержания СКФ и функции почечных канальцев. глюкокортикоиды увеличивают почечную экскрецию воды; когда-то пробу с водной нагрузкой использовали для выявления надпочечниковой недостаточности. Задержка воды при первичной надпочечниковой недостаточности отчасти связана с повышенной секрецией АДГ, который стимулирует реабсорбцию воды в почках.
Помимо действия на транспорт одновалентных катионов и воды глюкокортикоиды влияют и на обмен кальция. Они каким-то образом препятствуют всасыванию кальция в кишечнике, одновременно усиливая его экскрецию почками. Сочетание этих эффектов приводит к снижению содержания кальция в организме. Сердечно-сосудистая система. Как уже отмечалось, действие кортикостероидов на сердечно-сосудистую систему связано прежде всего с изменением почечной экскреции натрия под влиянием минералокортикоидов. Это действие особенно ярко проявляется при первичном гиперальдостеронизме. Развивающаяся при этом расстройстве артериальная гипертония ведет к дальнейшему поражению сердечно-сосудистой системы, способствуя развитию атеросклероза, инсультов и гипертрофической кар-диомиопатии. Механизм артериальной гипертонии остается не совсем ясным, но низкосолевая диета может значительно снижать АД.
глюкокортикоиды повышают также чувствительность сосудов к другим вазоактивным веществам. При надпочечниковой недостаточности снижается реакция на нор-адреналин и ангиотензин 11. Это отчасти объясняют экспериментальные исследования, в которых показано, что глюкокортикоиды увеличивают число адренорецепторов в сосудистой стенке. Если надпочечниковая недостаточность обычно сопровождается артериальной гипотонией, то у больных с повышенной секрецией глюкокортикоидов (как при гипофизарном синдроме Кушинга) или у получающих синтетические глюкокортикоиды (даже почти лишенные минералокортикоидной активности) наблюдается артериальная гипертония.
Механизмы развития артериальной гипертонии под влиянием глюкокортикоидов не известны. Не ясно, в частности, связано ли повышение АД при синдроме Кушинга со стимуляцией глюкокортикоидных или минералокортикоидных рецепторов. При артериальной гипертонии на фоне избытка глюкокортикоидов низкосолевая диета обычно неэффективна (в отличие от артериальной гипертонии при гиперальдостеронизме).
Обнаружено и прямое действие альдостерона на сердце и сосуды. У крыс, которым вводили альдостерон, наблюдалась не только артериальная гипертония, но и кардиосклероз (Funderet al., 1997). Предполагается, что последний обусловлен не повышением АД, а прямым действием альдостерона на сердце, так как спиронолактон (блокатор минералокортикоидных рецепторов) предотвращал развитие кардиосклероза, не влияя на АД. Это объясняет (по крайней мере, частично) эффективность спи-ронолактона при сердечной недостаточности (Pitt et al., 1999). Скелетные мышцы. Пермиссивное действие кортикостероидов необходимо для нормальной работы скелетных мышц; снижение работоспособности — одно из основных проявлений надпочечниковой недостаточности. Первичная надпочечниковая недостаточность часто сопровождается мышечной слабостью и утомляемостью, которые, как считают, вызваны нарушением кровообращения. Однако работа мышц страдает и при избытке глюко-и минералокортикоидов. Мышечная слабость при первичном гиперальдостеронизме связана в основном с ги-покалиемией, а не с прямым влиянием минералокортикоидов на скелетные мышцы. В основе же атрофии скелетных мышц при хроническом избытке глюкокортикоидов (будь то вследствие глюкокортикоидной терапии или эндогенной гиперкортизолемии) лежат неизвестные механизмы. Этот эффект, получивший название стероидной миопатии, отчасти объясняет слабость и утомляемость, характерные для синдрома Кушинга (см. ниже). ЦНС. Многие влияния кортикостероидов на ЦНС опосредованы действием этих гормонов на АД, а также на уровень глюкозы и электролитов в плазме. Изучение распределения и функции рецепторов стероидных гормонов в головном мозге способствовало выявлению и прямого действия кортикостероидов в ЦНС, проявляющегося изменениями настроения, поведения и возбудимости головного мозга.
При первичной надпочечниковой недостаточности иногда наблюдаются различные изменения психики, в том числе апатия, депрессия и раздражительность, порой развивается явный психоз. Заместительная глюкокортикоидная терапия приводит к исчезновению этих симптомов. Существенное клиническое значение имеют и реакции ЦНС на введение глюкокортикоидов. У большинства больных при этом улучшается настроение, что дает ощущение благополучия, несмотря на продолжающуюся болезнь. Иногда возникают более глубокие изменения поведения, включая эйфорию, бессонницу, беспокойство и психомоторное возбуждение. У меньшего, но все же значительного числа больных, получающих глюкокортикоиды, развиваются тревожное состояние, депрессия или даже явный психоз. При синдроме Кушинга неврозы и психозы довольно часты. После отмены глюкокортикоидов или излечения синдрома Кушинга эти нарушения обычно исчезают.
Механизмы влияния кортикостероидов на активность нейронов не известны, но важно подчеркнуть, что возбудимость нейронов может зависеть от местной продукции стероидов (называемых нейростероидами) в головном мозге (Baulieu, 1998). У грызунов глюкокортикоиды повреждают нейроны гиппокампа, приводя к ухудшению памяти (Lupien and McEwan, 1997). У человека также обнаружена связь между высоким базальным уровнем кортизола и атрофией гиппокампа с ухудшением памяти (Lupien et al., 1998). Если эти результаты удастся подтвердить, они будут иметь важное значение для профилактики возрастного ослабления памяти и оправдают применение средств, уменьшающих влияние глюкокортикоидов на нейроны гиппокампа при старении.
Кроветворение [ править | править код ]
Судя по тому, что при синдроме Кушинга часто наблюдается эритроцитоз, а при первичной надпочечниковой недостаточности — нормоцитарная нормо-хромная анемия, глюкокортикоиды как-то влияют на содержание гемоглобина и эритроцитов в крови. Более четко эффекты глюкокортикоидов проявляются при аутоиммунной гемолитической анемии, когда их иммуносу-прессивное действие ослабляет процесс разрушения эритроцитов.
глюкокортикоиды влияют и на лейкоциты. При первичной надпочечниковой недостаточности, как отмечал еще Аддисон, наблюдается увеличение массы лимфоидной ткани и числа лимфоцитов в крови. Напротив, для синдрома Кушинга характерны лимфопения и уменьшение массы лимфоидной ткани. Введение глюкокортикоидов приводит к снижению общего числа лимфоцитов, эозинофилов, моноцитов и базофилов. После однократного введения гидрокортизона снижение числа этих клеток в крови происходит через 4—6 ч и сохраняется в течение суток. Этот эффект связан в основном с перераспределением клеток, а не с их разрушением. Число же нейтрофилов под влиянием глюкокортикоидов возрастает: ускоряется их выход из костного мозга, замедляется исчезновение из крови и уменьшается краевое стояние. глюкокортикоиды эффективны при некоторых лимфомах, что может быть связано со способностью этих гормонов индуцировать апоптоз клеток лимфоидного ряда.
Противовоспалительное и иммуносупрессивное действие [ править | править код ]
глюкокортикоиды изменяют не только число, но и активность лимфоцитов. Это одна из важнейших сторон противовоспалительного и иммуносупрессивного действия глюкокортикоидов. Они предотвращают или подавляют воспалительную реакцию, развивающуюся в ответ на механические, химические, инфекционные воздействия, на введение антигенов и на облучение. Хотя причина болезни при этом не устраняется, подавление воспалительной реакции имеет огромное клиническое значение; именно поэтому глюкокортикоиды относятся к числу наиболее часто назначаемых средств. Им принадлежит неоценимая роль в лечении и тех заболеваний, в основе которых лежат нежелательные иммунные реакции, будь то гуморальные (например, крапивница, гл. 65) или клеточные (например, отторжение трансплантата, гл. 53). Иммуносупрессивный и противовоспалительный эффекты глюкокортикоидов трудно разделить, вероятно потому, что оба они связаны с подавлением функции лейкоцитов (Chrousos, 1995).
В основе противовоспалительного действия глюкокортикоидов лежат различные механизмы. Эти вещества подавляют продукцию различных факторов, участвующих в развитии воспаления. Уменьшается выделение вазоактивных веществ и хемоат-трактантов, секреция липаз и протеаз, перемещение лейкоцитов из сосудов в очаги повреждения и, наконец, фиброз. Все это значительно подавляет воспаление. Некоторые клетки и факторы, на которые действуют глюкокортикоиды, перечислены в табл. 60.3.
Влияние стресса на иммунитет, равно как и участие в этом гипоталамо-гипофизарно-надпочечниковой системы, надежно установлено (Sapolsky et al., 2000). Отсюда понятно, что глюко-кортикоиды являются важнейшими физиологическими регуляторами иммунной системы, защищающими организм от опасных последствий неконтролируемого воспаления.
Такие воздействия, как травмы, инфекции и болезни, сопровождаются усилением продукции цитокинов — сигнальных молекул, обеспечивающих взаимодействие моноцитов, макрофагов, Т- и В-лимфоцитов в иммунном ответе. К цитокинам относятся ИЛ-1, ИЛ-6 и ФНОа, которые стимулируют гипотала-мо-гипофизарно-надпочечниковую систему. Наиболее широким спектром действия обладает ИЛ-1. Он стимулирует выделение кортиколиберина гипоталамическими нейронами, непосредственно усиливает секрецию АКТГ гипофизом и может повышать продукцию глюкокортикоидов надпочечниками (Turnbull and Rivier, 1999). Как отмечалось выше, глюкокортикоиды, в свою очередь, подавляют иммунную систему, препятствуя секреции цитокинов, в том числе интерферона у, ГМ-КСФ, интерлейкинов (ИЛ-1, ИЛ-2, ИЛ-3, ИЛ-6, ИЛ-8, ИЛ-12) и ФНОа. Таким образом, гипоталамо-гипофизарно-надпочечниковая и иммунная системы при стрессе взаимодействуют, что, по-видимому, играет важную физиологическую роль.
Хотя глюкокортикоиды традиционно считаются иммунодепрессантами, ряд данных свидетельствует, что, угнетая клеточный иммунитет, они усиливают выработку антител, то есть стимулируют гуморальный иммунитет (Elenkov and Chrousos, 1999). Механизмы такого действия глюкокортикоидов не ясны; возможно, глюкокортикоиды подавляют активность Т-хелперов типа 1, но активируют Т-хелперы типа 2 (гл. 53).
Фармакокинетика [ править | править код ]
Всасывание [ править | править код ]
Гидрокортизон и его многочисленные аналоги, в том числе синтетические, эффективны при приеме внутрь. Некоторые водорастворимые эфиры гидрокортизона и сходные соединения вводят в/в, что приводит к быстрому возрастанию их концентрации во внеклеточной жидкости. Более длительные эффекты обеспечивает в/м введение суспензий гидрокортизона, его аналогов и эфиров. Небольшие изменения химической структуры могут заметно сказаться на скорости всасывания, быстроте и продолжительности действия препарата.
глюкокортикоиды поступают в кровь даже при местном их применении (введении в суставы, конъюнктивальный мешок, нанесении на кожу и вдыхании). Если препараты применяются длительно, наносятся на большие участки кожи или места их нанесения закрывают окклюзионной повязкой, то могут возникать и системные эффекты, в том числе угнетение гипоталамо-гипофизарно-надпочечниковой системы.
Транспорт и элиминация [ править | править код ]
В норме более 90% гидрокортизона, попавшего в кровь, обратимо связывается с белками плазмы. Лишь свободный препарат проникает в клетки и оказывает действие. Кортикостероиды связываются в основном с двумя белками — транскортином и альбумином. Секретируемый печенью транскортин представляет собой а,-глобулин, обладающий высоким сродством к стероидам, но относительно малой емкостью. Альбумин также продуцируемый печенью, обладает малым сродством, но высокой емкостью. При нормальных или низких концентрациях кортикостероидов большая их часть связана с белками. Однако с ростом концентрации участки связывания насыщаются, и концентрация свободных кортикостероидов значительно увеличивается. Кортикостероиды конкурируют друг с другом за участки связывания на транскортине, сродство которого к кортизолу и большинству его синтетических производных выше, чем к альдостерону и метаболитам стероидов, конъюгированным с глюкуроновой кислотой. Поэтому у последней группы соединений свободная фракция выше.
Таблица 60.3. Влияние глюкокортикоидов на различные факторы, участвующие в воспалении и иммунных реакциях
При беременности или приеме эстрогенов сывороточная концентрация транскортина, а также общего и свободного кортизола многократно возрастает. Физиологическое значение этих сдвигов остается неясным.
Все биологически активные кортикостероиды и их синтетические аналоги содержат двойную связь мелщу атомами С-4 и С-5 и кетогруппу в положении 3. Метаболизм стероидных гормонов, как правило, протекает путем последовательного присоединения к их молекулам атомов кислорода или водорода и затем конъюгирования с образованием водорастворимых производных. Восстановление двойной связи между атомами С-4 и С-5, приводящее к потере гормональной активности, происходит как в печени, так и вне ее, но последующее восстановление кетогруппы в положении 3 до гидроксильной группы с образованием тетрагидрокортизола — только в печени. В ферментативных реакциях, протекающих в печени и в меньшей степени — в почках, гидроксильная группа большинства таких восстановленных стероидов взаимодействует с глюкуроновой кислотой или сульфатом. Образующиеся водорастворимые конъюгаты (сульфаты и глюкурониды) — основные формы стероидов, экскрети-руемые с мочой. У человека экскреция стероидов с желчью и калом весьма незначительна.
Синтетические стероиды с кетогруппой в положении II (такие, как кортизон и преднизон) приобретают биологическую активность только после ферментативного восстановления в соответствующие 11 p-гидроксип роизводные. Эту реакцию катализирует в печени 11 β-гидроксистероидцегидро-геназа типа 1. При недостаточности этого фермента (например, при тяжелой печеночной недостаточности или в редких случаях наследственного отсутствия фермента) следует использовать стероиды, не требующие ферментативной активации, то есть гидрокортизон и преднизолон вместо кортизона или преднизона.
Структурно-функциональная зависимость [ править | править код ]
Химические модификации молекулы кортизола позволили получить производные с более избирательной глюкокортикоид-ной или минерапокортикоидной активностью. Многие синтетические глюкокортикоиды, даже в максимальных дозах, почти не влияют на водно-электролитный баланс. Кроме того, удалось получить производные с большей активностью и более длительным действием. Сейчас существует множество глюкокортикоидных препаратов для приема внутрь, парентерального и местного применения. Некоторые из них перечислены в табл. 60.4. Поскольку противовоспалительное и метаболическое действие глюкокортикоидов опосредовано одними и теми же рецепторами, не удается создать препараты только с противовоспалительным действием, не влияющие на углеводный, белковый и жировой обмен или лишенные угнетающего влияния на гипоталамо-гипофизарно-надпочечниковую систему.