легкие 2 степени зрелости у плода что это такое
Легкие 2 степени зрелости у плода что это такое
Введение. Изучение возрастных особенностей и морфометрических характеристик органов плодов и новорожденных представляет интерес не только для морфологических наук, но и для клинических дисциплин, таких как неонатология и педиатрия 2. Это обуславливает актуальность нашей работы.
Цель исследования – изучение развития и возрастных особенностей легких у плодов и новорожденных.
Материалы и методы исследования. Обзор литературы по теме исследования, нами были изучены органокомплексы грудной полости 6 плодов в возрасте: 16; 17; 18, 20, 28, 36 и 2 новорожденных, включающих трахею, бронхи, легкие, сердце с перикардом, которые фиксировали в 10% растворе нейтрального формалина. Проведено препарирование комплекса трахея, бронхи, легкие, проведена органометрия, изготовлен препарат для музея кафедры. Материал был разделен на группы в зависимости от возраста, проведено измерение площади диафрагмальной поверхности; длины щелей легкого; ширина; высота; размеры долей легкого (рис.1). Данные статистически обработаны (Exel).
Рис. 1. Морфометрия легких плода
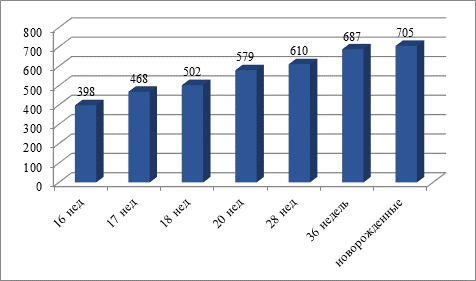
Рис.2. Изменение площади диафрагмальной поверхности легких у плодов и новорожденных (мм2)
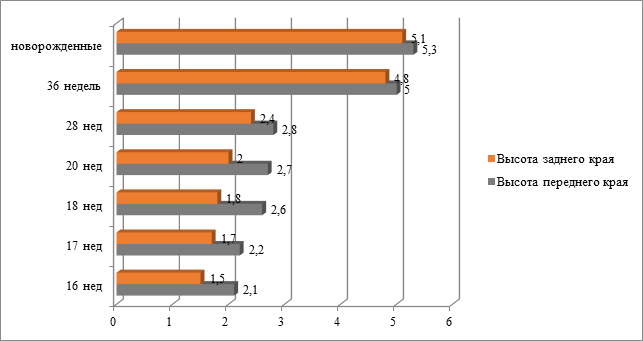
Рис.3. Изменение средней высоты переднего и заднего краев легких у плодов и новорожденных (см)
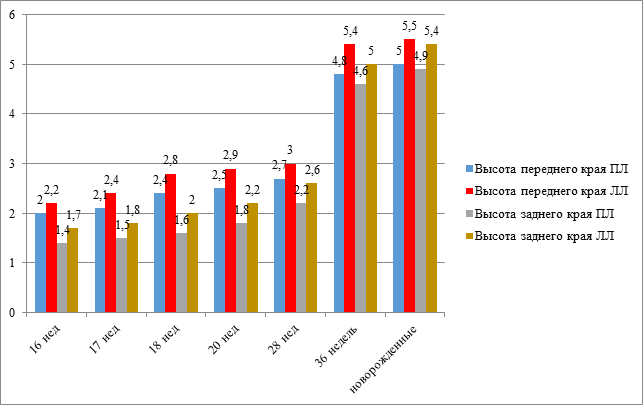
Рис.4. Изменение высоты переднего и заднего краев правого (ПЛ) и левого (ЛЛ) легкого у плодов и новорожденных (см)
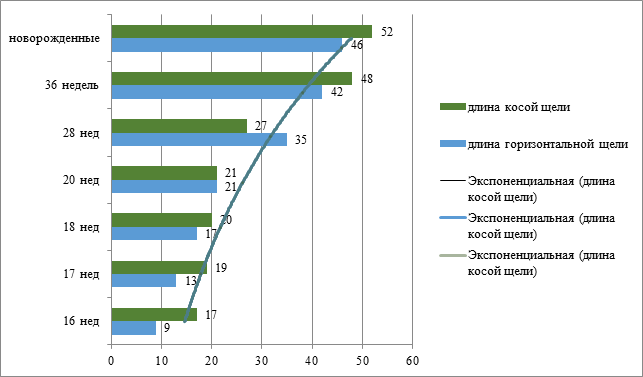
Рис.5. Изменение длины косой и горизонтальной щелей легких у плодов и новорожденных (мм)
Выводы. На основании проведенного исследования мы сделали следующие выводы:
1.В плодном периоде легкие проходят 3 стадии, в которых происходит усложнение внутренней структуры при небольших изменениях морфометрических показателей (увеличение в 1,72 раза).
2. Резкий прирост средней высоты легких по переднему и заднему краям отмечен в период с 28 по 36 неделю.
3. Выявлены различия высоты переднего и заднего краев легких справа и слева на всех этапах развития и возрастные различия в длине косой и горизонтальной щелей легких.
4. Изменения длины горизонтальной щели могут свидетельствовать о увеличении ширины легких в период с 20 по 36 неделю.
5.Обнаруженные нами изменения морфометрических показателей легких объясняются подготовкой дыхательной системы плода к рождению, происходящей во внутриутробном периоде.
Публикации в СМИ
Синдром респираторного дистресса новорождённых
Синдром респираторного дистресса новорождённых (СРДН, (синдром дыхательных расстройств) — тяжёлое патологическое состояние, возникающее чаще у недоношенных детей, с ведущим синдромом острой дыхательной недостаточности.
Этиология и патогенез. При ряде состояний (недоношенность, асфиксия при рождении, СД у матери), протекающих на фоне незрелости лёгких и гипоксии, нарушается синтез сурфактанта лёгочной ткани, что приводит к неполному расправлению лёгких и развитию классического симптомокомплекса — прогрессирующего ателектаза, внутрилёгочного шунтирования крови, гипоксемии и цианоза. На внутренней поверхности альвеол, альвеолярных ходов и респираторных бронхиол обнаруживают отложение гиалиноподобного вещества.
Генетические аспекты • Наследственная предрасположенность возникает при наличии лёгочных протеинозов у родителей • Мутации гена, ассоциированного с сурфактантом белка 1 (178630, 10q21–q24, ген SFTP1) — одна из причин развития СРДН.
Патоморфология • Лёгочная ткань пурпурно-красного цвета • Расширение правых отделов сердца • Артериальный проток может быть открыт • Обширные ателектазы • Гиалиновые мембраны.
Клинические проявления • Начальные признаки возникают в первые часы жизни • Слабый крик после рождения, приступы цианоза • Дыхание поверхностное, часто судорожное • Инспираторная одышка с западением грудины, втяжением межрёберных промежутков и раздуванием крыльев носа • Кожные покровы бледные, прогрессирующий цианоз • Периферические отёки • Аускультация •• Над областью лёгких — ослабление дыхания, разнокалиберные влажные хрипы •• Тоны сердца приглушены, систолический шум.
Диагностика • Лабораторные исследования •• Амниотическая жидкость (отошедшие околоплодные воды или амниоцентез) ••• Соотношение лецитин/сфингомиелин (фосфолипиды, входящие в состав сурфактанта). Их соотношение в амниотической жидкости косвенно характеризует количество внутриальвеолярного сурфактанта и степень зрелости лёгких. Соотношение 2:1 и выше — признак функциональной зрелости лёгких ••• Отсутствие фосфатидилглицерола (фосфатидная кислота, её присутствие в околоплодной жидкости свидетельствует о зрелости лёгких плода в III триместр беременности) •• Признаки респираторного, а также метаболического ацидоза, гипоксемия, гиперкапния • Рентгенологическое исследование органов грудной клетки — ретикулогранулярный рисунок паренхимы (точечные участки просветления чередуются с точечными участками затенения — картина «толчёного стекла») в сочетании с ателектазами различной распространённости.
Дифференциальная диагностика • Стеноз лёгочной артерии • Транспозиция магистральных сосудов • Тетрада Фалло • Диафрагмальная грыжа • Пневмоторакс • Сепсис • Пневмония, вызванная стрептококками группы В • Аспирационная мекониальная пневмония • Транзиторное тахипноэ новорождённых • Ателектаз лёгких • Киста лёгких • Внутричерепное кровоизлияние.
ЛЕЧЕНИЕ
Режим стационарный, палата интенсивной терапии.
Тактика ведения • Интратрахеальное введение сурфактанта • Помещение пациента в кислородную палатку с регулируемыми температурным режимом и влажностью • Самостоятельное дыхание с постоянным положительным давлением (СДППД) показано при наличии у ребёнка самостоятельных дыхательных движений. Кислородно-воздушную смесь подают под давлением 5–7 мм рт.ст. через носовые канюли, назофарингеальную или эндотрахеальную трубку • ИВЛ — показана при апноэ, неэффективности СДППД. Осуществляют через эндотрахеальную трубку • Тщательное наблюдение за состоянием дыхательной системы и ССС, по показаниям — сердечные средства • Ощелачивающая терапия 4–5% р-ром натрия гидрокарбоната и трисбуфером • Парентеральное введение жидкости из расчета 65 мл/кг в первый день и 100 мл/кг на 2–3-й день • Антибиотики при подозрении на инфицирование • Контроль paО2 и paСО2 (чрескожные методы определения) • Пульсовая оксиметрия • Питание через зонд при необходимости • Экстракорпоральную мембранную оксигенацию проводят при неэффективности всех предыдущих мероприятий (противопоказана детям с массой тела менее 2 кг).
Лекарственная терапия
• Сурфактанты •• Профилактическое введение — сразу после рождения при наличии факторов риска, затем повторно 2 раза через каждые 12 ч •• Терапевтическое введение — при появлении признаков или симптомов СРДН, затем повторно через 12 ч •• Колфосцерила пальмитат 5 мл/кг вводят шприцем в эндотрахеальную трубку через боковое отверстие в специальном адаптере без прерывания ИВЛ.
• Аминофиллин в/в — 8 мг/кг, затем по 1,5 мг/кг каждые 8 ч (для стимуляции дыхания и предупреждения приступов апноэ и брадикардии после удаления эндотрахеальной трубки).
• Глюкоза в/в — 10% р-р 5 мл/кг в течение 10 мин сразу после рождения, затем инфузия со скоростью 4–8 мг/кг/мин (быстрое прекращение инфузии может привести к гипогликемии).
Осложнения • Кровоизлияния в желудочки мозга • Напряжённый пневмоторакс • Ретинопатия недоношенных • Апноэ недоношенных.
Течение и прогноз • Течение острое, вероятность летального исхода максимальна при низкой массе тела • Смертность — 45–50% пациентов в первые 2 сут, с каждым днём шансы выживания возрастают • Благоприятный прогноз при гестационном возрасте не менее 28 нед и надлежащем уходе.
Сопутствующая патология • Открытый артериальный проток • Открытое овальное отверстие.
Беременность: СД у беременной увеличивает вероятность СРДН.
Профилактика • Профилактика преждевременных родов • В случае наличия признаков незрелости лёгких плода (при амниоцентезе) необходимо назначить бетаметазон не позднее, чем за 24 ч до родов (индуцирует образование сурфактанта).
Сокращения • СРДН — синдром респираторного дистресса новорождённых • СДППД — самостоятельное дыхание с постоянным положительным давлением.
МКБ-10 • P22 Дыхательное расстройство у новорождённого [дистресс]
Код вставки на сайт
Синдром респираторного дистресса новорождённых
Синдром респираторного дистресса новорождённых (СРДН, (синдром дыхательных расстройств) — тяжёлое патологическое состояние, возникающее чаще у недоношенных детей, с ведущим синдромом острой дыхательной недостаточности.
Этиология и патогенез. При ряде состояний (недоношенность, асфиксия при рождении, СД у матери), протекающих на фоне незрелости лёгких и гипоксии, нарушается синтез сурфактанта лёгочной ткани, что приводит к неполному расправлению лёгких и развитию классического симптомокомплекса — прогрессирующего ателектаза, внутрилёгочного шунтирования крови, гипоксемии и цианоза. На внутренней поверхности альвеол, альвеолярных ходов и респираторных бронхиол обнаруживают отложение гиалиноподобного вещества.
Генетические аспекты • Наследственная предрасположенность возникает при наличии лёгочных протеинозов у родителей • Мутации гена, ассоциированного с сурфактантом белка 1 (178630, 10q21–q24, ген SFTP1) — одна из причин развития СРДН.
Патоморфология • Лёгочная ткань пурпурно-красного цвета • Расширение правых отделов сердца • Артериальный проток может быть открыт • Обширные ателектазы • Гиалиновые мембраны.
Клинические проявления • Начальные признаки возникают в первые часы жизни • Слабый крик после рождения, приступы цианоза • Дыхание поверхностное, часто судорожное • Инспираторная одышка с западением грудины, втяжением межрёберных промежутков и раздуванием крыльев носа • Кожные покровы бледные, прогрессирующий цианоз • Периферические отёки • Аускультация •• Над областью лёгких — ослабление дыхания, разнокалиберные влажные хрипы •• Тоны сердца приглушены, систолический шум.
Диагностика • Лабораторные исследования •• Амниотическая жидкость (отошедшие околоплодные воды или амниоцентез) ••• Соотношение лецитин/сфингомиелин (фосфолипиды, входящие в состав сурфактанта). Их соотношение в амниотической жидкости косвенно характеризует количество внутриальвеолярного сурфактанта и степень зрелости лёгких. Соотношение 2:1 и выше — признак функциональной зрелости лёгких ••• Отсутствие фосфатидилглицерола (фосфатидная кислота, её присутствие в околоплодной жидкости свидетельствует о зрелости лёгких плода в III триместр беременности) •• Признаки респираторного, а также метаболического ацидоза, гипоксемия, гиперкапния • Рентгенологическое исследование органов грудной клетки — ретикулогранулярный рисунок паренхимы (точечные участки просветления чередуются с точечными участками затенения — картина «толчёного стекла») в сочетании с ателектазами различной распространённости.
Дифференциальная диагностика • Стеноз лёгочной артерии • Транспозиция магистральных сосудов • Тетрада Фалло • Диафрагмальная грыжа • Пневмоторакс • Сепсис • Пневмония, вызванная стрептококками группы В • Аспирационная мекониальная пневмония • Транзиторное тахипноэ новорождённых • Ателектаз лёгких • Киста лёгких • Внутричерепное кровоизлияние.
ЛЕЧЕНИЕ
Режим стационарный, палата интенсивной терапии.
Тактика ведения • Интратрахеальное введение сурфактанта • Помещение пациента в кислородную палатку с регулируемыми температурным режимом и влажностью • Самостоятельное дыхание с постоянным положительным давлением (СДППД) показано при наличии у ребёнка самостоятельных дыхательных движений. Кислородно-воздушную смесь подают под давлением 5–7 мм рт.ст. через носовые канюли, назофарингеальную или эндотрахеальную трубку • ИВЛ — показана при апноэ, неэффективности СДППД. Осуществляют через эндотрахеальную трубку • Тщательное наблюдение за состоянием дыхательной системы и ССС, по показаниям — сердечные средства • Ощелачивающая терапия 4–5% р-ром натрия гидрокарбоната и трисбуфером • Парентеральное введение жидкости из расчета 65 мл/кг в первый день и 100 мл/кг на 2–3-й день • Антибиотики при подозрении на инфицирование • Контроль paО2 и paСО2 (чрескожные методы определения) • Пульсовая оксиметрия • Питание через зонд при необходимости • Экстракорпоральную мембранную оксигенацию проводят при неэффективности всех предыдущих мероприятий (противопоказана детям с массой тела менее 2 кг).
Лекарственная терапия
• Сурфактанты •• Профилактическое введение — сразу после рождения при наличии факторов риска, затем повторно 2 раза через каждые 12 ч •• Терапевтическое введение — при появлении признаков или симптомов СРДН, затем повторно через 12 ч •• Колфосцерила пальмитат 5 мл/кг вводят шприцем в эндотрахеальную трубку через боковое отверстие в специальном адаптере без прерывания ИВЛ.
• Аминофиллин в/в — 8 мг/кг, затем по 1,5 мг/кг каждые 8 ч (для стимуляции дыхания и предупреждения приступов апноэ и брадикардии после удаления эндотрахеальной трубки).
• Глюкоза в/в — 10% р-р 5 мл/кг в течение 10 мин сразу после рождения, затем инфузия со скоростью 4–8 мг/кг/мин (быстрое прекращение инфузии может привести к гипогликемии).
Осложнения • Кровоизлияния в желудочки мозга • Напряжённый пневмоторакс • Ретинопатия недоношенных • Апноэ недоношенных.
Течение и прогноз • Течение острое, вероятность летального исхода максимальна при низкой массе тела • Смертность — 45–50% пациентов в первые 2 сут, с каждым днём шансы выживания возрастают • Благоприятный прогноз при гестационном возрасте не менее 28 нед и надлежащем уходе.
Сопутствующая патология • Открытый артериальный проток • Открытое овальное отверстие.
Беременность: СД у беременной увеличивает вероятность СРДН.
Профилактика • Профилактика преждевременных родов • В случае наличия признаков незрелости лёгких плода (при амниоцентезе) необходимо назначить бетаметазон не позднее, чем за 24 ч до родов (индуцирует образование сурфактанта).
Сокращения • СРДН — синдром респираторного дистресса новорождённых • СДППД — самостоятельное дыхание с постоянным положительным давлением.
МКБ-10 • P22 Дыхательное расстройство у новорождённого [дистресс]
Может ли УЗИ определить зрелость легких плода?
ПРО ОТНОСИТЕЛЬНЫЕ И ТОЧНЫЕ МЕТОДЫ ОЦЕНКИ РАЗВИТИЯ ЛЕГКИХ ПЛОДА
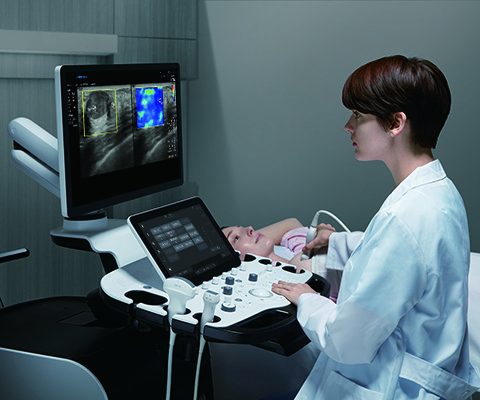
Перинатальная УЗ диагностика бесспорно является необходимым для наблюдения беременности, для уверенности в ее нормальном течении и помощи при необходимости. Каждая будущая мама мечтает, чтобы ребенок родился здоровым.
«Зрелые ли легкие у плода?» — вопрос, который можно услышать от женщин.
Действительно, зрелость легких плода имеет важное значение для внеутробного выживания ребенка. И на сегодняшний день нет единого сонографического стандартизированного исследования этого критерия. Именно для оценки развития легких плода все методы УЗ исследования являются относительными, а не точными. Точные данные дает другой метод диагностики. Рассмотрим эти особенности подробно.
Дыхательные движения незначительной амплитуды у плода, как тренировка мышц, начинаются до рождения. Легкие заполнены жидкостью и еще не функционируют, но готовятся к этому, накапливая сурфактант. Количество сурфактанта в альвеолярной жидкости возрастает в последние недели перед родами. И при нормальной физиологической беременности количество сурфактанта в легких плода в достаточном количестве накапливается до 36 недели. Это означает, что его хватит для самостоятельного дыхания ребенка после рождения. Для детей рожденных раньше срока проводится лечение глюкокортикостероидами для стимулирования выработки сурфактанта.
С помощью УЗИ можно относительно оценить количество производимого в легких плода сурфактанта. Ультразвуковые волны не могут точно определить его количество. К относительным методов оценки относятся:
Именно по последнему методу врачи часто проставляют степень зрелости легких плода по шкале 0, 1, 2. Но, все же, это относительные показатели.
Точное определение дородовой зрелости легких возможно только с помощью анализа амниотической жидкости окружающей плод. В ней определяют соотношение лецитина и сфингомиелина (L/S соотношение). И этот метод используется редко, так как требует определенных навыков.
Для женщин с осложненной беременностью для профилактики назначают дексаметазон. Это помогает избежать респираторного дистресс синдрома (РДС) у новорожденных детей и поможет для многих из них дышать самостоятельно сразу после рождения.
Как вы поняли, каждый из методов ультразвукового исследования дает относительные показатели зрелости легких плода, при этом УЗ диагностика плода является одним из многогранных, важных и информативных методов диагностики для здоровья матери и ребенка.
Подготовлено по материалам Натальи Урсаки — кандидата медицинских наук, врача УЗИ, пренатолога.
Запись к Наталье Олеговны на УЗ скрининг беременности по контактам корпуса 1 ЛДЦ «Мед-Атлант» или через форму записи на сайте.
Ультразвуковая биометрия легких плода
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Введение
В последние годы существенную помощь в оценке состояния новорожденного стали оказывать результаты ультразвукового об следования в различные сроки беременности и непосредственно перед родами. Применение эхографии позволило в подавляющем большинстве случаев своевременно диагностировать различные врожденные пороки развития плода, определить их прогностическую значимость и выбрать оптимальную тактику ведения беременности, родов и периода новорожденности.
Только в единичных исследованиях авторы [12] определяли поперечный диаметр, длину и окружность грудной клетки и легко го, устанавливали цифровые взаимоотношения этих величин и проводили сравнение с данными патологоанатомического вскрытия умерших новорожденных. Представленные в статье данные не содержат зависимости цифровых параметров легких плода от срока беременности. Это существенно снижает практическую ценность статьи. Более детально исследованы легкие плода [13]: проведена ультразвуковая биометрия основных пара метров плода, а также установлены их соотношения с длиной и поперечником легких. Однако переднезадний размер легких не определен и не вычислен их объем. Имеются также сообщения [14] о возможности использования трехмерных датчиков для определения объема легких плода, но данная работа является поисковой, и ее результаты пока не находят широкого применения.
Цель исследования
Учитывая отсутствие в доступной литературе нормальных биометрических параметров легких плода, авторами предлагаемой статьи проведено исследование, цель которого состояла в разработке методики измерения легких у плода, изучении характера их роста и особенностей внутриутробных дыхательных движений в различные сроки беременности.
Материалы и методы
Проведено 462 ультразвуковых исследования (УЗИ) на 13-40-й неделе беременности. В исследование включены только соматически здоровые беременные, у которых на момент исследования клинический срок гестации совпадал с данными фетометрических измерений. Во всех наблюдениях течение беременности было благоприятным, роды завершились в срок рождением живых, доношенных и здоровых детей.
Обязательным условием, предъявляемым к плодам, включенным в настоящее исследование, являлись благоприятные условия визуализации органов и систем. При этом особое внимание уделялось качеству визуальной оценки и возможностям проведения биометрии обоих легких плода. Стандартная ультразвуковая биометрия включала измерение бипариетального (БПР), лобно-затылочного (ЛЗР) размеров головы плода, среднего поперечного диаметра грудной клетки (ДГ), среднего поперечного диаметра живота (ДЖ), длины бедренной кости (ДБ), длины плечевой кости (ДП) и среднего диаметра сердца (ДС). Во всех наблюдениях биометрические пара метры находились в диапазоне допустимых колебаний и не выходили за 5 и 95 персентилей. Измерения осуществляли в миллиметрах (мм).
Поперечник (ширину) легкого определяли при поперечном сканировании дистальных отделов грудной клетки. При этом зона сканирования проходила практически над диафрагмой. Точки отсчета ширины легкого располагались между его наиболее удаленным латеральным краем и зоной примыкания к сердцу слева или справа. Переднезадний размер определяли по наиболее удаленным точкам легкого в зоне его примыкания к диафрагме (рис. 1 б).
Пренатальная оценка зрелости легких плода на 3D УЗИ
АВТОРЫ: Sha-Sha Wang, Xue-Ye Tian, Hong-Wei Yan, Ting Yuan, Xiao-Ye Zheng, Zhen Han
Введение
Идентификация фосфолипидов в амниотической жидкости, включая фосфатидилглицерол, фосфатидилэтаноламин и соотношение лецитин/сфингомиелин (L/S соотношение), является основным методом определения дородовой зрелости легких, который широко применяется в медицинской практике.
С 1980-х годов многие исследовали использование ультразвука для контроля зрелости легких плода. Исследование эхогенности легких плода, дыхательноподобных движений плода, допплеровского спектра, связанного с назальным потоком жидкости при дыхательноподобных движениях плода (BRNFF) и данные объема легких связаны с анализом зрелости легких плода, однако до сих пор нет единого набора сонографических критериев.
В Китае для ультразвукового исследования развития легких плода нет нормативного диапазона показателей, как определения объема легких, например. Таким образом, данное исследование было проведено (I) для оценки возможности и точности ультразвуковых показателей оценки зрелости легких плода; (II) установления границ нормы объема легких плода и сравнения эхогенности легких к эхогенности печени плода (FLLIR) в китайской популяции.
МЕТОДЫ
Пациенты
Проведено проспективное исследование у женщин с одноплодной беременностью. Данное исследование было одобрено Комитетом по этике Сиань Цзяо-Tong University, провинция Шаньси, Китай. В целом 1188 беременных женщин (с гестационным сроком 20 недель) были отобраны в отделении акушерства и гинекологии в больнице Сиань Цзяо-Tong University, в период с июня 2008 года по июнь 2011 года. У женщин с регулярным менструальным циклом срок гестации определяли от первого дня последней менструации, а у женщин с нерегулярным менструальным циклом, гестационный возраст определяли на УЗИ данными измерения копчико-теменного размера (КТР) плода на 8-12 неделе беременности. Критерии включения беременных были (I) один плод; (II) индекс массы тела беременной в пределах 19.8-26.0; (III) отсутствие в анамнезе хронической артериальной гипертензии; и (IV) отсутствие в анамнезе сахарного диабета (тип I или тип II) до беременности. Критерии исключения: (I) пороки развития плода, (II) самопроизвольный аборт, (III) внутриутробная гибель плода, (IV) инфекция в амниотической жидкости, и (V) уменьшенное количество амниотической жидкости.
Ультразвуковое исследование и клинические параметры
УЗИ проводили на аппарате Philips HDI-4000, оборудованном конвексным датчиком частотой 3,5 МГц. Рассчитывали допплеровский спектр, связанный с назальным потоком жидкости во время дыхательных движений плода, объем легких плода, параметры тока крови в легочной артерии, а также эхогенность легких. Амниотическая жидкость была получена от беременных путем амниоцентеза, или во время родов. Измерение фосфоглицеридов в амниотической жидкости проводили с помощью тонкослойной хроматографии.
Расчет соотношения эхогенности легких к эхогенности печени плода (FLLIR)
Проводили исследования в положении плода на спине, датчик был размещен параллельно позвоночнику плода таким образом, что легкие плода и печень были на той же глубине. Удовлетворительные изображения были сохранены (полученные на одинаковом усилении (50 дБ). Все изображения были зафиксированы в конце вдоха беременной и в состоянии покоя плода.
Оценка эхогенности проводилась гистограммой Adobe Photoshop (2003 Adobe Systems, 8.0.1 версия). Для сравнения использовался фиксированного размера квадратный образец (0,5 см х 0,5 см, 24 пикселей × 24 пикселей) печени и легких на той же глубине, избегая при этом больших кровеносных сосудов. Программное обеспечение автоматически обеспечивает гистограмму зоны отбора проб.
Средние серые значения легких плода и печени регистрировали для расчета соотношения интенсивности легких к печени плода. Среднее из трех измерений, полученных на разной глубине, регистрировали как конечный результат.
Объем легких
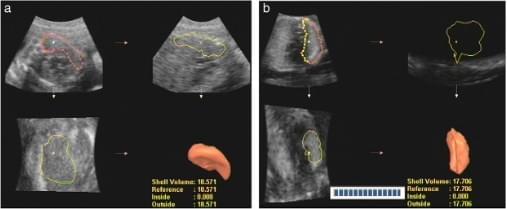
Объем легких плода в состоянии покоя измеряли с помощью виртуального компьютерного анализа (VOCAL) на 3-D УЗИ. Метод был использован для получения последовательных шести секций каждого легкого вокруг неподвижной оси, от верхушки к основанию на 30° от предыдущего среза. Контур каждого легкого автоматически рисуется в шести плоскостях, чтобы получить измерения объема 3-D. Стартовой плоскостью вращения для каждого легкого был самый большой переднезадний диаметр. После автоматического расчета предел каждой плоскости был рассмотрен и скорректирован вручную. Программное обеспечение может автоматически восстановить 3D изображения и рассчитать объем (Рис.1). Рассчитали объем левого и правого легкого и определили общий объем легких путем получения суммы объемов обоих легких. Результаты были сохранены в базе данных ультразвукового аппарата.
Рис.1. Измерение объема легких у плода с гестационным сроком 29 недель и 3 дня с помощью функции VOCAL 3-D УЗИ. (А) правое легкое; (B) левое легкое.
Гемодинамические показатели легочной артерии
Измерение кровотока в легочной артерии было проведено в поперечном срезе грудной клетки плода на уровне среза четырех камер сердца, с использованием цветного и спектрального допплера. Гемодинамические параметры легочной артерии, такие как максимальная скорость (Vmax), пульсационный индекс (ПИ), индекс резистентности (ИР), и S/D соотношение были измерены в период полного покоя плода. Контрольный объем установлен следующими параметрами: ширина 2 или концентрация фосфатидилглицерола была > 1 ммоль/л, легкие плода были определены, как зрелые.
Статистический анализ
Сорок одну беременную исключили из исследования вследствие несоответствия критериям, остальные тысячу сто сорок семь пациентов (возрастной диапазон 18-44 лет, средний возраст 28.19 ± 4.05) включилиы в исследование. Все участники дали письменное информированное согласие до начала исследования, в соответствии с требованиями Комитета Исследования Человека. Во время проведения исследования у 125 беременных были обнаружены осложнения беременности, поэтому они также были исключены. И, наконец, 1022 беременные были нами проанализированы.
Расчет соотношения эхогенности легких к эхогенности печени плода, срок гестации и зрелость легких
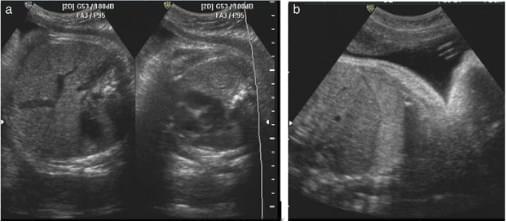
Соотношение эхогенности легких к эхогенности печени было легче получить, когда плод находился в положении на спине, потому что было меньше помех от теней ребер и позвонков. Были отобраны поперечные срезы грудной клетки и брюшной полости для расчета FLLIR (рис. 2).
Рис.2. (а) Поперечный срез, демонстрирующий эхогенность легких и печени плода на сроке гестации 32 недели и 2 дня. (B) Эхогенность легких была выше, чем в печени у плода гестационным сроком 38 недель и 5 дней.
На ранних сроках беременности эхогенность легких ниже, чем в печени плода. В 31-33 недели эхогенность легких становится более интенсивной, в то время как эхогенность печени плода претерпевает незначительные изменения (Таб.1). FLLIR стал > 1.1 после 34 недели беременности.
Обсуждение
На сегодняшний день нет единого сонографического стандарта исследования легких плода. В нашем исследовании мы использовали 3-D индексы для определения маркеров зрелости легких плода у женщин с нормальной беременностью и сравнили уровень фосфоглицеридов в амниотической жидкости. Мы обнаружили, что FLLIR > 1.1, FLV > 50 мл и регулярные дыхательные движения после 34 недель беременности коррелирует со зрелостью легких плода.
Поскольку легкие и печень плода находятся в одинаковых средах и эхогенность печени является относительно стабильной, FLLIR может служить полезным показателем зрелости легких. Для того чтобы свести к минимуму ошибки в эксперименте, мы рассматривали эхограммы легких и печени плода на той же глубине три раза, и определили средние данные в качестве конечного результата.