лептин где вырабатывается и за что отвечает
Лептин где вырабатывается и за что отвечает
Лептин – это гормон жировой ткани, обеспечивающий регуляцию энергетических, нейроэндокринных и метаболических процессов организма. Он служит клинико-лабораторным маркером риска сахарного диабета 2-го типа и ишемической болезни сердца, а также применяется для диагностики ожирения и вторичной аменореи.
Гормон жировой ткани, гормон голода.
Leptin, adipo-stat signal.
Иммуноферментный анализ (ИФА).
Нг/мл (нанограмм на миллилитр).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Лептин получил название от греческого слова leptos, что означает «худой, тонкий». Этот гормон вырабатывается клетками жировой ткани и регулирует энергетические, нейроэндокринные и метаболические процессы организма.
Функция лептина осуществляется через его взаимодействие с рецепторами ObRs, находящимися в головном мозгу, а также в некоторых периферических тканях. Существует несколько изоформ ObRs: ObRa и ObRc, необходимые для транспорта молекулы лептина через гематоэнцефалический барьер (ГЭБ), и ObRb, обеспечивающий основные регуляторные эффекты в гипоталамусе. В результате взаимодействия с ObRb лептин стимулирует синтез анорексигенных (подавляющих аппетит) медиаторов (в частности, проопиомеланокортина) и тормозит синтез орексигенных (стимулирующих аппетит) медиаторов (в частности, нейропептида Y). Кроме того, лептин воздействует на мезолимбическую систему, формирующую мотивацию к принятию пищи и чувство удовлетворения от еды, и на нейроны центров продолговатого мозга, также формирующие чувство насыщения. По сути, лептин является уникальным «датчиком», координирующим многие нейроэндокринные процессы человека в соответствии с его энергетическими запасами. В норме повышение концентрации лептина происходит после обильной еды и сопровождается снижением аппетита.
Наследственный дефицит данного гормона возникает из-за некоторых мутаций в его гене, приводящих к укорачиванию молекулы лептина и нарушению ее структуры. При отсутствии подавляющего влияния лептина на аппетит люди испытывают постоянное чувство голода и набирают вес. Пациенты с этим редким врождённым дефектом характеризуются выраженным ожирением, развивающимся уже в детском возрасте, гипотиреозом, гипогонадизмом и задержкой полового развития. Несмотря на то что врождённый дефицит лептина встречается редко (у 5-6 % страдающих ожирением), его следует учитывать при диагностике ожирения, так как применение экзогенного лептина у таких пациентов значительно снижает вес и нормализует уровень половых гормонов.
Однако у подавляющего большинства пациентов с ожирением имеется переизбыток лептина на фоне невосприимчивости к его действию. При этом отсутствует контроль гипоталамуса и других структур головного мозга за частотой и количеством принятия пищи. Пациент испытывает голод даже при наличии адекватных его физиологическим затратам запасов энергии. Считается, что невосприимчивость к лептину развивается в результате структурных и функциональных дефектов на уровне рецептора ObRb, избыточной продукции ингибиторов лептина, а также при нарушении транспорта молекулы лептина через ГЭБ.
Около 1 миллиарда людей во всем мире страдает ожирением. С эволюционной точки зрения способность запасать энергию в виде жира при условии избытка пищи была необходима для выживания человека как вида, поэтому естественный отбор был направлен на закрепление мутаций, обеспечивающих накопление жировой ткани. В современном обществе, изобилующем продуктами питания, эти сложившиеся адаптационные механизмы более не являются преимуществом, однако по-прежнему сильны. Моногенные варианты (мутации одного гена) наблюдаются у малой доли пациентов с ожирением, в подавляющем же большинстве случаев ожирение – полигенное (обусловленное отклонениями в нескольких генах) и полифакториальное (вызванное сочетанием внутренних и внешних факторов) заболевание. Большое значение в развитии ожирения имеют малоподвижный образ жизни, курение и особенности рациона.
Ожирение – ведущий фактор риска развития сахарного диабета. Избыток жировой ткани провоцирует усиленную продукцию инсулина и гиперинсулинемию, что, в свою очередь, приводит к уменьшению количества рецепторов инсулина в периферических тканях и инсулинорезистентности. В норме лептин независимо от эффекта инсулина усиливает утилизацию глюкозы периферическими тканями и окисление жирных кислот в печени, увеличивает чувствительность периферических тканей к инсулину и снижает его секрецию бета-клетками поджелудочной железы. В связи с этим при наличии резистентности к лептину часто развивается и инсулинорезистентность, нарушается утилизация глюкозы и возрастает риск развития сахарного диабета 2-го типа, поэтому измерение концентрации лептина может быть использовано для оценки риска развития этого заболевания.
Ишемическая болезнь сердца (ИБС) также связана с ожирением. Высокая концентрация лептина стимулирует оксидативный стресс (окислительное повреждение клеток) в эндотелиоцитах, разрастание гладкомышечных клеток и отложение солей кальция в сосудистой стенке. Эти изменения приводят к нарушению реакции сосуда в ответ на дилатацинные стимулы (например, воздействие алкоголя, снижение артериального давления) и способствуют развитию атеросклероза. Избыток лептина связан с повышением концентрации протромбогенных факторов, таких как фибриноген, фактор VII и фактор фон Виллебранда. Структурные особенности лептина позволяют отнести его к семейству провоспалительных цитокинов – белков, поддерживающих воспаление. Например, лептин участвует в созревании Т-лимфоцитов в тимусе, поддержании пула NK-клеток, хемотаксисе и активации нейтрофилов. На гуморальном уровне лептин стимулирует продукцию фактора некроза опухолей α (TNF-α) и ИЛ-6. Эти иммунологические нарушения, обусловленные повышенным уровнем лептина и некоторых других цитокинов, позволяют рассматривать ожирение как хроническое воспалительное заболевание. Повышенный уровень лептина является предиктором развития инфаркта миокарда, нестабильной стенокардии или внезапной сердечной смерти. Таким образом, повышение концентрации лептина может рассматриваться как клинико-лабораторный маркер риска ИБС.
Концентрация лептина прямо пропорциональна массе жировой ткани и отражает энергетические запасы организма. Истощение энергетических запасов (в результате голодания, интенсивных физических нагрузок) сопровождается понижением концентрации лептина, что провоцирует характерные нейроэндокринные изменения: снижение уровня тироксина (понижение температуры тела и метаболизма, чувство холода, замедление реакций), повышение уровня гормонов стресса соматотропина, адреналина и кортизола (усиление липолиза и глюконеогенеза в печени, гипертриглицеридемия и гипергликемия) и снижение уровня половых гормонов (характерный признак истощения – вторичная аменорея и ановуляция, а также остеопороз).
Гипоталамическая аменорея встречается у 3-8,5 % пациенток в возрасте 13-44 лет. Она сопровождается подавленной ритмической продукцией гонадотропин-рилизинг-гормона (Гн-РГ) гипоталамуса, что приводит к дефициту фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормона гипофиза, снижению уровня половых гормонов и ановуляции. Одной из причин гипоталамической аменореи является дефицит лептина. Применение экзогенного лептина у таких пациенток нормализует синтез ГнРГ, ФСГ, ЛГ и половых гормонов. Поэтому измерение уровня лептина может быть использовано для выявления причины вторичной аменореи, а также для определения тактики лечения женского бесплодия.
Для чего используется исследование?
Когда назначается исследование?
Что означают результаты?
Причины повышения уровня лептина:
Причины понижения уровня лептина:
Что может влиять на результат?
Кто назначает исследование?
Эндокринолог, диетолог, кардиолог, гинеколог-эндокринолог, врач-генетик.
Наш друг лептин
За что отвечает лептин?
Функции лептина
Исследования показали, что уровни лептина у пациентов с депрессией выше, чем в контрольных группах. В связи с серьезными побочными эффектами и длительным периодом времени для начала действия традиционных антидепрессантов последние исследования были сосредоточены на антидепрессивных эффектах нейропептидов и таких гормонов как лептин и грелин. Фармакологические исследования показали, что введение лептина в гиппокамп может оказывать эффект, подобный антидепрессанту, в то время как при введении лептина в гипоталамус положительного эффекта не обнаружено.
Лептин и нейтронсмиссия
Сообщалось, что введение лептина снижает плотность сайтов связывания селективного ингибитора транспортера 5-HT пароксетина. Исследователи предполагают, что лептин может функционально стимулировать транспортер 5-HT и увеличивать экспрессию на уровнях белка.
Нейтротрофические рецепторы лептина
Лептин может активировать BDNF-экспрессирующие нейроны гипоталамуса посредством активации нейронных цепей, которые стимулируют синтез BDNF в дендритах ( Liao et al., 2012 ). Напомню читателю моего Блога, что BDNF играет ключевую роль в ЦНС, связывая его рецептор. Введение лептина в задний мозг значительно увеличивает уровень BDNF в дорсальном комплексе. Несколько экспериментов in vivo и in vitro подтвердили, что лептин сам по себе может оказывать нейропротекторное и нейротрофическое действие за счет стимулирования передачи сигналов BDNF и уменьшения апоптоза и потери нейронов. Это может объяснить, почему лептин может улучшить когнитивные функции и стабилизировать поведение больных. Существуют неподтвержденные в эксперименте наблюдения, показывающие, что голодание и ограничение калорий, способствуя снижению уровня лептина, обладают антидепрессивным эффектом.
Влияние лептина на ось стресса
Метаболизм
Нейродегенеративные процессы
Исследователи продемонстрировали, что лептин вызывает нейротрофические и нейропротективные эффекты у пациентов с болезнью Альцгеймера. При этом уровень амилоида-β снижается как в экстрактах мозга, так и в сыворотке трансгенных мышей после лечения лептином. Кроме того, лептин влияет на рост нейритов в первичных культурах нейронов и может спасти нейрит от токсичности амилоида-β. Лептин восстанавливает дефицит пространственной памяти, вызванный амилоидом-β, и долгосрочное потенцирование in vivo в поздней фазе гиппокампа. Хроническая интрацеребровентрикулярная инъекция лептина вызывает улучшение пространственной памяти
Уровень лептина в крови
Уровень лептина в плазме крови колеблется в зависимости от времени суток, ночью на 20–30% ниже, чем днем. При появлении голода в ночное время это колебание нарушено. Доказано, что снижение массы тела на 10% уменьшает лептин на 53%. В то же прибавка веса на 10% многократно увеличивает уровень лептина. Всего 1 день значительного переедания поднимает показатель на 40%. Также лептин стимулирует синтез половых гормонов и щитовидной железы, СТГ (соматотропного гормона ).
Рекомбинантный лептин
Миалепта
Еврокомиссия одобрила препарат Миалепта (Myalepta) компании Aegerion Pharmaceuticals, предназначенный для терапии редкого заболевания липодистрофии в качестве вспомогательного средства для заместительной терапии при осложнениях, связанных с дефицитом лептина. На сегодняшний день это лекарственное средство первое и единственное, зарегистрированное для борьбы с дефицитом лептина, которое направлено на первопричину заболевания. Липодистрофия является редким заболеванием, требующим высокоспециализированного лечения. До одобрения препарата Миалепта пациенты могли только принимать инсулин для борьбы с осложнениями заболевания и изменить образ жизни. Если липодистрофию не лечить, то она может привести к серьезному поражению органов.
Ожирение и гормон лептин
Принято считать, что толстые люди — безвольные, ленивые, слабые, неспособные взять себя в руки. Хотя причины ожирения сложны и разнообразны, современные исследования показывают, что дело не столько в силе воле, сколько в биохимии организма, и особое внимание уделяется гормону лептину, который был открыт совсем недавно (1).
Что такое лептин?
Лептин — гормон, который вырабатывается жировыми клетками. Чем больше жира в теле, тем больше лептина производится (3, 4). С его помощью жировые клетки «общаются» с мозгом.
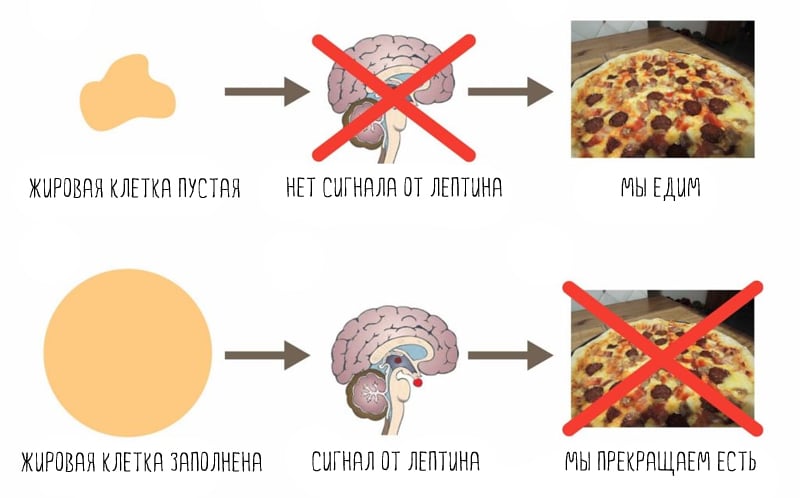
Лептин сообщает о том, сколько в организме запасено энергии. Когда его много, мозг понимает, что в организме достаточно жира (энергии). Как результат, нет сильного голода, а скорость обмена веществ на хорошем уровне (5).
Таким образом, главная роль лептина — долгосрочное управление энергетическим балансом (6). Он помогает поддерживать организм во время голода, давая сигнал мозгу включать аппетит и снижать метаболизм. Он же защищает от переедания, «выключая» голод (7).
Резистентность к лептину
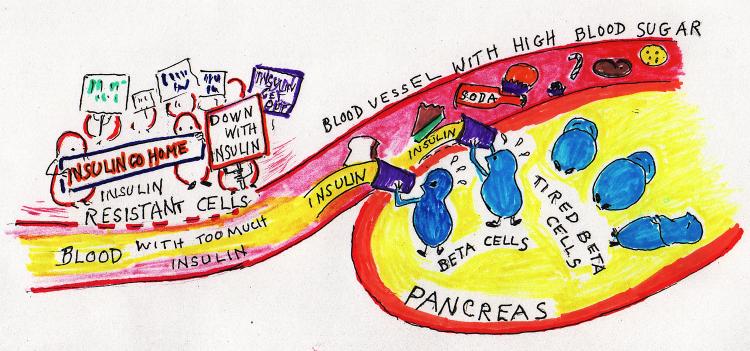
У людей с ожирением высокий уровень лептина (10) По логике, мозг должен знать, что энергии запасено в организме более чем достаточно, но иногда чувствительность мозга к лептину нарушена. Это состояние называется лептин-резистентностью и в настоящее время считается основной биологической причиной ожирения (12).
Когда мозга теряет чувствительность к лептину, нарушается управление энергетическим балансом. Жировых запасов в теле много, лептина производится тоже много, но мозг его не видит. Лептин-резистентность – это когда ваше тело думает, что вы голодаете (хотя это не так) и настраивает пищевое поведение и обмен веществ соответственно (11, 13, 14, 15):
Человек ест слишком много, двигается мало, становится вялым, обмен веществ его и активность щитовидной железы снижены, лишний вес вплоть до ожирения — результат.
Это замкнутый круг:
Что вызывает лептин-резистентность?
1. Воспалительные процессы
Воспаление в организме может протекать бессимптомно. У людей с ожирением подобные процессы могут происходить в подкожно-жировой клетчатке при сильном переполнении жировых клеток или в кишечнике из-за увлечения «западной» диетой, богатой на рафинированные, переработанные продукты.
К месту воспаления поступают иммунные клетки, называемые макрофагами, и выделяют воспалительные вещества, некоторые из которых мешают работе лептина.
2. Фастфуд
Фастфуд и западная диета с большим количеством переработанных продуктов так же может быть причиной лептин-резистентности. Предполагается, что основной виновник этого — фруктоза, которая широко распространена в виде добавок в продукты питания и как одна из составляющих сахара (31).
3. Хронический стресс
Хронически повышенный стрессовый гормон кортизол снижает чувствительность рецепторов мозга к лептину.
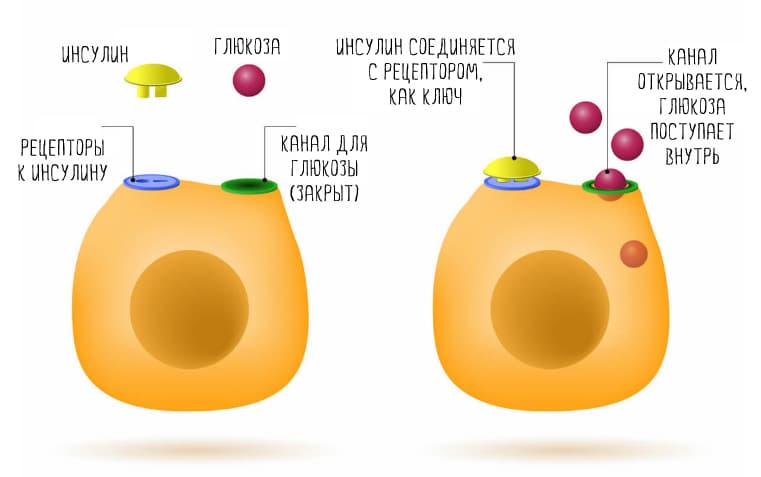
4. Нечувствительность к инсулину
Когда в организм поступает очень много углеводов, выделяется много инсулина, чтобы убрать глюкозу из крови. Если инсулина хронически много, клетки теряют чувствительность к нему. В этих условиях неиспользованная глюкоза превращается в жирные кислоты,что мешает транспорту лептина в мозг (28).
5. Лишний вес и ожирение
Чем больше жира в теле, тем больше производится лептина. Если лептина слишком много, мозг снижает количество рецепторов к нему, и его чувствительность к нему снижается. Так что это порочный круг: б ольше жира = больше лептина = больше резистентность к лептину = больше жира в организме.
6. Генетика
Иногда встречается генетически нарушенная чувствительность рецепторов мозга к лептину или мутации в самой структуре лептина, которые не дает мозгу его увидеть. Считается, что до 20% страдающих ожирением, имеют эти проблемы.
Что делать?
Лучший способ узнать, есть ли у вас резистентность к лептину — узнать свой процент жира. Если у вас высокий процент жира, который говорит об ожирении, если у вас много лишнего веса особенно в области живота, есть вероятность.
Так же для первичной диагностики ожирения используется индекс массы тела (BMI — body mass index). Рассчитать его можно по формуле:
ИМТ = вес тела в кг : (рост в кв.м.)
Пример: 90 кг : (1,64 х 1.64) = 33.4
Хорошая новость в том, что лептин-резистентность в большинстве случаев обратима. Плохая — в том, что пока нет простого способа сделать это, как и не существует пока лекарства, которое способно улучшить чувствительность к лептину. Пока в арсенале худеющего знакомые всем советы по смене образа жизни — здоровая диета, контроль калорий, силовые тренировки и повышение ежедневной бытовой активности.
Лептин где вырабатывается и за что отвечает
Понимание конкретной биологической роли эффекторных молекул нашего организма имеет не только теоретическую ценность, но и важное практическое значение, заключающееся в возможности их использования в качестве биомаркеров и мишеней для терапевтического воздействия [1–3]. В последнее время, благодаря усовершенствованию молекулярно-генетических технологий, методов белкового анализа, открывается множество различных регуляторных соединений, которые не только меняют наше представление о функционировании органов и тканей, но и создают предпосылки для улучшения лечебно-профилактических стратегий [4, 5]. К числу молекул, имеющих большие перспективы для практического здравоохранения, относится белок лептин.
Целью этой статьи является систематизация существующих данных о биологической роли лептина. В статье нами последовательно будут рассмотрены следующие аспекты: генетика и биология лептина, сигнальный путь и механизм действия лептина, регуляция образования лептина, а также функции лептина в норме и при патологических процессах.
Лептин (в переводе с греч. leptos – тонкий) – гормон пептидной природы, выделяемый адипоцитами. Открытие лептина Y. Zhang с соавт. в 1994 г. вызвало большой интерес в плане дальнейшего изучения гормональной функции жировой ткани [6, 7]. Первоначально открытый лептин также назвали «белок ob» (сокращенно от obese, англ. – страдающий ожирением). Ген, кодирующий образование лептина, также первоначально был назван «геном ob» (сейчас чаще используется термин «ген LEP»), он расположен на хромосоме 7q31.31. С момента открытия лептина сформировалась новая концепция о функционировании жировой ткани, согласно которой она действует как активный эндокринный орган, помимо инертного органа хранения липидов и энергии, как считалось ранее [6–8]. Лептин состоит из 167 аминокислот и вырабатывается преимущественно белой жировой тканью нашего организма. Считается, что общая концентрация лептина, циркулирующего в организме, равна общему количеству жира человека. Первоначальные исследования показали, что лептин может играть определенную роль в контроле избыточного набора жира в нашем организме, но впоследствии стало известно, что большее высвобождение лептина приводит к большему потреблению пищи и накоплению жира. Лептин также вырабатывается плацентой и желудком, но гораздо в меньшем количестве по сравнению с жировой тканью [9, 10]. Лептин, имеющий молекулярную массу 16 кД, действует в головном мозге через нейронные гипоталамические пути и таким образом регулирует энергетический гомеостаз [8]. Исследования показали, что дефицит лептина приводит к ожирению, что объясняет его роль в потреблении пищи, использовании энергии, репродукции, функциях щитовидной железы и иммунитете [11]. Несколько исследований также показали, что лептин вызывает окисление жиров у людей с ожирением [12]. Благодаря широкому разнообразию функций лептина, исследователи предприняли усилия, чтобы продемонстрировать и прояснить его роль с биологической точки зрения.
Генетика и биология лептина
Ген лептина был первоначально обнаружен с помощью метода поиска, ассоциированного с болезнью гена мышей ob/ob, и поэтому его также называют «геном ob». Этот ген экспрессируется в белой жировой ткани, желудке, плаценте и, возможно, в молочной железе. Он относится к семейству цитокинов, так как имеет кристаллическую структуру [6, 13]. Лептин, будучи гормоном, имеет циркадные (суточные) вариации концентрации с повышенным уровнем, обнаруживаемым вечером, и импульсной секрецией в ранние утренние часы. Поскольку он преимущественно продуцируется адипоцитами, его основная роль заключается в регулировании энергетического гомеостаза, который включает в себя потребление пищи, использование энергии и регулирование массы тела. Он также играет другие важные функции, такие как регулирование иммунных и воспалительных реакций, вызывая ангиогенез и заживление ран. Из-за своей роли в энергетическом гомеостазе и регулировании массы тела его также называют «гормоном против ожирения» или «гормоном похудения» [14, 15]. Помимо этого, исследования показали, что лептин играет важную роль в формировании высокого кровяного давления у людей с ожирением [14, 16, 17].
Сигнальный путь и действие лептина
Лептин оказывает свое действие, связываясь с рецептором лептина (LEP-R или OB-R), который у человека кодируется геном LEPR. LEP-R обнаруживается во многих областях мозга и эндотелии мозговых капилляров. LEP-R входит в состав семейства цитокиновых рецепторов гликопротеина 130. После соматической рекомбинации LEP-R были сгенерированы различные изоформы рецептора лептина, из которых LEPEb является наиболее важной и самой длинной изоформой, вызывающей сильный сигнальный путь. Исследования сообщили о мутациях в LEPR, которые вызывают ожирение. После связывания с LEPR лептин осуществляет сигнальный каскад через Янус-киназу (JAK), сигнальный преобразователь и активатор транскрипции (белок STAT). В некоторых исследованиях было показано, что лептин активирует путь STAT3 в гипоталамической области мозга (рис. 1) [18–20].
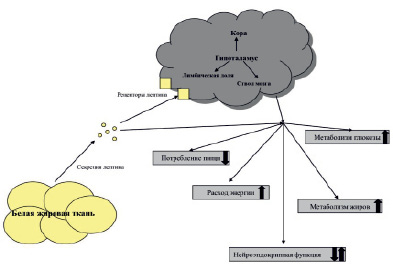
Рис. 1. Эффекты лептина. Примечание. Лептин действует либо напрямую, либо путем активации определенных центров в центральной нервной системе для уменьшения потребления пищи, увеличения расхода энергии, влияния на метаболизм глюкозы и жиров или изменения нейроэндокринной функции
Регуляция образования лептина
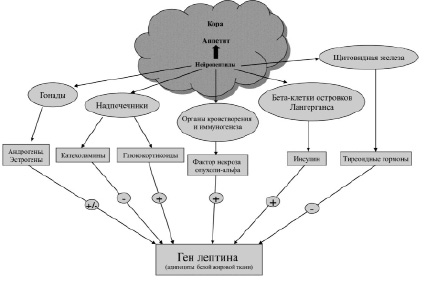
Регуляция образования лептина происходит многими гормонами в организме человека в виде увеличения или уменьшения его синтеза на клеточном уровне. Инсулин увеличивает синтез лептина, в то время как адреналин, норадреналин и дофамин снижают синтез лептина. Помимо этих факторов, фактор некроза опухоли-α также увеличивает секрецию лептина (рис. 2). Глюкоза и жирные кислоты также влияют на экспрессию лептина и, в свою очередь, на его секрецию [21–23].
Рис. 2. Регуляция образования лептина. Примечание. Лептин после высвобождения из адипоцитов связывается с рецепторами лептина в гипоталамусе и изменяет экспрессию нескольких нейропептидов; они, в свою очередь, снижают аппетит, увеличивают расход энергии за счет изменения симпатического и парасимпатического тонуса и изменяют нейроэндокринную функцию. Повышение уровня лептина активирует оси щитовидной железы, гормона роста и гонад и подавляет ось гипофиз – надпочечник. Лептин, действуя прямо или косвенно (изменяя уровни других гормонов и нейропептидов), также влияет на кроветворение и иммунную функцию и улучшает метаболизм глюкозы и жиров. Наконец, измененная продукция и уровни циркуляции гормонов и цитокинов влияют на выработку лептина адипоцитами: + – стимулирующее действия, – – ингибирующее действие
Биологическая роль лептина
Согласно результатам многочисленных клинических и экспериментальных исследований лептин выполняет в организме человека множество важнейших функций, а именно: регуляцию обмена липидов, регуляцию энергетического гомеостаза, регуляцию нейроэндокринных функций, регуляцию обмена углеводов, играет важную роль в развитии новорожденных, детском возрасте и в периоде полового созревания, а также принимает участие в метаболизме сердечно-сосудистой системе, костной ткани и иммунных реакциях [23–25]. Такая многогранная роль лептина делает его весьма ценным и перспективным объектом дальнейших исследований с целью возможностей использования в качестве раннего биомаркера и в качестве лекарственного препарата.
Роль лептина в регуляции энергетического гомеостаза
Лептин играет важную роль в энергетическом гомеостазе, регулируя аппетит. Лептин активирует сложную нейрональную петлю, состоящую из анорексигенных нейронов (т.е. снижающих аппетит), которые высвобождают проопиомеланокортин (POMC), и орексигенных нейронов (т.е. стимулирующих аппетит), которые высвобождают нейропептид Y (NPY), регулирующий потребление пищи. Недавний метаанализ показал, что состояние натощак и диета с ограничением калорий до половины от общей потребности могут значительно снизить уровень лептина. Клинически мутация в гене лептина или его рецепторе приводит к ожирению из-за гиперфагии. Исследования показали, что введение лептина таким пациентам снижает потребление пищи за счет повышения сытости [24–26].
Роль лептина в регуляции нейроэндокринной функции
Уровень лептина падает во время голодания, и это не зависит от жировой массы. Голодание приводит к нейроэндокринным реакциям как у человека, так и у мышей, что включает в себя снижение уровня гормонов, важных для размножения. Это, в свою очередь, уменьшает изменения во время беременности (энергозатратный процесс), снижает уровень гормонов, высвобождаемых из щитовидной железы, что замедляет скорость метаболизма, повышает уровень гормона роста, который может участвовать в перемещении запасов энергии в организме и может замедлять деятельность, связанную с ростом. Но исследование показало, что пациент, у которого имеется дефицит лептина с рождения, может иметь нормальный рост и развитие организма, а также нормальное функционирование надпочечников, в отличие от того, что было замечено в экспериментах у мышей [27, 28].
Роль лептина в регуляции обмена углеводов. Инсулинорезистентность и метаболический синдром
Мутация гена лептина, наблюдаемая у мышей ob/ob и мышей db/db, а также генетический дефицит лептина, наблюдаемый у человека, показали резистентность к инсулину и некоторые особенности метаболического синдрома. Лечение лептином корригировало гиперинсулинемию, гипергликемию до потери веса как у мышей, так и у человека. Но у человека он также снижал уровень триглицеридов, холестерина и липопротеинов низкой плотности (ЛПНП) и повышал уровень липопротеинов высокой плотности (ЛПВП) [29]. Лептин также был вовлечен в воспаление, обнаруженное у тучных женщин, которое может привести к гестационному сахарному диабету (ГСД). Лептин не только контролирует баланс между насыщением и энергией матери, но и вырабатывается плацентой, которая, в свою очередь, поддерживает жизнеспособность плода. Основным источником циркулирующего лептина у матери является его плацентарная продукция, которая мобилизует жир у матери, усугубляя вероятность возникновения ГСД. При ГСД лептин оказывает значительное влияние на плаценту аутокринным/паракринным способом. Это приводит к увеличению размеров плаценты, облегчает перенос плацентарных питательных веществ через глицериновый транспортер и аквапорин-9 и увеличению размеров плода (макросомия). В основном инсулинорезистентность может усугублять течение ГСД и способствовать повышению уровней лептина в плазме крови при ГСД, а дальнейшее воспаление, связанное с ожирением, играет свою собственную роль в развитии инсулинорезистентности. Поэтому для лечения ГСД рассматриваются питательные вещества, обладающие противовоспалительным действием.
Ожирение с инсулинорезистентностью участвует в обострении синдрома поликистозных яичников (СПКЯ), при котором исследования выявили более высокий уровень лептина. Недавнее исследование продемонстрировало индукторный эффект лептина при иммунном дисбалансе, наблюдаемом при СПКЯ, за счет индукции интерферона-γ (INF-γ), который может участвовать в апоптозе гранулезных клеток [30, 31].
Роль лептина в регуляции метаболизма сердечно-сосудистой системы и сердечно-сосудистых заболеваниях (ССЗ)
Роль лептина в развитии и метаболизме ССЗ до конца не изучена. Несколько экспериментальных исследований на животных моделях, таких как диабетические (db/db) и тучные (ob/ob) модели, отчетливо показали благотворную роль лептина в регуляции сердечного метаболизма. При нормальных физиологических условиях сердце использует глюкозу и жир в качестве источника энергии, но предпочтительно глюкозу. В моделях животных с дефицитом лептина или LEP-R нарушается регуляция сердечного метаболизма путем перехода на повышение использования жиров вместо обычного предпочтительного использования глюкозы. Это приводит к повышенному окислению жира, увеличению потребления кислорода миокардом и снижению сердечной деятельности, что в конечном итоге приводит к системным метаболическим нарушениям, таким как инсулинорезистентность, резистентность к лептину и метаболическая дисфункция. Кроме того, повышенные уровни триглицеридов и накопление жира в миокарде на таких животных моделях приводили к липотоксичности, которая, в свою очередь, влияет на сократительную способность сердца [22, 32]. Таким образом, исследования, проведенные на животных моделях, показывают, что лептин может защитить сердце от накопления липидов и липотоксических эффектов, действуя как антилипотоксическое средство.
В различных исследованиях наблюдались противоречивые результаты относительно связи лептина с ишемической болезнью сердца (ИБС) и хронической сердечной недостаточностью (ХСН). Повышенный уровень лептина был связан с риском развития ИБС и ХСН. Однако терапия, снижающая уровень лептина, может способствовать снижению сердечно-сосудистого риска у таких пациентов. Сообщалось, что более высокие уровни лептина предсказывают риск развития инсульта, атеросклеротическое поражение сонных артерий и заболевания периферических артерий (ЗПА). Также сообщалось, что гиперлептинемия ускоряет рост аневризмы брюшной аорты, но для установления четкой связи требуются дальнейшие исследования [22, 33, 34].
Роль лептина у новорожденных
Плацента выделяет лептин в пуповинную кровь, что имеет большое значение для новорожденных. Было установлено, что уровни лептина положительно связаны с общей массой тела и жировой массой новорожденного. Помимо энергетического гомеостаза, лептин регулирует рост, способствует кроветворению и лимфопоэзу в неонатальном периоде. Секреция лептина с молоком также позволяет предположить, что уровень лептина у матери может влиять на рост новорожденных младенцев [35–37].
Роль лептина в детском возрасте и при половом созревании
В детском возрасте и периоде полового созревания лептин посылает сигнал в мозг для накопления жиров, за счет чего в конечном итоге регулирует пубертатные изменения, менструальный цикл и репродукцию. В начале полового созревания увеличение жировой массы тела происходит из-за повышенного уровня лептина у нормальных детей, что, в свою очередь, предполагает, что он вызывает половое созревание у людей. Напротив, лица с мутациями в гене LEPR страдают ожирением, остаются препубертатными и имеют гипогонадотропный гипогонадизм [38–40].
Роль лептина в метаболизме костной ткани и воспалении
Известно, что лептин играет важную роль при ревматических заболеваниях и остеоартрите. Уровень лептина повышен у больных остеоартритом. Большинство исследований выявили катаболическую роль лептина в хрящах. Роль лептина при этих заболеваниях также предполагает, что он действует как провоспалительный фактор на метаболизм хряща. Лептин рассматривается не только как медиатор воспаления при аутоиммунных заболеваниях, но и при других воспалительных заболеваниях [41, 42]. В противоположность этому, хронические воспалительные состояния, вторичные по отношению к метаболическим, аутоиммунным или инфекционным заболеваниям, могут привести к резистентности к лептину, за которой последует развитие ожирения, которое, в свою очередь, потенцирует воспаление [42–44].
Роль лептина в иммунных реакциях
Лептин регулирует как естественные, так и приобретенные иммунные реакции. Что касается врожденного иммунитета, лептин увеличивает силу естественных киллеров (NK) клеток и способствует активации гранулоцитов, макрофагов и дендритных клеток [45–47]. Что касается адаптивного иммунитета, лептин увеличивает размножение новообразованных Т- и В-лимфоцитов, в то же время он уменьшает размножение регуляторных Т-клеток (Т-супрессоров). Таким образом, лептин активирует В-лимфоциты, которые секретируют цитокины для контроля продукции и созревания Т и В-лимфоцитов [48, 49].
Заключение
Таким образом, лептин, или белок ob, является гормоном, который преимущественно продуцируется адипоцитами белой жировой ткани и реагирует с рецептором лептина, который, в свою очередь, инициирует сигнальный каскад по пути JAK-STAT. Передача сигналов лептина активирует выработку различных нейропептидов, таких как проопиомеланокортин и нейропептид Y, что приводит к снижению и увеличению аппетита соответственно. Уровень лептина в крови отражает общее количество запасов энергии в жировой ткани, а это, в свою очередь, направляет центральную нервную систему на регулирование энергетического гомеостаза, нейроэндокринных функций, метаболической регуляции, роста новорожденных, ряда изменений в детском и половом возрасте. Дефицит лептина может быть обусловлен либо мутацией в гене лептина, либо наследственной липоатрофией. Дефицит лептина приводит к нарушениям многих важнейших функций, в частности вызывает репродуктивную недостаточность, ожирение, инсулинорезистентность, сахарный диабет, метаболический синдром и аутоиммунные заболевания. Дальнейшее изучение и уточнение биологической роли лептина является актуальным научно-исследовательским направлением для улучшения ранней диагностики и разработки лечебно-профилактических мероприятий при данных нозологиях.