лимфогистиоцитарная инфильтрация что это
МОРФОЛОГИЧЕСКИЕ КРИТЕРИИ ДИАГНОСТИКИ ХРОНИЧЕСКОГО ЭНДОМЕТРИТА
В работе приведены основные патологоанатомические критерии при установлении диагноза хронический эндометрит.
Для выявления частоты и морфологических критериев хронического эндометрита нами, в одном из частных клиник города, изучены материалы диагностического выскабливания полости матки, нередком при гистероскопическом исследовании. В гинекологическом отделении клиники в последние 2 года исследованы соскобы от 622 женщин.
При обострении ХЭ появляются очаговые или диффузные инфильтраты из лейкоцитов, выраженная гиперемия и отек эндометрия
Таким образом, при исследовании материала диагностического выскабливания полости матки ( соскоба) патологоанатомы должны четко выявлять гистологические проявления хронического эндометрита. В нашем материале морфологические изменения эндометрия соответствовали хроническому неспецифическому лимфоцитарному эндометриту.
Повторные исследования материала с диагнозом хронический эндометрит после окончания курса лечения позволяет судить об эффективности проведенного лечения. Нормализация морфологической характеристики эндометрия ( отсутствие лимфоцитарных инфильтратов, макрофагов, плазматических клеток, фиброза и отека стромы) позволяет судить о восстановлении функциональной активности эндометрия и является критерием эффективности лечения.
Литература
3. Коваленко В.Л и др Характеристика эпителия и внеклеточного матрикса эндометрия при невынащивании беременности ранних сроков, ассоциированном с хроническим эндометритом Арх.пат,2000,№3, с 40-43
8. Сухих Г.Т, Шуршалина А.В, Верясов Иммуноморфологические особенности эндометрия у женщин с хроническим эндометритом В.Н Бюлл.экспер и биол.,2006,№1,113-115
9. Salamonsen L.A., Zhang J., Brasted M. // j. Reprod. Immunol/ 2002. Vol.52, N2.P. 95-108
Созылмалы эндометритті анықтаудың морфологиялық критерийлері
Ахметов Ж.Б
ҚазҰМУ, патологиялық анатомия кафедрасы
Morphological criteria of the diagnosis of chronic endometritis.
Akhmetov J.B.
Department of Pathology of the Kazakh National Medical University.
Abstract Ordinaly chronic endometritis is asymptomatic and discovered during histological examination. For the diagnosis of chronic endometritis is important to indicate the day of taking the material, and the optimal time is 7-9 day of the menstrual cycle. The criteria for the diagnosis of chronic endometritis are lymphoid infiltration in the lower part of the functional and basal layers of the endometrium. Among cell infiltrates it is possible found isolated macrophages and plasma cells. For the diagnosis of chronic endometritis important signs are the fibrosis of the stroma of endometrium and sclerosis of the wall of spiral vessels. According to our data the frequency of chronic endomtrita is 12.5%.
Кафедра патологической анатомии КазНМУ им. С. Д. Асфендиярова
Клинико-морфологические параллели при доброкачественных заболеваниях шейки матки
| Среди гинекологических заболеваний доминирующее положение занимают доброкачественные, в том числе и предраковые, заболевания шейки матки. Многочисленные исследования, раскрывающие вопросы этиологии и патогенеза заболеваний шейки матки, до настоящего времени не позволили окончательно решить эти проблемы. Неоднозначны взгляды на вопросы лечения и профилактики этой патологии. |
В литературе имеются указания на высокое содержание в подэпителиальных тканях лимфоцитов, в том числе киллеров [2, 3], роль которых при доброкачественных процессах шейки матки окончательно не выяснена.
Если этиологический фактор эпителиальной дисплазии в литературе получил достаточно широкое освещение, то в отношении псевдоэрозии шейки матки такой ясности нет. Отсутствие четкой кольпоскопической картины предраковых процессов шейки матки затрудняет их клиническую диагностику, выбор места биопсии и своевременное лечение [1, 4, 8, 10].
Целью работы явилась сравнительная оценка клинических проявлений и патоморфологических изменений при доброкачественных заболеваниях шейки матки, выявление этиологических и патогенетических механизмов в развитии фоновых и предраковых заболеваний шейки матки.
Всем больным были выполнены расширенная кольпоскопия и прицельная биопсия шейки матки. Всего было взято 116 биоптатов. Патоморфологическое исследование проводилось в серийных срезах с окраской препаратов гематоксилином и эозином, по Папаниколау, Паппенгейму, гистохимическими методами. Препараты исследовали под увеличением до 1200 раз. Проведен сравнительный анализ результатов клинических и патоморфологических исследований. В последующем всем больным было проведено криохирургическое лечение выявленных патологических изменений шейки матки.
Результаты и их обсуждение
Таким образом, проведенное кольпоскопическое исследование показало, что в процессе заживления псевдоэрозии шейки матки формируется патологическая зона, характеризующаяся выраженным полиморфизмом.
После выполненной в прошлом диатермокоагуляции и лазеровапоризации псевдоэрозии у 21 женщины железистые структуры под многослойным плоским эпителием были обнаружены вновь, что свидетельствует о неэффективности проведенного лечения. У 1 женщины после криодеструкции шейки матки железистые структуры отсутствовали.
Следует отметить, что из 31 женщины с выявленной патологией верхнего отдела полового аппарата у 15 диагностировано вирусное поражение шейки матки, у 27 лимфоцитарная инфильтрация в строме.
Поскольку выявление вирусных телец в эпителиальных клетках при патоморфологическом исследовании биопсированных тканей представляет большие трудности, следует предположить, что они в исследованном материале обнаружены не во всех случаях. Тем не менее сопутствующая вирусной инвазии лимфоцитарная инфильтрация стромы, легко выявляемая при исследовании, может служить индикатором вирусного поражения.
Таким образом, кольпоскопическую картину эндоцервикоза в стадии завершенной эпидермизации не следует интерпретировать как выздоровление.
При кольпоскопической картине, характеризовавшейся усилением сосудистого рисунка и наличием атипических сосудов в зоне перекрытия, морфологически ЦИН диагностирована у 8 из 15 больных, причем во всех случаях усиление сосудистого рисунка и атипические сосуды сопутствовали картине вирусного цервицита.
Таким образом, полученные результаты свидетельствуют о том, что для ЦИН характерны кольпоскопические картины основы лейкоплакии, полей, открытых протоков желез с эпидермизацией в зоне перекрытия, лейкоплакии. Наличие кистовидно расширенных желез в зоне перекрытия не характерно для ЦИН, тем не менее, у 1 (2,38%) больной из 42 она была выявлена в стенке такой железы.
У большинства больных ЦИН находилась в краях псевдоэрозии в зонах стыка различных типов эпителия.
1. Клиническая картина доброкачественных заболеваний шейки матки, определяемая кольпоскопическим методом, не всегда отражает истинный характер патологического процесса. Невозможна клиническая диагностика предраковых заболеваний (цервикальная интраэпителиальная неоплазия). Вероятность ЦИН наиболее высока при кольпоскопической картине основы лейкоплакии, лейкоплакии, полей, открытых протоков желез с их эпидермизацией.
2. Любые изменения шейки матки, выявленные при расширенной кольпоскопии, требуют биопсии с патоморфологическим уточнением диагноза.
3. Кольпоскопическая картина эндоцервикоза в стадии завершенной эпидермизации патоморфологически представляет собой сложный патологический процесс, включая ЦИН, и не может считаться состоянием выздоровления.
4. Подтверждены данные литературы о том, что этиологическим фактором ЦИН и лейкоплакии является вирусное поражение тканей шейки матки. Индикатором его может служить лимфоцитарная инфильтрация стромы, диагностируемая при патоморфологическом исследовании.
5. Можно предположить, что одним из этиологических факторов псевдоэрозии шейки матки (эндоцервикоза) может быть вирусная инвазия, приводящая к дегенерации многослойного плоского эпителия шейки матки, замещению его цилиндрическим эпителием цервикального типа с пролиферативными процессами в нем и образованием железистых структур.
Другие уточненные неинфекционные гастроэнтериты и колиты (K52.8)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
2. Эозинофильный колит:
— изолированный эозинофильный колит (проктоколит);
— эозинофильный гастроэнтероколит.
Термином «микроскопические колиты» (МК) обозначают особую форму хронических воспалительных заболеваний кишечника, при которой наблюдается синдром диареи, при этом в слизистой оболочке толстой кишки больных определяются признаки воспаления.
Период протекания
Период протекания более 4 недель
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
В качестве возможных триггерных механизмов развития болезни рассматривают курение и влияние лекарственных веществ.
Эозинофильный колит
Этиология неизвестна. Ранее большое значение в его развитии придавали пищевой аллергии, однако она играет роль менее чем у 20% больных. Часто у них отмечается повышенная концентрация IgE в плазме натощак; прием пищи-аллергена вызывает боль в животе, понос и подъем концентрации IgE. В основном уровень иммуноглобулинов при эозинофильном колите остается в норме, не выявляют каких-либо отклонений и реакция бласттрансформации лимфоцитов, определение уровня комплемента и числа лимфоцитов. Таким образом, возможны два варианта болезни: IgE-зависимый и IgE-независимый.
Эпидемиология
Признак распространенности: Крайне редко
Факторы и группы риска
5. Кишечные инфекции Clostridium difficile, Yersinia enterocolitica, Campylobacter jejuni.
6. Гиперпродукция желчи.
Эозинофильный колит
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Микроскопический колит
Признаки
Лимфоцитарный колит
Коллагеновый колит
Длительность диареи (лет)
Средний возраст (лет)
Нормальная эндоскопическая картина
Нормальная рентгенологическая картина
Увеличение содержания межэпителиальных лимфоцитов
Различия
Отношение женщин и мужчин
Частота обнаружения аутоантител
Расширение субэпителиального слоя коллагена
Эозинофильный колит
Симптомы разнообразны и зависят от локализации, степени поражения, возраста. Все проявления сводятся к определенной группе признаков:
— лихорадка (редко);
— потеря веса;
— рвота, тошнота;
— боли в животе, спазмы, вздутие живота;
— кровь в стуле в небольших количествах (редко);
— пальпируемое образование в животе (иногда);
— диарея;
— нарушения сна.
В зависимости от того, какой слой стенки поражен сильнее, выделяют 3 основных клинических варианта течения заболевания:
Диагностика
Микроскопический колит
Программа обследования включает:
Биопсия. Следует брать биоптаты из слизистой оболочки не только сигмовидной ободочной кишки, но и из проксимальных отделов толстой кишки, поскольку именно в указанных отделах выявляются гистологические изменения, свойственные лимфоцитарному колиту.
Эозинофильный колит
Диагностика складывается из:
— тщательно собранного анамнеза (семейный анамнез, связь с приемом пищи);
— выявления сопутствующей аллергической патологии;
— клинической диагностики колита (гастроэнтероколита, проктоколита);
— тестов (клинических и аллергологических);
— инструментальные методы исследования (эндоскопия, биопсия) применяются редко, т.к. диагноз может быть установлен в большинстве случаев клинически.
Тесты
1. Элиминационные диагностические диеты. Простейшим типом элиминационной диеты является исключение из рациона «подозреваемых продуктов» на срок 2-4 недели или дольше. Продолжительность диагностической элиминационной диеты может быть уменьшена до 3-5 дней у детей с ранним клиническим ответом (исчезновением симптомов). При отсутствии подозреваемых аллергенов из рациона исключаются теоретически наиболее значимые пищевые аллергены.
3. Пищевая провокация.
Выбор метода. Двойная слепая, плацебо-контролируемая, оральная провокация с использованием вероятного антигена является идеальным методом для подтверждения развития побочных реакций на пищевые белки, однако такой подход редко используется в клинической практике.
Не слепой метод провокации (когда врач и пациент знают о приеме в пищу потенциального аллергена) может быть использован только в том случае, если симптомы могут быть оценены врачом и пациентом объективно. Использование двойного слепого, плацебо-контролируемого теста возможно, если симптомы по мнению врача являются лишь субъективными.
Информированное согласие. В любом случае пищевая провокация должна выполняться с согласия пациента, т.к. возможны различные реакции со стороны других органов и систем. Эпизоды анафилаксии в анамнезе являются относительным противопоказанием к проведению провокации.
Начальная доза, например, молока должна быть заведомо ниже тех доз, которые могут вызвать реакцию, и должна увеличиваться поэтапно до 100 мл. Сроки появления реакции могут разниться от нескольких часов до нескольких дней. Среднее время между поступлением аллергена и началом проявления отсроченных клинических симптомов составило 13,3 дней (диапазон 4-26 дней). Сильно отсроченные проявления, включая внекишечные (дерматит и пр.), были отмечены лишь у небольшой группы пациентов.
Подготовка: предварительное проведение эффективной элиминационной диеты или достаточно длительное спонтанное уменьшение/исчезновение симптомов.
Оценка результатов. Пищевая провокация была принята в качестве стандартного критерия для диагностики пищевой непереносимости при любом механизме ее развития. Тест считается положительным, если симптомы исчезают после полной элиминации патогенного агента из пищи или если симптомы повторяются в течение 48 часов после провокации. Реакция должна быть воспроизводимой.
Конкретные клинические картины:
1. Энтероколитический синдром:
— Prick-test и RAST, как правило, отрицательны;
— стул, как правило, содержит скрытую кровь, нейтрофилы и эозинофилы;
— при биопсии тощей кишки выявляется атрофия ворсинок и инфильтрация лимфоцитами, эозинофилами и тучными клетками.
2. Колит и проктоколит:
— в анализе кала, как правило, обнаруживаются нейтрофилы;
— эозинофилы могут отсутствовать;
— результаты колоноскопии представлены ниже.
Лабораторная диагностика
Эозинофильный колит
При обследовании могут отмечаться анемия, гипопротеинемия, снижение содержания витаминов и микроэлементов, изменение показателей пробы с D-ксилозой.
У 60%-80% пациентов выявляется эозинофилия.
Исследование кала на эозинофилы. Выявление эозинофилов в кале является важным ключом к диагностике аллергического колита. Однако после обострения в кале могут преобладать лимфоциты и нейтрофилы с небольшим количеством эозинофилов. В кале иногда удается обнаружить кристаллы Шарко-Лейдена.
Дифференциальный диагноз
Дифференциальную диагностику микроскопического колита следует проводить с синдромом раздраженного кишечника, целиакией, болезнью Крона, неспецифическим язвенным колитом, гипотиреозом. Исключают инфекционные колиты, лямблиоз, ишемический колит. Выясняют, употреблял ли больной слабительные препараты.
При дифференциальной диагностике эозинофильного гастроэнтерита и колита требуется исключение заболеваний, протекающих с эозинофилией и аналогичной гистологической картиной (болезнь Крона, коллагенозы, злокачественные новообразования, паразитарные инвазии). Наибольшие трудности представляет дифференциация эозинофильного гастроэнтерита с болезнью Крона, лимфомой кишечника и узелковым периартериитом.
Осложнения
— анемия;
— обезвоживание;
— гиповитаминозы.
Лечение
Микроскопический колит
Общие положения
Лечение направлено на снижение воспаления и симптомов диареи и по сути является эмпирическим (метод «проб и ошибок»), так как каждый случай индивидуален. При адекватно подобранной терапии, большинством симптомов можно управлять. Однако когда лечение заканчивается, симптомы обычно появляются вновь. Большинству пациентов, следовательно, необходимо постоянное лечение чтобы контролировать симптомы. Случаются спонтанные длительные ремиссии.
Поскольку единого мнения по терапии микроскопического колита не существует, ниже приводятся различные мнения.
Диета
1. Конкретных диет не существует. Пищевые продукты, содержащие кофеин, или лактоза должны быть исключены из рациона, так как они стимулируют секрецию жидкости в толстой кишке. Если пациент не в состоянии переваривать жиры, низкое содержание жиров в рационе может быть полезным. Следует избегать приема НПВП (ибупрофен и пр.), так как исследования показали, что они могут быть связаны с коллагеновым колитом. Однако прием парацетамола (ацетаминофен) является допустимым.
Лекарственные препараты
Субсалицилат висмута назначается для лечения коллагеновых колитов курсом 8 недель, в среднем по 8 таблеток в сутки. Эффективность препарата имеет доказательства в исследованиях.
Мезаламин (асакол) также может быть эффективным для лечения хронической диареи, связанной с коллагеновым колитом. Назначается курсом до 6 месяцев. Некоторыми авторами он рассматривается как «препарат первой линии».
Холестирамин чаще всего назначают для лечения высокого уровня холестерина в крови, но этот препарат также может быть использован для уменьшения диареи в случаях коллагенового колита. Холистирамин выпускается в виде порошка, который смешивается с водой. Как правило, препарат применяют в низкой дозе от 1/2 до 1 пакетика в день. Отмечается достаточно хороший эффект холистирамина в низких дозах, чтобы остановить эпизоды водянистой диареи, особенно те, которые возникают после еды. В более высоких дозах холестирамин может вызвать запор (в этих случаях требуется снижение дозы). Кроме того холестирамин может уменьшить всасывание других препаратов, принятых с ним в одно и тоже время. Дополнительной выгодой от лечения может быть снижение холестерина в крови.
Не существует никаких доказательств эффективности других методов лечения, таких как: экстракт босвеллии пильчатой (индийское ладанное дерево), пробиотиков и прочих препаратов и веществ.
Терапия антибактериальными препаратами не оправдала надежд в связи с быстрым возвращением симптомов и высоким риском побочных эффектов.
Один из возможных алгоритмов терапии выглядит следующим образом:
— Первая линия терапии: лоперамид (имодиум) или дифоксилат/атропин (lomotil) для легкой диареи.
— Вторая линия терапии: висмут субсалицилат 2-3 табл. 3-4 раза в день, в течение 1-2 месяцев (эффективно у 90% больных); мезаламин 3 г/сутки в течение 8 недель или холестирамин (особенно, если нарушение всасывания желчных кислот подтверждено документально) при средней дозе до 8 г/сутки при умеренной клинике.
— Третья линия терапии. Если пациент по-прежнему не отвечает на терапию или если у пациента клинически более тяжелый колит, рекомендуется 6-недельный курс будесонида в минимальной эффективной дозе (обычно 9 мг каждое утро) или 2-недельный курс высоких доз преднизолона (60-80 мг/сутки). Курсы будесонида предпочтительнее вследствие меньшего побочного эффекта. Рецидивы, возникающие после прекращения приема будесонида, обычно лечатся возобновлением приема этого же лекарства.
Более длинные курсы преднизолона (до 2 месяцев) могут быть необходимы у некоторых пациентов, рефрактерных к терапии, но рецидивы встречаются и после ее прекращения.
— Четвертая линия. В некоторых упорных случаях может быть эффективен азатиоприн (около 2 г/кг/сутки) или 6-меркаптопурин, но ответ на такую терапию может возникать часто только через несколько месяцев. Метотрексат является альтернативным препаратом.
У пациентов, отвечавших на лечение, но испытывающих рецидивы, часто бывают эффективны ранее использованные и показавшие себя лекарства.
Лимфоцитарная инфильтрация Джесснера-Канофа
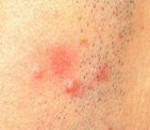
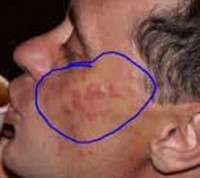
Лимфоцитарная инфильтрация Джесснера-Канофа – редкий хронический дерматоз, характеризующийся доброкачественной инфильтрацией кожи лимфоцитами. Заболевание имеет волнообразное течение, склонно к саморазрешению. Клинически проявляется высыпанием на неизменённой коже плоских гладких синюшно-розовых бляшек или папул, которые сливаются в очаги величиной с ладонь ребенка или взрослого. Первичные элементы имеют чёткие границы, шелушатся. Бляшки обычно единичные, располагаются на лице, шее, туловище, конечностях. Диагностируется клинически с гистологическим подтверждением, иногда проводят молекулярно-биологические исследования. Лечение – НПВС, гормональная терапия, препараты местного действия.
Общие сведения
Лимфоцитарная инфильтрация Джесснера-Канофа – доброкачественная псевдолимфома кожи с хроническим волнообразным рецидивирующим течением. Встречается редко. Чаще возникает у мужчин старше 20 лет. Сезонных, расовых различий не имеет, не эндемична. Иногда наблюдается улучшение в летний период. Впервые данная патология была описана в 1953 году, когда М. Джесснер и Н. Каноф рассмотрели ее как самостоятельное заболевание со сквозной инфильтрацией лимфоцитами всех слоёв дермы. Название «псевдолимфома» в 1965 году ввел К. Мач, объединивший инфильтрацию Джесснера-Канофа в одну группу с другими разновидностями лимфоцитарной инфильтрации.
В 1975 году О. Браун отдифференцировал тип заболевания, отнеся инфильтрацию лимфоцитами к В-клеточным псевдолимфомам, однако позже специалисты стали рассматривать патологию как Т-псевдолимфому. Именно Т-лимфоциты обеспечивают доброкачественное течение патологии и возможность спонтанной инволюции первичных элементов. Дальнейшие исследования показали, что в возникновении и течении лимфоцитарной инфильтрации Джесснера существенную роль играет иммунная система организма. Возможно, это связано с тем, что клетки иммунной системы располагаются в пищеварительном тракте, а он поражается в 70% случаев заболевания. Изучение лимфоцитарной инфильтрации Джесснера-Канофа продолжается и в настоящее время. Понимание причин возникновения и развития Т-лимфоидных процессов имеет большое значение в разработке патогенетического лечения псевдолимфом.
Причины лимфоцитарной инфильтрации
Наиболее вероятными причинами лимфоцитарной инфильтрации Джесснера-Канофа принято считать гиперинсоляцию, укусы клещей, инфекции, патологию желудочно-кишечного тракта, использование дерматогенной косметики и нерациональный приём лекарственных препаратов, провоцирующих системные иммунные нарушения, визуально представленные инфильтративными изменениями в коже. Механизм лимфоцитарной инфильтрации Джесснера-Канофа заключается в следующем: интактный эпидермис даёт Т-лимфоцитам возможность инфильтрировать глубокие слои дермы, располагаясь в сосочковых выростах и вокруг сосудистых сплетений по всей толще кожи. Триггеры заболевания запускают воспаление, на которое реагируют непосредственно клетки кожи и клетки иммунной системы. В процесс купирования воспаления включаются Т-лимфоциты, обеспечивающие доброкачественный ответ иммунной системы в виде пролиферации эпителиальных клеток дермы.
Одновременно в коже развивается банальное воспаление, проходящее три стадии: альтерации, экссудации и пролиферации с участием гистиоцитов – клеток ретикулярной ткани. Гистиоциты группируются и образуют островки, напоминающие лимфоидные фолликулы. На конечном этапе купирования воспаления два параллельных процесса пролиферации дополняют и усиливают друг друга. Так возникает очаг лимфоцитарной инфильтрации. Поскольку лимфоциты гетерогенны, оценка их гистохимических свойств с помощью иммунологических маркеров и моноклональных антител легла в основу иммунофенотипирования. Этот анализ имеет большое диагностическое значение в современной дерматологии.
Симптомы лимфоцитарной инфильтрации
Первичным элементом кожной сыпи при лимфоцитарной инфильтрации Джесснера-Канофа является крупная плоская розово-синюшная бляшка или папула с чёткими границами и гладкой поверхностью, имеющая тенденцию к периферическому росту. Сливаясь между собой, первичные элементы образуют кольцевидные или дугообразные «острова» с участками шелушения. Разрешение высыпавших элементов начинается с центра, поэтому сливные очаги могут иметь западание в центральной части. Типичной локализацией принято считать лицо, шею, околоушное пространство, затылок, лоб, щёки и скулы. Редко высыпания появляются на коже туловища и конечностях. Обычно первичный элемент одиночный, реже наблюдается тенденция к распространению процесса.
Лимфоцитарная инфильтрация Джесснера-Канофа характеризуется волнообразным рецидивирующим течением. Резистентна к проводимой терапии, способна спонтанно саморазрешаться. Рецидивы обычно возникают в местах прежней локализации, но могут захватывать и новые участки кожного покрова. Несмотря на длительное хроническое течение, внутренние органы в процесс не вовлекаются.
Диагностика лимфоцитарной инфильтрации
Заболевание диагностируется дерматологом на основании анамнеза, клиники, гистологии и люминесцентного микроскопирования (типичное свечение на границе дермоэпидермального соединения не определяется) с обязательной консультацией иммунолога и онколога. Гистологически при лимфоцитарной инфильтрации Джесснера-Канофа выявляется неизменённый поверхностный слой кожи. В толще дермальных слоёв обнаруживается группирование лимфоцитов и клеток соединительной ткани вокруг сосудов.
В сложных случаях проводят иммунотипирование опухоли, гистохимическое и молекулярное тестирование. К. Фан с соавторами рекомендуют основывать диагностику на результатах ДНК-цитофлюориметрии с анализом количества нормальных клеток (при лимфоцитарной инфильтрации Джесснера-Канофа более 97%). Дифференциальную диагностику проводят с саркоидозом, системной красной волчанкой, центробежной эритемой Биетта, кольцевидной гранулёмой, группой лимфоцитарных опухолей, токсикодермией и сифилисом.
Лечение лимфоцитарной инфильтрации
Лечение направлено на купирование острой фазы лимфоцитарной инфильтрации Джесснера-Канофа и увеличение продолжительности светлых промежутков. Терапия патологии неспецифическая. Отмечается хороший терапевтический эффект при назначении антималярийных препаратов (хлорохин, гидроксихлорохин) и нестероидных противовоспалительных средств (диклофенак, индометацин) после предварительного лечения сопутствующей патологии желудочно-кишечного тракта. Если состояние пищеварительной системы позволяет, применяют энтеросорбенты. Местно показаны гормональные кортикостероидные мази и кремы, а также инъекционные блокады очагов высыпаний триамцинолоном и бетаметазоном. При резистентности к проводимой терапии подключают плазмаферез (до 10 сеансов).