лимонная кислота и сода реакция что образуется
Чудеса и сода: делаем интересные опыты с хорошо знакомым продуктом
Взаимодействие соды с уксусом называется реакцией нейтрализации. Суть её состоит в том, что уксусная кислота при взаимодействии с щелочью, каковой является сода, нейтрализуют друг друга, выделяя углекислый газ. Эту реакцию домохозяйки использую в кулинарии для придания пышности выпечке. Но гораздо эффектнее данная химическая реакция выглядит в опыты под названием «Извержение вулкана».
В качестве жерла вулкана можно приспособить небольшую пластиковую бутылку. Для достоверности можно спрятать ее внутрь горки песка. Насыпаем в бутылочку пищевую соду и краситель, добавляем пару ложек моющего средства. После этого аккуратно добавляем уксусной кислоты. К восторгу зрителей вулкан начинает извергать мыльную пену, словно огненную «лаву».
Примерно 1/3 бутылки заполняем водой, в которую нужно добавить три чайных ложки уксуса или всыпать столько же лимонной кислоты и перемешать. В воздушный шар насыпаем через воронку соду. Надеваем на горлышко бутылки воздушный шарик и постепенно пересыпаем соду из шарика в бутылку.
В результате шарик начинает надуваться за счет выделения углекислого газа.
Наливаем горячую воду в стакан или банку. Добавляем соду и размешиваем. Когда сода перестанет растворяться, это значит, что ее стало достаточно для нашего опыта. На нитку подвешиваем предметы, на которых будем выращивать кристаллы, – например, проволоку. Нитку привязываем к палочке и устанавливаем на банку. Ждем около суток.
При остывании жидкости сода прекратит растворяться и станет оседать на нитке с фигуркой. Когда вода, насыщенная содой, начнет понемногу испаряться, кристаллы будут «расти».
Сначала растворить в стакане свежей чистой и прокипяченной воды половину ложки уксуса, а затем добавить столько же соды. После того как в напитке началась реакция взаимодействия кислоты и щелочи, в ней образуется пена из мелких пузырьков, можно пить небольшими глотками. Этот напиток прекрасно утоляет жажду и избавляет от изжоги.
Вместо уксуса можно взять лимонную кислоту – четверть ложки на стакан воды. Если напиток сделать без лимонной кислоты на натуральном лимонном соке, будет еще лучше и полезней. Лимонный сок подарит напитку свежий аромат и приятный вкус. А если добавить пищевых красителей, получится набор веселых и вкусных напитков.
Чтобы составлять тайные письма, можно сделать невидимые чернила из соды. Возьмем стакан и заполним его теплой водой наполовину. Добавим 2-3 чайные ложки пищевой соды и тщательно размешаем. Затем обмакиваем кисточку в жидкость и пишем на бумаге тайное послание. От воды на поверхности бумаги появятся мокрые следы. Чтобы сделать надпись невидимой, потребуется её просушить. Это можно сделать, положив бумажный лист на батарею либо на солнце.
Как только надпись просохнет, ни один человек не сможет прочитать её. Но если только нагреть утюг и провести им по поверхности листа несколько раз или подержать лист бумаги с письмом над горящей свечой, надпись обретет коричневый оттенок, и тайное станет явным.
Добавим в воду темный рис или любую иную крупу. Поначалу она осядет на дно. Затем добавим в стакан воды ложку соды, тщательно размешаем и начнем вливать в стакан уксус. В итоге каждое зернышко риса покроется маленькими шариками и начнет «танцевать» в стакане, сперва поднимаясь вверх, а затем опускаясь вниз.
После того, как этот завораживающий танец начнет затихать, можно добавить в воду краситель и блестки из фольги и понаблюдать, как они распределяются по стакану, создавая иллюзию парения в пространстве.
Применением соды – надежный способ потушить пламя. Нагреем пищевую соду и поместим над ней горящую спичку. И тут же увидим, что она гаснет, потому что сода разлагается и высвобождает углекислый газ, который не позволит огню разгореться.
Кстати, такой же газ входит в состав пожарных огнетушителей. Не зря же огнетушитель – это первое, что обычно используется для предотвращения возгорания в помещении или автомобиле.
Такой опыт лучше проводить с использованием алюминиевой кастрюли, а при отсутствии таковой можно положить на дно обычной кастрюли алюминиевую фольгу. Положим туда потускневшие серебряные изделия так, чтобы они касались алюминия. В отдельной кастрюле или чайнике нагреем воду до кипения. После того, как она закипит, добавим столовую ложку пищевой соды на литр воды. Выльем содовый раствор на изделия из серебра, пока он полностью их не покроет. Если серебро слишком тусклое, потребуется повторить процедуру.
Темный налет представляет собой сульфид серебра, который образуется от его соединения с серой. При взаимодействии с содой происходит химическая реакция, при которой алюминий забирает серу из серебра. Таким образом оно опять обретает свой первоначальный блеск.
Эффективные способы гашения соды лимонной кислотой
Пищевая сода – один из наиболее широко используемых разрыхлителей в выпечке, однако до сих пор некоторые хозяйку задаются вопросом — как погасить соду лимонной кислотой. Рассмотрим эту пищевую добавку более подробно, а так же научимся использовать в кулинарии.
Также известное как бикарбонат натрия, это химическое соединение встречается в природе в кристаллическом виде, а для последующего использования в кулинарии или быту его измельчают до мелкого порошка.
Принцип работы пищевой соды в выпечке
Пищевая сода известна любой хорошей домохозяйке и пекарю. Это щелочное соединение выделяет углекислый газ, маленькие пузырьки которого начинают активно работать над тестом, заставляя его подняться быстрее. Также благодаря возникающим процессам формируется структура теста, что делает его воздушным и «пушистым».
Для ускорения процесса выделения углекислого газа можно воздействовать на пищевую соду тремя способами:
Смешивание с кислотными соединениями
Наилучшим способом, гарантирующим отличный результат, является добавление на стадии замешивания теста кислотных соединений. Это может быть уксус, йогурт, кефир или лимонная кислота. Так что, если в рецептуре выпечки присутствует кисломолочный продукт, то переживать о дополнительном добавлении кислот не нужно. Добавленные в выпечку мелиса или мед, хотя это и кажется невероятным, также активируют реакцию пищевой соды.
Реакция с теплом
Пищевая сода будет производить углекислый газ при воздействии тепла даже без добавления кислот. Минимальная температура для начала этого процесса – 80 С. Данный способ хоть и быстрый, но не гарантирует получение воздушной структуры теста.
Использование кислот и тепла
Самые опытные домохозяйки объединяют два варианта в один. Тесто, в которое добавили пищевую соду и кислоту, накрывается полотенцем и ставиться на 1 час в теплое место (достаточно поместить его на включенную батарею). Под воздействием тепла тесто начинает медленно подниматься и становиться легким и, как может показаться, пушистым. Максимальный подъем теста будет происходить уже в духовке, где воздействие температур более сильное — это завершающий аккорд действия углекислого газа.
Пищевая сода часто работает настолько быстро, что этот процесс можно буквально наблюдать в режиме реального времени. А готовая сдоба может поразить любого своей нежной и пористой структурой, полученной благодаря разложению соды в процессе выпечки.
Отличия между пищевой содой и разрыхлителем
При попытке заменить в рецептуре выпечки разрыхлитель на пищевую соду, можно потерпеть фиаско, поскольку два эти вещества, несмотря на колоссальное сходство, работают по-разному. Пищевая сода — это “чистый” бикарбонат натрия, без добавления каких-либо веществ. Разрыхлитель — это та же пищевая сода со “встроенной” кислотой. В разрыхлителе кислота находится в виде солей, поэтому она не реагирует с основным компонентом (пищевой содой). Для начала реакции необходимо только добавить жидкость. Поэтому недостаточно просто заменить разрыхлитель на соду. Необходимо учитывать добавление к последней кислотного компонента, например, лимонной кислоты.
Как проверить свежесть соды
Многие утверждают, что у пищевой соды нет срока годности. Она стоит на полке у каждого уважающего себя человека и, ввиду использования в небольших дозировках (в выпечке необходима всего 1 ч. ложка), может простоять в шкафу годы. Поэтому стоит отметить, что сода имеет свойство разлагаться со временем. И чтобы не разочароваться в ней в случае неудач в хлебопекарном деле, стоит проверить её эффективность заранее.
Для этого не нужно отправлять щелочь в лабораторию. Достаточно провести простой эксперимент в домашних условиях. Просто добавьте щепотку пищевой соды к небольшому количеству лимонной кислоты (уксуса) в миске. Появление пены является подтверждением того, что сода всё ещё активна и будет работать.
Правила гашения пищевой соды
Рассмотрим, как гасится сода лимонной кислотой.
Для достижения сильного эффекта, к пищевой соде необходимо добавить кислоту, которая подействует как катализатор и запустит реакцию быстрее. Этот процесс называется гашение соды. При соблюдении необходимых условий, кислотно-щелочная реакция будет сильной и устойчивой на протяжении всего процесса выпечки.
Очень важно, чтобы процесс выделения углекислого газа происходил непосредственно в тесте. В противном случае, он будет расходоваться зря, и желаемый эффект не будет достигнут. Более того, при гашении соды «на стороне», есть риск вместо пористой структуры получить лишь мыльный привкус. Поэтому опытные пекари советуют смешать отдельно все сухие и жидкие (в том числе и кислоты для гашения) компоненты рецептуры по отдельности, а потом объединить их в ёмкость, где будет готовиться тесто.
Если при замешивании теста будет допущена ошибка, то выделение газа будет минимальным и, вполне возможно, тесто не поднимется вовсе.
Использование лимонной кислоты для гашения: пропорции
Самый распространенный способ гашения пищевой соды – добавление к ней лимонной кислоты. Начинающим стоит обратить своё внимание на неё, поскольку при использовании этого компонента можно не бояться испортить вкус выпечки при ошибках в пропорциях. Можно использовать как порошок лимонной кислоты, так и сок лимона.
При использовании сока лимона не требуется никаких подготовительных операций. На 1 ч. ложку соды требуется всего 10 ч. ложек лимонного сока. Необходимо только помнить, что компоненты добавляются по правилам “правильного гашения”.
Лимонную кислоту необходимо перед добавлением в замес заранее развести с водой. Для этого потребуется треть стакана воды. Такое же количество понадобится и для соды. Жидкие компоненты смешиваются в отдельной ёмкости, после чего добавляются к муке и соде.
Как сделать разрыхлитель в домашних условиях
Приготовление домашнего разрыхлителя очень простое, с ним справится даже новичок. Более того, это сократит затраты во времени в будущем — не придется каждый раз производить подготовку кислоты и соды.
Для приготовления разрыхлителя понадобится:
Смешайте все компоненты и тщательно встряхните ёмкость для их равномерного распределения по всему объему тары. Полученный разрыхлитель добавляется сразу в муку при приготовлении замеса.
Хранить его стоит в сухом темном месте. Срок хранения не отличается от срока годности обычной пищевой соды.
Альтернативные способы гашения соды
Определенно бывают случаи, когда дома не оказалось лимонной кислоты или лимона. Поэтому важно рассмотреть использование других кислот для гашения пищевой соды.
Гашение соды уксусом столовым 9%
Использование этой кислоты также распространено, как и лимонной. Единственная опасность таится в том, что при случайной ошибке в дозе в большую сторону можно получить на выходе выпечку с горьковатым привкусом. Поэтому методика смешивания жидких и сухих компонентов по отдельности для начинающего не подойдет.
При использовании уксуса гашение соды лучше проводить отдельно от всех компонентов. Наберите необходимое количество соды (обычно, это не больше 1 ч. ложки) и добавьте к ней несколько капель уксуса. Как только смесь начнет пузыриться и шипеть (это значит, что кислоты достаточно), добавьте ее в замес.
Гашение соды яблочным уксусом
Технология использования этой кислоты аналогична с технологией при гашении соды столовым уксусом. Единственная разница лишь в том, что яблочный уксус даёт меньше горечи.
Гашение соды кисломолочными продуктами
При использовании кефира или сметаны, так же как и с лимонной кислотой, можно не бояться совершить промах в дозировке. Они никак не испортят вкусовые качества готового продукта. Соотношение гашения соды составляет 1:1, то есть на 1 ч.ложку щелочи понадобится всего 1 ч.ложка кислоты.
Если же рецептура предполагает использование в ней кисломолочным продуктов, то просто добавьте соду в тесто. Дополнительное добавление кислот уже не потребуется.
Рецепты
Рецепт бананового пирога с черникой
Этот пирог прост в приготовлении, и не требует особых знаний. Для пирога понадобятся следующие ингредиенты:
Готовность пирога можно проверить спичкой. После её погружения в пирог спичка должна остаться сухой, без остатков теста.
Оладьи без дрожжей с использованием соды и лимонной кислоты
Понадобятся следующие ингредиенты:
Обжаривайте оладьи на хорошо нагретой сковороде до готовности.
Химизм реакции лимонной кислоты с бикарбонатом натрия и его зависимость от давления.
Изменено 21.12.16 автор FerrumCat
Только сейчас сообразил. По мере расходования CO2 давление в системе будет падать, и реакция пойдет дальше. То есть будет эффект частичного редуктора.
Не редуктора, а аккумулятора. У редуктора давление на выходе постоянно, до тех пор пока давление на входе выше или равно заданного давлению на выходе.
Так ребята, стоп! Чего то я не понимаю. Какое изменение давления, где? У меня стоял манометр на аппарате. Давление в процессе поднималось всего лиш на 0,5 атмосфер!
Если запускать реакцию сжатием бутылок, то нормальный человек не сможет превысить начальный порог в 1 атм.
Вы уж извините старого.
Вы о каком изменении давления пишете.
Автор темы написал подробно, как проекает реакция лимонки с содой, разбил эту реакцию на последовательные этапы и показал зависимость от внешних условий. Еще бы автор темы источник этой информации указал, было бы вообще прекрасно.
Изменено 22.12.16 автор WViktor
Если разбираться дальше, то не стоит рекомендовать применение сильных кислот. С ними идёт очень бурная реакция и бутылки могут лопнуть. Это заметно даже с уксусом. Тут нужен опыт работы. И вообще, нам больше скандалы по поводу кислоты не нужны. Прецендент был.
Более интересными могли быть данные по влиянию объёма жидкости в системе, её площади и пр.
FerrumCat рассматривает процесс не в конкретном генераторе, а в закрытой емкости, когда ЛК и сода загружаются одновременно. При этом давление зависит от количества реагентов и объема емкости. Просто изложена последовательность реакций и их зависимость от внешних условий. По этому теоретически давление может быть любым. Но при этом FerrumCat показывает, что с ростом давления реакция идет не до конца, но проходит полностью при снижении давления.
Hedin . Более интересными могли быть данные по влиянию объёма жидкости в системе, её площади и пр.
Вы не единожды обращали внимание на этот вопрос.
Могу предположить, что эта зависимость связана с конкретной реализацией генератора, а именно генератора Славкина, которой Вы придерживаетесь. А именно не полным охватом зоной подаваемой кислоты зоны соды в бутылке. И чем более широкое дно, тем меньше пересекаются зоны распространения кислоты и соды. Такая же картина скорее всего получается и при увеличении количества воды в системе.
Славкин предложил решение, но на него ни кто не обратил внимание. Надо перевернуть бутылки крышками вниз. Тогда сода постоянно будет перемещаться под действием силы тяжести практически в одну точку, в крышку, за счет конфигурации бутылки в виде воронки. В эту же точку (на крышку) надо подавать и кислоту. Это конечно не решит проблему полностью, но во многом нивелирует указанную Вами зависимость. Умозрительно наиболее правильно, в случае с перевернутыми бутылками, использовать высокие бутылки с узким плавно сужающимся горлышком, типа таких:
Изменено 22.12.16 автор kichrot
Hedin
И вообще, нам больше скандалы по поводу кислоты не нужны.
FerrumCat
Вывод — при 1 атм выход по лимонной кислоте 83%, при 10 атм — 60%
Изменено 24.12.16 автор oltrew
Продолжение подробного обзора кислот-солей будет позже. и может кто добавит свои СО2-прикладные химические знания.
Глядя на табличку, удобнее делать выводы о неприменимости, сложности, неэффективности применения некоторых в-в или об их необходимых концентрациях в растворе.
Пример с растворимостями:
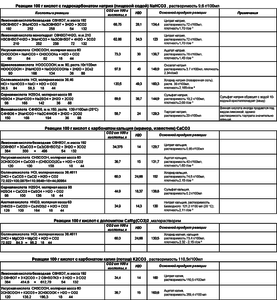
При реакции 100 г лимонной кислоты с пищевой содой образуется 134 г Цитрата натрия (ЦН), растворимостью 72г/100мл (25 C). А воды всего 28 и 34 г. При насыщении (а может и раньше) ЦН выстесняет из раствора значительно менее растворимую соду. В насыщенном растворе цитрата натрия вместо 96 г/л соды будет всего 13 г/л, т.е. в 7,5 раз меньше (пропорционально растворимостям). Такое сильное изменение концентрации соды в растворе заметно увеличивает химический гистерезис и разгоняет давление.
От 100 г безводной кислоты образуется 134,4 г ЦН. Для его полного растворения нужно добавить не менее 159 мл воды.
При использовании моногидрата нужно добавлять не менее 137 мл воды на 100 г кислоты.
С учетом присутствия в растворе еще соды, на 100 г лимонной кислоты должно быть (округлил) не менее 200 г воды для безводной и не менее 150 г воды для моногидрата.
Почти такая же ситуация с уксусной кислотой. При реакции 100 г 70%-ной эссенции с пищевой содой образуется 95,7 г ацетата натрия растворимостью 76г/100мл. А воды всего 30 г. Значит для НЕпоявления в зоне реакции нерастворимого осадка ацетата натрия, воды в соде должно быть не менее 110 г на каждые 100 г эссенции (с учетом еще растворенной соды). А эссенция и 80%-ная бывает.
Тема интересная и полезная, желательно ее закрепить.
Цветные опыты для малышей
Хотите окунуться в мир волшебства и превращений? Предлагаем Вашему вниманию цветные опыты для малышей! Существуют такие вещества, которые меняют цвет в кислоте и в щелочи. Называются они индикаторы. Для ребенка это слово новое и сложное. Его суть он поймет несколькими годами позже, а пока ему достаточно просто увидеть первые химические опыты с изменением цвета и восхититься этим маленьким чудом! Кроха может наблюдать за Вашими действиями, а может помогать (капать, перемешивать, наливать, переливать, насыпать ложкой и пр.), и тогда радости будет еще больше.
Цветные опыты для малышей
Важно! Даже самые безобидные химические опыты для малышей следует проводить только в присутствии взрослого! Наши цветные опыты ориентированы примерно на детей от трех лет. Можно проводить их и раньше, если ребенку это интересно. Не забывайте о мерах предосторожности и внимательно следите за тем, чтобы малыш не обжегся и не попробовал материалы и жидкости на вкус.
Меняем цвет чая
Материалы и оборудование:
черный чай, кипяченая вода, лимонная кислота, питьевая сода (в качестве щелочи), прозрачные пластиковые стаканчики объемом 50 мл (5 шт.), чайные ложки (лучше пластиковые).
1. Наполните 3 стаканчика на 1/2 крепким чаем.
2. Возьмите еще два стаканчика, наполните их до половины кипяченой водой. В одном стаканчике растворите 1/3 чайной ложки лимонной кислоты, а в другом – столько же соды (лучше растворить ее в горячей воде), долейте воды до полного стакана.
3. Выставьте стаканчики с чаем в ряд перед ребенком, попросите его в первый стаканчик перелить кислоту, а в третий – раствор соды. Что при этом произошло и как изменился цвет? Чай с кислотой посветлел, а чай с содой потемнел.
при растворении лимонной кислоты в воде стаканчик станет чуть холоднее, чем был;
при растворении соды в горячей воде выделится углекислый газ.
Похожие опыты для малышей с изменением цвета можно провести с вином, виноградным и ежевичным соком, соком свеклы и цветной капусты.
Маленькому помощнику придется выполнить немало действий: налить воду, заварить чай, набрать ложкой лимонную кислоту, размешать ее. Это все прекрасно тренирует моторику. Между делом можно еще посчитать стаканчики, повторить понятия светлый-темный.
Делаем цветную пену
Материалы и оборудование:
1. Возьмите большой стакан, налейте в него 1 маленький стаканчик (50 мл) воды, окуните ватную палочку в “зеленку”, а затем подкрасьте ею воду в стакане.
2. Медленно прилейте раствор кислоты к раствору зеленки в большом стакане. Цвет на глазах начнет меняться (от изумрудно-зеленого до салатового, желтоватого). Зеленка – тоже индикатор! Волшебное зрелище, не правда ли?
3. Всыпьте в получившийся раствор две чайные ложки соды. Начнется бурная реакция: салатовый раствор вновь начнет превращаться в бирюзовый, а над раствором образуется голубая пена!
Пояснение для родителей: в процессе опыта в стакане появились пузырьки углекислого газа, образовалась пена, а индикатор снова поменял свой цвет, так как щелочи стало больше, чем кислоты из-за добавленной соды.
Такая зрелищная цветная химическая реакция понравится малышу!
Находим в продуктах крахмал
Что такое крахмал и где он содержится? Крахмал – это такое вещество, в котором растения делают запасы на случай засухи или для зимовки. Например, люди обнаружили, что клубни картофеля очень питательны (ими легко можно наесться), не менее питательны и пшеница, кукуруза, тыква, рис. Во всех этих продуктах содержится много крахмала. Попробуйте вместе с крохой «увидеть» крахмал в продуктах.
Материалы и оборудование:
раствор йода, кипяченая вода холодная и горячая, крахмал, прозрачные пластиковые стаканы объемом 50 мл (3 шт.), чайные ложки (лучше пластиковые), ватная палочка, кусочки фруктов и овощей (картофель, морковь, яблоко и др.), мякиш белого хлеба.
1. Примерно наполовину наполните стакан водой и капните туда пару капель йода. Обратите внимание малыша на цвет раствора йода (желто-бурый/коричневатый), дайте понюхать.
2. В два других стакана поместите немного (не больше ¼ чайной ложки) крахмала, прилейте 2-3 чайные ложки холодной воды и перемешайте, а затем наполовину заполните стаканы кипятком и перемешайте. Дайте полученным растворам остыть.
3. Прилейте 5-10 капель получившегося раствора йода к 1 из стаканов с раствором крахмала и наблюдайте за изменением цвета. Он станет серо-сиреневым.
4. Во второй стакан с раствором крахмала добавьте половину раствора йода. Жидкость станет сине-черного цвета.Объясните юному исследователю, что крахмал и йод реагируют друг с другом. Получается, что йод – индикатор содержания крахмала и наоборот!
5. Давайте теперь проверим, в каких продуктах есть крахмал (пусть это делает ребенок), будем окунать в раствор йода кусочки фруктов и овощей и внимательно их рассматривать. Если увидим черный, синий или голубой цвет, то в продукте есть крахмал!
Таков удивительный мир химии и цветных реакций. Впереди Вас ждут необычные эксперименты, открытия и новые опыты для малышей!
Игропедагог, эксперт по вопросам раннего развития