лиссэнцефалия у детей что это
Публикации в СМИ
Агирия
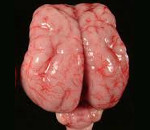
Агирия (лиссэнцефалия, агирия–пахигирия) — дефект развития в виде слабой выраженности извилин коры головного мозга вследствие нарушения миграции нейробластов в эмбриогенезе. Агирия типа I — основное проявление синдромов Миллера–Дикера и Нормана–Робертса. Агирия типа II (кортикальная дисплазия) — нарушение цитоархитектоники с облитерацией субарахноидального пространства эктопической нейроглиальной тканью и гидроцефалией — компонент синдрома Уокера–Варбурга, врождённой мышечной дистрофии Фукуяма (253800) и некоторых других семейных синдромов.
• Миллера–Дикера синдром агирии (агирия типа I, *247200, три локуса: 17p.13.3, ген LIS1 [601545, в 90% — делеция]; 2p11.2, ген LIS2 [*600217]; второй локус 2q13, r ): микроцефалия, агирия (утолщённая кора с 4 слоями клеток) в сочетании с дефектами развития лицевого скелета и множественными пороками развития внутренних органов.
• Нормана–Робертса синдром — вариант агирии I типа с микроцефалией, низким покатым лбом и выступающей спинкой носа (*257320, r ); в отличие от синдрома Миллера–Дикера, делеции в хр. 17 не обнаружено.
• Уокера–Варбурга синдром (агирия типа II, *236670): сочетание агирии с обструктивной гидроцефалией (микрополигирия).
• Агирия X-сцепленная (*300067, Xq22.3–q23, ген LISX, À доминантное): сочетание агирии с агенезией мозолистого тела.
• Пахигирия с умственной отсталостью и судорожными припадками (600176, r ): тяжёлая энцефалопатия, умственная отсталость, задержка психомоторного развития, генерализованные клоникотонические судороги, утолщение коры мозга до 10–12 мм на МРТ.
МКБ-10. Q04.3 Другие редукционные деформации мозга
Код вставки на сайт
Агирия
Агирия (лиссэнцефалия, агирия–пахигирия) — дефект развития в виде слабой выраженности извилин коры головного мозга вследствие нарушения миграции нейробластов в эмбриогенезе. Агирия типа I — основное проявление синдромов Миллера–Дикера и Нормана–Робертса. Агирия типа II (кортикальная дисплазия) — нарушение цитоархитектоники с облитерацией субарахноидального пространства эктопической нейроглиальной тканью и гидроцефалией — компонент синдрома Уокера–Варбурга, врождённой мышечной дистрофии Фукуяма (253800) и некоторых других семейных синдромов.
• Миллера–Дикера синдром агирии (агирия типа I, *247200, три локуса: 17p.13.3, ген LIS1 [601545, в 90% — делеция]; 2p11.2, ген LIS2 [*600217]; второй локус 2q13, r ): микроцефалия, агирия (утолщённая кора с 4 слоями клеток) в сочетании с дефектами развития лицевого скелета и множественными пороками развития внутренних органов.
• Нормана–Робертса синдром — вариант агирии I типа с микроцефалией, низким покатым лбом и выступающей спинкой носа (*257320, r ); в отличие от синдрома Миллера–Дикера, делеции в хр. 17 не обнаружено.
• Уокера–Варбурга синдром (агирия типа II, *236670): сочетание агирии с обструктивной гидроцефалией (микрополигирия).
• Агирия X-сцепленная (*300067, Xq22.3–q23, ген LISX, À доминантное): сочетание агирии с агенезией мозолистого тела.
• Пахигирия с умственной отсталостью и судорожными припадками (600176, r ): тяжёлая энцефалопатия, умственная отсталость, задержка психомоторного развития, генерализованные клоникотонические судороги, утолщение коры мозга до 10–12 мм на МРТ.
МКБ-10. Q04.3 Другие редукционные деформации мозга
Лиссэнцефалия у детей что это
Звоните нам по телефону 8 (812) 241-10-46 с 7:00 до 00:00 или оставьте заявку на сайте в любое удобное время
Ваша заявка принята!
Благодарим за обращение.
В ближайшее время с вами свяжется наш специалист.
Лиссэнцефалия, шизэнцефалия, порэнцефалия: причины, симптомы, прогноз
Сглаживание извилин коры головного мозга (агирия) формируется внутриутробно. Патогенетическим механизмом развития нозологии является нарушение эмбриогенеза, обусловленного патологией распространения из первичной нервной трубки нейробластов. Сглаживание поверхности сопровождается снижением умственной, интеллектуальной активности.
Сопутствующие неврологические расстройства постепенно нарастают. Заболевание приводит к летальному исходу еще в грудном возрасте.
Отсутствие мозговых извилин – исключает оптимальное функционирование второй сигнальной системы, которая существует только у человека. Складчатость повышает функциональную поверхность мозга.
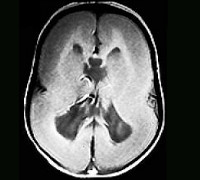
Даже раннее выявление с помощью МРТ головного мозга не позволяет спасти жизнь ребенку с лиссэнцефалией первого или второго типа.
На протяжении беременности врожденные пороки развития церебральных структур определяются ультразвуковым обследованием (УЗИ). Достоверность процедуры – 60%, поэтому иногда после МРТ выявляются врожденные пороки развития мозга, хотя внутриутробный мониторинг патологии не определяет патологических состояний.
Пример заключения магнитно-резонансной томографии:
Нозология нередко сочетается со стигмами церебрального дисэмбриогенеза – макроцефалией, агирией, микроцефалией.
Медицинские источники утверждают, что патологию может обнаружить УЗИ после двадцать шестой недели беременности.
МРТ: норма и лиссэнцефалия
Лиссенцефалия 2 типа имеет альтернативное название «синдром Норман-Робертс». Канадские ученые, открывшие заболевание, считают основной причиной формирования заболевания мутацию гена «RELN».
Участок ДНК, отвечающий за нозологию, кодирует образование протеина «рилина». Синдром характеризуется множеством клинических изменений:
Перинатальное УЗИ обнаруживает большую часть случаев болезни.
Причины возникновения лиссенцефалии
Формирование внутримозговой коры у плода проходит несколько стадий развития. Вначале происходит деление нейронов. Постепенно нервные клетки мигрируют из первоначального матрикса в места постоянного расположения. Остальные этапы эмбриогенеза сопровождаются специализацией клеточных пластов, отвечающих за анатомические структуры.
Сложный процесс образования мозга должен проходить под строгим контролем биохимических механизмов. Любое внешнее вмешательство нарушает внутриутробное развитие.
Основные причины возникновения лиссэнцефалии:
Внутрисемейные случаи передачи заболевания достаточно редки. Если встречается нозология у нескольких членов семьи, требуется генетическое консультирование.
Средняя распространенность нозологии первого типа – 11% на миллион новорожденных детей. Большинство ситуаций провоцируется генетическими дефектами гена LIS1. На втором месте встречается гипоплазия мозжечка из-за дефекта гена TUBA1A.
После наследственных аномалий на втором месте – вирусное инфицирование в первом триместре беременности.
Основные виды лиссенцефалии
Встречается свыше двадцати морфологических форм заболевания:
Мышечная дистрофия с олигофренией Фукуяма передается аутосомно-рецессивным способом. Наследственная миотония имеет прогрессирующее течение.
Особенности шизэнцефалии, порэнцефалии, голопрозэнцефалии
Билатеральная расщелина церебральных полушарий формируется на этапе эмбриогенеза. Морфологическая структура образования бывает разомкнутой или сомкнутой.
Односторонняя локализация патологии на МРТ снимках может напоминать кисту. Вдоль расщелины расположены патологические участки церебральной паренхимы – микрогирия, зоны повышенной повторной активности, спастические параличи.
Порэнцефалия характеризуется образованием кистозных полостей внутри церебральной паренхимы. Причины возникновения патологии – кровоизлияние внутрь головного мозга, инфаркты, инсульты. Типичная локализация кисты – сильвиева борозда.
В редких случаях порэнцефалия характеризуется образованием аномальных ходов между кистозной полостью и желудочковыми пространствами. Нозология нередко характеризуется другими стигмами дисэмбриогенеза:
У ребенка с пороком развития возникают неврологические расстройства:
Осложняют клиническую картину сопутствующие изменения:
Псевдопорэнцефалические кисты нередко имеют унилатеральное (одностороннее) расположение. Нередко сочетаются с пороками центральной нервной системы, дефектами клеточной миграции.
Шизэнцефалия на МРТ
Голопрозэнцефалия – что это такое
Заболевание возникает по причине патологического разделения химического вещества прозэнцефалона.
Классификация нозологии по степени тяжести:
Самая тяжелая – последняя форма. При ней наблюдается ряд врожденных аномалий:
На фоне множественных аномалий части лица трудно различимы. Сопутствующие пороки нейрональной миграции:
Этиологические механизмы наследственных дефектов не установлены. Голопрозэнцефалия в большинстве случаев завершается смертельным исходом, но неполная форма может приводить к инвалидности.
Симптомы лиссэнцефалии
Клинические проявления нозологии определяются сразу после рождения ребенка. Отмечаются не только генетические дефекты, но и нарушения глотания у малыша, повышенный мышечный тонус, отсталость в развитии от сверстников.
Симптомы лиссэнцефалии у ребенка 2-5 месяцев:
Вначале умственная отсталость не прослеживается. После первого года жизни наблюдаются расстройства психоречевых навыков. Дети раздражительны, тревожны, мышечная активность снижена.
При сравнении со сверстниками наблюдается значительное отставание в развитии, формировании мышечной системы, иннервации внутренних органов, малого таза.
При легком течении заболевания ребенок может дожить до подросткового возраста. Внешние аномалии ограничивают социального общения. Больные редко доживают до восемнадцати лет, но существует около двадцати разновидностей патологии. Проявления первого типа:
Определить лиссэнцефалию при отсутствии положительных результатов внутриутробного УЗИ сложно. Клиническая картина возникает после рождения. Мышечные параличи, судороги появляются сразу или на протяжении первого года.
В большинстве случаев установить диагноз лиссэнцефалии поможет ультразвуковое обследование. Врач может назначить магнитно-резонансную томографию беременной женщине и ребенку. МРТ является безвредной, но в первом триместре не проводится из-за отсутствия практической информации о влиянии магнитного поля на плод.
Первые признаки лиссэнцефалии у новорожденных
Раннее выявление нозологии помогает продлить жизнь малышу, но спасти от смерти не удается. Первые признаки у новорожденных:
На протяжении первого года жизни присоединяются другие проявления – речевые расстройства, недержание мочи, учащение дыхания и сердцебиения.
Синдром летального птеригума (Нормана-Робертса) возникает при лиссэнцефалии первого типа. К вышеописанным проявлениям присоединяется ряд проявлений:
Мозжечковая атаксия характеризуется нарушением координации. Ребенок не может удержать равновесия, поддерживать вертикальную позицию. Родители вначале обращают внимание на сложности посадки, сохранения горизонтального положения.
Диагностика лиссэнцефалии
Устанавливается диагноз сразу после рождения с помощью УЗИ, КТ и МРТ. Внутриутробно обнаружить проявления можно с 20 недели. Выявление малейших нарушений развития головного мозга плода требует дополнительной диагностики. В зависимости от степени повреждений принимается решение о возможности прерывания беременности. При подозрении на наследственные формы проводится генетическое консультирование всех членов семьи.
Поздняя верификация патологии требуется постоянного консервативного лечения. Терапия тяжелых форм проводится в стационаре под контролем квалифицированных врачей.
Основные виды диагностики лиссэнцефалии:
Самое достоверное исследование – МРТ при лиссэнцефалии у новорожденных, позволяющее определить самые мельчайшие аномалии.
Дифференциальная диагностика
Схожими клиническими признаками характеризуется ряд хромосомных аномалий – синдром Пена-Шокейра, Нунана, артрогрипоз. Генетическое консультирование верифицирует нозологии до появления клинических симптомов.
Контрактуры суставов удается диагностировать ближе к первому году, когда ребенок предпринимает попытки сидеть или ходить. Внешние проявления водянки мозги – увеличенная форма черепа, выпячивание родничков.
Прогноз и продолжительность жизни
Большинство детей не доживает до года. Если ребенку удается дожить до 3 лет, он остается инвалидом и погибает от сопутствующих инфекций, тяжелых осложнений – парезы кишечника, мочевого пузыря, конечностей, дыхательной мускулатуры.
Угнетение глотательного рефлекса обуславливает затруднения питания, что обеспечивает дефицит массы тела, приводит к снижению иммунитета.
Прогноз неблагоприятный даже при внутриутробном выявлении аномалий развития.
Звоните нам по телефону 8 (812) 241-10-46 с 7:00 до 00:00 или оставьте заявку на сайте в любое удобное время
Лиссэнцефалия у детей что это
Особенности симптоматической эпилепсии и другие неврологические нарушения у детей с лиссэнцефалией
Пороки развития головного мозга являются одной из частых причин возникновения эпилепсии в детском возрасте.
Лиссэнцефалия представляет собой кортикальную мальформацию, которая развивается в результате глобальных нарушений нейронально-глиальной миграции. В качестве вероятной ее причины рассматривается ухудшение «транспортной» функции специфических астроцитов и радиальных глиальных волокон, участвующих в миграции зародышевых клеток.
Отсутствие извилин в зрелом мозге (агирия) является морфологическим субстратом полной лиссэнцефалии, наличие лишь единичных, рудиментарных и утолщенных извилин (пахигирия) – неполной лиссэнцефалии. Клинические проявления лиссэнцефалии представлены задержкой психомоторного развития, спастической тетраплегией и резистентной эпилепсией. Возможности современной нейровизуализации и электрофизиологических методов диагностики позволяют определить роль пороков головного мозга в этиопатогенезе эпилепсии и прогнозе заболевания. Наиболее информативным методом в диагностике структурных изменений является магнитно-резонансная томография (МРТ), позволяющая прицельно изучить соотношение серого и белого вещества головного мозга, а также исключить новообразования и травмы.
По результатам некоторых эпидемиологических исследований отдельных нозологических форм кортикальных мальформаций известно, что они являются этиологическими факторами в 37,6% всех случаев эпилепсии. Резистентность к антиэпилептической терапии при наличии выявленного порока головного мозга может служить показанием к хирургическому лечению. По данным зарубежных авторов, среди пациентов с рефрактерными эпилепсиями, подвергшихся хирургическому лечению, у 30–75% детей раннего возраста причиной фармакорезистентности оказались пороки головного мозга.
Цель исследования: изучить и сопоставить клинико-электрофизиологические и нейровизуализационные результаты обследования детей с лиссэнцефалией, оценить эффективность противоэпилептической терапии и выявить частоту фармакорезистентных форм эпилепсии.
Авторами проанализированы данные анамнеза, результаты неврологического осмотра, семиотика эпилептических приступов, данные нейровизуализационных и электрофизиологических исследований 22 пациентов с лиссэнцефалией, которые проходили обследование и лечение в отделении психоневрологии Санкт-Петербургского государственного педиатрического медицинского университета в 2012–2015 гг.
При нейровизуализационном обследовании в равной степени выявлены пахигирия и агирия, с преимущественной локализацией мальформации в лобных отделах головного мозга. В подавляющем большинстве случаев при клиническом обследовании выявлено наличие моторного дефицита, когнитивных и поведенческих нарушений. Дебют эпилептических приступов достоверно чаще наблюдался в возрасте до 6 мес. Чаще отмечались эпилептические спазмы и фокальные эпилептические приступы как со вторичной генерализацией, так и без нее. Корреляция нейровизуализационных и электроэнцефалографических данных отмечалась у половины обследованных детей.
Локализация мальформации наблюдалась чаще в лобной области (n = 12; 55%), диффузная агирия выявлена у трех пациентов (14%). У части обследованных пациентов ЛЭ ассоциирована с последствиями гипоксически-ишемического поражения головного мозга (n = 5; 23%), с агенезией и (или) гипоплазией мозолистого тела (n = 2; 9%), с гипоплазией полушарий или червя мозжечка (n = 2; 18%), вентрикуломегалией (n = 6; 27%). У двух пациентов (9%) лиссэнцефалия сочеталась с полимикрогирией, фокальной корковой дисплазией и нейрональной клеточной гетеротопией.
При клиническом обследовании выявлено наличие моторного дефицита (n = 20; 91%), когнитивных и поведенческих нарушений (n = 20; 91%). У двух детей с пахигирией не выявлено отклонений в неврологическом статусе. У детей с эпилепсией (n = 20) выявлена нейровизуализационно-электроэнцефалографическая корреляция в 45% случаев (n = 9).
В терапии эпилептических приступов у пациентов с ЛЭ чаще использовались вальпроаты (100%). Реже – топирамат (30%), вигабатрин (25%), АКТГ, леветирацетам, производные карбоксамида (20%), бензодиазепины (15%), фенобарбитал (15%), бензонал (5%). Два пациента терапию не получали в связи с отсутствием приступов.
В период лечения и при контрольном обследовании 20 больных с эпилепсией наблюдались положительные результаты в виде ремиссии (n = 2; 10%), урежения эпилептических приступов на 50–75% (n = 10; 50%), положительной динамикой на ЭЭГ (n = 2; 10%).
Таким образом, в терапии эпилептических приступов у пациентов преобладали препараты вальпроевой кислоты. Результаты проведенного исследования свидетельствуют о том, что одной из частых причин тяжелых форм эпилепсии являются пороки развития головного мозга, поэтому их ранняя диагностика, адекватное консервативное и хирургическое лечение способствуют снижению частоты формирования фармакорезистентности эпилепсии и инвалидизации больных.
Лиссэнцефалия
Лиссэнцефалия – группа генетически обусловленных аномалий развития головного мозга, характеризующихся частичным или полным недоразвитием извилин и борозд коры больших полушарий, а также нарушением ее ультраструктуры. Выраженность и сочетания симптомов этого состояния различаются при разных формах заболевания, наиболее распространены судороги, глубокая умственная отсталость, нарушения глотания и гипотония мышц. Диагностика лиссэнцефалии может производиться ультразвуковыми методиками (в том числе и пренатально), компьютерной и магнитно-резонансной томографией, для наиболее распространенных форм возможно определение посредством молекулярно-генетического анализа. Специфического лечения не существует, используют симптоматическую и поддерживающую терапию.
Общие сведения
Лиссэнцефалия – группа тяжелых аномалий развития головного мозга, которые сопровождаются недоразвитием коры больших полушарий с формированием пахигирии (наличием всего нескольких извилин и борозд) или агирии (полным отсутствием складчатости коры). Данная патология может выступать в качестве самостоятельного генетического заболевания или входить в симптомокомплекс других синдромов – например, Миллера-Дикера, Фукуямы и Уокера-Варбурга. Механизм наследования различных типов лиссэнцефалии может быть аутосомно-рецессивным, аутосомно-доминантным (в данном случае чаще всего имеют место спонтанные или герминативные мутации) и сцепленным с Х-хромосомой. Из-за многообразия механизмов наследования половое распределение нарушения неодинаково при различных формах патологии. Лиссэнцефалия является достаточно редкой генетической аномалией развития мозга, поэтому встречаемость определена только для наиболее распространенной первой группы нарушений – она составляет 11,7 случаев на 1 000 000 новорожденных. Для остальных групп лиссэнцефалии встречаемость не установлена, в том числе и потому, что во многих случаях плод с подобной патологией не вынашивается, и беременность самопроизвольно прерывается в первом триместре еще до определения наличия порока.
Причины лиссэнцефалии
Основная общая причина всех типов лиссэнцефалии – нарушение процесса миграции клеток-предшественников нейронов (нейробластов) из передних отделов нервной трубки к будущей коре больших полушарий. В результате этого вместо сложной складчатой структуры, которая имеет в своем составе шесть слоев, образуется гладкая или имеющая в разы меньше борозд кора, состоящая из 2-4 слоев (в зависимости от формы заболевания). Поскольку кора больших полушарий у человека отвечает за когнитивные функции, в ней содержится огромное число нервных центров и обширные ассоциативные зоны, лиссэнцефалия приводит к тяжелейшим расстройствам. Кроме того, при некоторых типах мутаций, вызывающих данное состояние, возможно развитие аномалий других органов и тканей, что еще больше усугубляет состояние больного.
Наиболее распространенные типы лиссэнцефалии обусловлены дефектами гена PAFAH1B1, также известного под названием LIS1 и расположенного на 17-й хромосоме. Многие врачи-генетики отмечают, что для возникновения выраженного недоразвития коры головного мозга и синдрома Миллера-Дикера необходимы не точечные мутации в LIS1, а крупные делеции с захватом сотен пар азотистых оснований. Нередко при этом повреждаются и окружающие гены, что становится причиной разнообразных фенотипических проявлений данного типа лиссэнцефалии. Ген LIS1 кодирует внутриклеточную субъединицу сложного по своей структуре фермента, который принимает активное участие в миграции нейробластов. Дефекты в структуре этой субъединицы приводят к нарушению данного процесса и развитию данного заболевания.
Другая форма лиссэнцефалии обусловлена мутацией гена DCX, локализованного на Х-хромосоме, поэтому наследование этого типа патологии сцеплено с полом. Белок, получаемый в результате экспрессии данного гена, участвует в формировании особого типа микротрубочек, которые вырабатываются только нейробластами и необходимы им для формирования связей между клетками. Нарушения в структуре DCX приводят к синтезу дефектного белка, что провоцирует лиссэнцефалию. Другой относительно изученный вариант этого состояния, также сцепленный с Х-хромосомой, вызывается мутациями гена ARX, который является фактором транскрипции для иных генов. Он контролирует развитие коры больших полушарий, поджелудочной железы и половых органов, из-за чего дефекты ARX проявляются многочисленными пороками данных органов, в том числе лиссэнцефалией.
Еще одним распространенным вариантом лиссэнцефалии является форма заболевания, обусловленная мутацией гена RELN, расположенного на 7-й хромосоме. Дефекты этого гена приводят к так называемому синдрому Норман-Робертса, который, помимо прочего, сопровождается выраженным нарушением складчатости коры больших полушарий. Ген RELN кодирует последовательность гликопротеида рилина, который принимает активное участие в формировании нервной ткани, а также контролирует образование новых дендритов и функционирование долговременной памяти у взрослых людей. Удалось идентифицировать еще один ген, приводящий к развитию лиссэнцефалии – TUBA1A, который локализован на 12-й хромосоме. Он кодирует определенный компонент цитоскелета нейронов, его дефект приводит к неполноценности нейробластов, что нарушает процесс их миграции в эмбриональном периоде.
Классификация лиссэнцефалии
На сегодняшний день выявлено более двадцати вариантов лиссэнцефалии. Эти варианты обусловлены различными мутациями, имеют отличия в фенотипических проявлениях заболевания, разные механизмы наследования и тяжесть симптомов. Долгое время разновидности патологии не удавалось успешно классифицировать из-за значительного разнообразия генетических дефектов и недостаточных данных о ключевых генах, приводящих к развитию некоторых форм заболевания. Лишь в 2003-м году удалось создать достаточно приемлемую с точки зрения современной генетики и неврологии классификацию лиссэнцефалии, которая учитывает основные нюансы этого состояния. Специалисты разделяют все формы лиссэнцефалии на пять классов:
Данная классификация критикуется некоторыми исследователями по причине наличия большого количества «белых пятен» в виде включения в нее форм лиссэнцефалии с неопределенными ключевыми генами. Однако в настоящее время именно это разделение считается наиболее общепринятым в научном мире. Классификация корректируется по мере дальнейшего изучения данного состояния.
Симптомы лиссэнцефалии
Основными проявлениями лиссэнцефалии являются мышечная слабость, выявляемая уже при рождении, частые расстройства глотания и сосания, судорожные припадки, сильное отставание в физическом и умственном развитии. Выраженность тех или иных проявлений заболевания зависит от наличия пороков развития как головного мозга, так и других органов и систем, а также от степени недоразвития коры. Наиболее тяжелые формы патологии наблюдаются при наличии полной агирии. Иногда больные лиссэнцефалией могут доживать до подросткового и даже взрослого возраста, глубокое недоразвитие центральной нервной системы сохраняется в течение всей жизни. Некоторые пациенты проживают жизнь на грани вегетативного состояния. Летальный исход при лиссэнцефалии наступает из-за осложнений, обусловленных пороками других органов и систем, а также из-за вторичных пневмоний, сердечно-сосудистых и иных аномалий.
Диагностика и лечение лиссэнцефалии
В отношении лиссэнцефалии возможна пренатальная диагностика при помощи ультразвуковых методов исследования, при этом увеличение разрешающей способности УЗИ-аппаратуры способствует все более раннему определению заболевания. Развитие нарушений в строении коры больших полушарий происходит на 14-20-й неделе гестации, в настоящее время уже в этот период можно определить патологию и поставить вопрос о прерывании беременности. После рождения ребенка с подозрением на лиссэнцефалию диагноз подтверждают при помощи КТ и МРТ. Молекулярно-генетическая диагностика обладает высокой точностью, но она доступна только в отношении тех форм заболевания, для которых известны ключевые гены. Специфического лечения лиссэнцефалии не существует, применяют противосудорожные препараты, ноотропы и другие средства, позволяющие уменьшить выраженность симптоматики. При наличии иных пороков развития производится их коррекция по медицинским показаниям.
Прогноз и профилактика лиссэнцефалии
Прогноз практически любой формы лиссэнцефалии крайне неблагоприятный, большинство больных умирает в раннем детстве от осложнений и других пороков развития. Описаны отдельные легкие случаи этого состояния с частичным или очаговым недоразвитием коры больших полушарий, но не все специалисты склонны причислять такие типы патологии к лиссэнцефалиям. Профилактика возможна только в рамках пренатальной диагностики. При наличии в роду подобных заболеваний имеет смысл провести генетический анализ на носительство генов аутосомно-рецессивных типов патологии. При обнаружении у плода нарушений формирования мозга, соответствующих лиссэнцефалии, ставится вопрос о прерывании беременности.