мелиоидоз это что за болезнь
Мелиоидоз
Что провоцирует / Причины Мелиоидоза:
В эндемичных по мелиоидозу регионах основным резервуаром возбудителя в природе являются почва и вода, загрязненные выделениями инфицированных животных. В этих районах возбудитель может быть выделен из почвы, стоячих водоемов, прудов, рисовых плантаций. Животные выделяют возбудителя с мочой и испражнениями, сами инфицируются при употреблении кормов и воды. Мелиоидозная инфекция может наблюдаться у многих видов животных: крыс, мышевидных грызунов, кроликов, коров, собак, кошек, кенгуру и др. Членистоногие не участвуют в передаче инфекции. В эндемичных районах мелиоидоз распространен широко, о чем свидетельствует тот факт, что у 7-10% взрослого населения этих районов обнаруживают антитела к возбудителю мелиоидоза. Заражение человека может наступать при употреблении инфицированной пищи или воды, а также аэрогенным путем (воздушно-пылевым). Часто инфицирование наступает при загрязнении мелких повреждений кожи почвой. Заражение человека от человека наблюдается крайне редко. Описан случай половой передачи инфекции больным хроническим простатитом (в секрете предстательной железы выявлен возбудитель мелиоидоза) супруге, которая никогда не была в эндемичных районах. Выявлено заболевание медицинской сестры, которая не была в эндемичных районах, но работала в палатах для больных мелиоидозом. Это указывает на возможность внутрибольничной инфекции лиц с ослабленным иммунитетом.
Патогенез (что происходит?) во время Мелиоидоза:
Симптомы Мелиоидоза:
Инкубационный период мелоидоза продолжается всего 2-3 дня (по данным лабораторных заражений со времени повреждения кожи и до развития болезни). Основные клинические формы:
1) септическая (острая, подострая, хроническая);
2) легочная (инфильтративная, абсцедирующая);
3) рецидивирующая;
4) латентная.
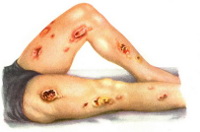
Септическая форма. У отдельных больных эта форма начинается относительно постепенно. Вначале появляется воспалительный инфильтрат на месте внедрения возбудителя (повреждения кожи), развивается регионарный лимфаденит, повышается температура тела и довольно скоро болезнь приобретает септическое течение. У большинства же больных септическая форма начинается внезапно с озноба, высокой лихорадки, резкой головной боли, одышки. В некоторых случаях заболевание протекает бурно, и больной умирает от инфекционно-токсического шока через 2-4 дня до развития у него вторичных септических очагов (молниеносная форма). В других случаях первичным очагом являются воспалительные изменения в легких, из которых затем гематогенно инфекция распространяется по различным органам и системам. Появляется общая слабость, температура с ознобом повышается до 39°С и выше, больного беспокоит кашель, боли в груди плеврального характера, выявляется притупление перкуторного звука, над пораженными отделами легких выслушиваются влажные хрипы. Процесс чаще локализуется в верхних долях. Затем тяжесть течения нарастает. Появляются множественные пустулы на коже и абсцессы в мышцах и внутренних органах. Болезнь продолжается 8-12 дней.
Очень быстрое развитие септической инфекции наблюдается у ослабленных лиц (наркоманы, диабетики, больные алкоголизмом и др.). В этих случаях быстро нарастают лихорадка и признаки общей интоксикации. Одновременно появляются признаки поражения легких и множественные поражения других органов. Отмечается фарингит, пустулезная сыпь по всему телу, жидкий водянистый стул, выраженная одышка, цианоз. У части больных появляются гнойные артриты, менингит, нарушение сознания. При рентгенографии легких отмечаются узелковые затенения диаметром около 10 мм, склонные к слиянию в более крупные инфильтраты. Эти формы болезни обычно не поддаются терапии.
При подострых и хронических формах мелоидоза отмечается более длительное течение с образованием вяло текущих абсцессов в различных органах и тканях. Эти формы периодически дают ремиссии, однако без этиотропной терапии больные также умирают в течение месяца (подострые формы) или через несколько месяцев (хронические формы).
Рецидивирующий мелиоидоз. Возбудитель мелиоидоза может длительно сохраняться в организме в виде латентной инфекции. Активизация латентной инфекции может проявляться в виде острого септического или легочного заболевания или в виде хронического локализованного гнойного заболевания. Рецидив развивается через длительное время после первичного инфицирования. Описан случай рецидива через 26 лет после заражения. Рецидив может быть спровоцирован хирургическим вмешательством, тяжелой гриппозной пневмонией, лучевой терапией и пр. Необходимо учитывать активизацию латентной мелиоидозной инфекции у больных СПИДом.
Диагностика Мелиоидоза:
Диагноз ставится комплексно, учитываются эпизоотические данные, клинические признаки, патологоанатомические изменения и результаты бактериологических исследований. Для выделения чистой культуры делают высевы из патматериала на МПА, МПБ, МПЖ. Биопробу ставят, вводя материал морским свинкам под кожу (самцам можно в брюшную полость), животные погибают на 10-20-й день (у самцов развивается орхит и перитонит, при подкожном введении – язва на месте инъекции).
Клинический диагноз септических форм мелиоидоза не представляет больших трудностей. Имеет значение пребывание в эндемичной местности, тяжелое течение болезни, прогрессирующая дыхательная недостаточность, множественные пустулезные элементы на коже, множественные абсцессы в подкожной клетчатке, мышцах и внутренних органах.
Пневмонические формы мелиоидоза можно диагностировать на основании эпидемиологических предпосылок, подострого течения пневмонии с поражением верхних долей, с ранним образованием тонкостенных полостей, кашля с гнойной или кровянистой мокротой, похудания, неправильной лихорадки с периодически возникающими ознобами.
Из лабораторных методов используют выделение возбудителей (из крови, гноя абсцессов, мокроты). Используют серологические реакции. РСК со специфическим антигеном считается диагностической уже в титре 1:8 и выше. Отрицательная РСК не исключает возможности мелиоидоза. Более чувствительна реакция гемагглютинации, которая рано становится положительной в титрах 1:16-1:64.
Дифференцируют от сапа, туберкулеза легких, глубоких микозов.
Лечение Мелиоидоза:
Прогноз. До введения в практику антибиотиков смертность при септических формах приближалась к 100%, при современных методах лечения при септических формах умирает около 50% и более. При других формах мелиоидоза прогноз более благоприятный. Вероятность отдаленных рецидивов около 20%.
Профилактика Мелиоидоза:
Специфическая профилактика не разработана. Больные мелиоидозом подлежат изоляции и госпитализации. В эндемичной местности проводят мероприятия по уничтожению грызунов и защите от них продуктов. Запрещается употребление сырой воды и купание в стоячих водоемах.
При подозрении на мелиоидоз больных животных изолируют и исследуют бактериологически. В неблагополучном хозяйстве проводят дезинфекцию, дератизацию и дезинсекцию. Убой на мясо больных и подозрительных по заболеванию животных запрещают.
К каким докторам следует обращаться если у Вас Мелиоидоз :
Мелиоидоз
Мелиоидоз относится к острым инфекционным заболеваниям, характеризующимся септическим течением, сопровождаемым образованием множественных очагов абсцесса в различных органах.
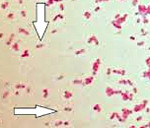
Возбудителем мелиоидоза является неустойчивая к воздействию высокой температуры и дезинфицирующих препаратов грамотрицательная палочка Pseudomonas pseudomallei, иначе бацилла Уитмора. Возбудителей инфекции распространяют животные – мыши, крысы, собаки, кошки, свиньи, коровы, лошади, овцы, козы. В регионах эндемичных по мелиоидозу бациллу Уитмора находят в стоячих водоемах, в почве, там, где испражнялись больные животные. Поврежденная кожа или слизистые оболочки прокладывают тот путь, по которому инфекция может проникать в организм человека.
Симптомы мелиоидоза
Симптомы мелиоидоза в зависимости от формы течения заболевания могут быть различными. При септической форме это появление инфильтрата в зоне поражения кожи, региональный лимфаденит, лихорадочное состояние, признаки общей интоксикации. При легочном течении заболевания появляется кашель с гнойной и кровянистой мокротой, боли в груди, нарастающая слабость, потеря веса, озноб. Важным фактором для своевременной постановки диагноза имеет информация о пребывании пациента в эндемичном по мелиоидозу регионе.
Лечение мелиоидоза
Лечение мелиоидоза нашими специалистами проводится адекватно форме течения заболевания и предваряется тщательными лабораторными обследованиями, которые дают необходимую информацию. На основании полученных данных опытный врач устанавливает точный диагноз, исключая схожие по своим проявлениям заболевания другой природы и степени тяжести. Лечение длительное. Своевременно начатые терапевтические процедуры и мероприятия обеспечивают продуктивность лечения мелиоидоза.
Консультация и прием врача
Более подробную информацию Вы можете узнать по телефонам указанным на сайте или обратиться в наш Медицинский Центр. Мы работаем Без Выходных с 8.00 до 22.00 по адресу: г.Москва ВАО (Восточный Административный Округ) Сиреневый Бульвар 32А
Мелиоидоз
(Болезнь Уитмора)
, MD, FACP, Charles E. Schmidt College of Medicine, Florida Atlantic University;
, MD, FACP, Wellington Regional Medical Center
Возбудитель Burkholderia pseudomallei может быть выявлен в почве и воде и является эндемичным для Юго-Восточной Азии, Австралии, Центральной, Западной и Восточной Африки, Индии, Среднего Востока и Китая.
Люди могут заразиться мелиоидозом путем инфицирования ранок на коже или ожогов, при приеме пищи или при попадании в дыхательные пути, но не прямо от зараженных животных или других людей.
В эндемичных районах мелиоидоз чаще возникает у пациентов с:
Иммунной недостаточностью, включая СПИД СПИД Инфекция вирусом иммунодефицита человека (ВИЧ) вызывается одним из 2 похожих ретровирусов (ВИЧ-1 и ВИЧ-2), которые разрушают CD4+ лимфоциты и ослабляют клеточный иммунитет, увеличивая риск оппортунистических. Прочитайте дополнительные сведения
Симптомы и признаки мелиоидоза
Мелиоидоз может проявляться остро или оставаться латентным в течение многих лет после бессимптомного первичного инфицирования. Смертность 10%, за исключением острого септицемического мелиоидоза, который является часто смертельным.
Острая легочная инфекция наиболее распространенная форма. Она варьирует от легкой формы до некротизирующей пневмонии. Начало может быть острым или постепенным, с головной болью, анорексией, плевритными болями или тупой болью в области грудной клетки и генерализованной миалгией. Лихорадка обычно > 39 ° C. Кашель, тахипноэ и хрипы являются характерными признаками. Мокрота может быть с вкраплениями крови. Рентген грудной клетки обычно показывает уплотнение верхней доли, часто кавитирующее и напоминающее туберкулез. Узелковые поражения, тонкостенные кисты и плевральный выпот могут также иметь место. Количество лейкоцитов в крови – от нормы до 20 000/мкл (20 × 10 9 /л).
Острая септицемическая инфекция начинается внезапно, с септического шока Сепсис и септический шок Сепсис представляет собой клинический синдром с развитием жизнеугрожающей органной дисфункции, вызванный нарушением регуляции ответа на инфекцию. При септическом шоке происходит критическое. Прочитайте дополнительные сведения и поражения многих органов, проявляющихся дезориентацией, тяжелой одышкой, сильной головной болью, фарингитом, болями в верхней части брюшной полости, диареей и пустулами на коже. Отмечаются высокая температура, гипотония, тахипноэ, яркий эритематозный румянец и цианоз. Могут быть выраженные миалгии. Иногда появляются симптомы артрита или менингита. Респираторные симптомы могут отсутствовать или выслушиваются хрипы и шум трения плевры.
Локализованная гнойная инфекция может возникать практически в любом органе, но чаще всего встречается в месте проникновения в кожу (или легкие) и регионарных лимфатических узлах. Типичные метастатические места инфекции включают печень, селезенку, почки, простату, кости и скелетные мышцы. Острый гнойный паротит распространен среди детей в Таиланде. У пациентов может не быть лихорадки.
Диагностика мелиоидоза
Окрашивание и посев
B. pseudomallei может быть выявлен в эксудате благодаря окрашиванию метиленовым синим или по Граму, а также посеву. Посевы крови часто отрицательны, за исключением случаев с бактериемией (например, при септицемии). Серологические анализы зачастую ненадежны в эндемичных районах, потому что результаты могут быть положительными из-за перенесенной инфекции.
Рентген-обследование ОГП, как правило, показывает узловые (4-10 мм) уплотнения, неправильной формы, но также может показать лобарные инфильтраты, двустороннюю бронхопневмонию или полостные поражения.
УЗИ или КТ брюшной полости и малого таза, вероятно, следует сделать для обнаружения абсцессов, которые могут присутствовать, независимо от клинической картины. Печень и селезенка могут пальпироваться. Показатели печеночных тестов, уровни аспартатаминотрансферазы и билирубина часто патологические. Почечная недостаточность и коагулопатии возникают в тяжелых случаях. Количество лейкоцитов в крови в норме или немного увеличено.
Лечение мелиоидоза
Пациентам с наличием симптомов назначают внутривенные антибиотики на протяжении нескольких недель с последующим длительным применением пероральной формы препарата.
Бессимптомный мелиоидоз не нуждается в каком-либо лечении.
Пациентам с наличием симптомов следует назначать цефтазидим по 30 мг/кг внутривенно каждые 6 часов в течение 2–4 недель (имипенем, меропенем и пиперациллин являются приемлемыми препаратами замены), затем антибиотики перорально (одну двойную таблетку триметоприма/сульфометоксазола [ТМП/СМК] 2 раза в день или доксициклин в дозе 100 мг 2 раза в день) в течение 3–6 месяцев. Детям
Ключевые моменты относительно мелиоидоза
Мелоидозом можно инфицироваться контактным путем через кожу, при проглатывании или вдыхании; им не заражаются непосредственно от инфицированных животных или людей.
Наиболее распространенным проявлением является острая легочная инфекция (иногда тяжелая), но гнойные поражения могут возникать на коже и/или во многих других органах; может возникать сепсис, который ведет к высокой смертности.
Диагноз устанавливают с помощью окрашивания и посева; посевы крови выполняются, но часто отрицательны, кроме случаев тяжелой септицемии.
Лечение пациентов, у которых присутствуют симптомы, проводят с помощью внутривенного введения цефтазидима с последующим длительным курсом перорального ТМП/СМК или доксициклина; у детей
Мелиоидоз
Мелиоидоз – бактериальная инфекция, вызываемая бациллой Уитмора и протекающая с образованием множественных септико-некротических очагов во внутренних органах и тканях. Клиническое течение мелиоидоза характеризуется лихорадкой с ознобом, кашлем с гнойной мокротой, болью в грудной клетке, лимфаденитом, рвотой, диареей. Типично развитие гнойно-воспалительных процессов в различных органах (абсцессов легкого, эмпиемы плевры, артрита, пиелонефрита, остеомиелита и др.). Подтвердить диагноз мелиоидоза позволяет бактериологическое исследование крови, мочи, мокроты, гноя; серологические методы. Для этиотропной терапии используются антибиотики препараты тетрациклинового ряда, левомицетин, сульфаниламиды.
Общие сведения
Мелиоидоз (ложный сап, пневмоэнтерит, псевдохолера, болезнь Уитмора) – инфекционное заболевание из группы сапронозов, характеризующееся острой или хронической септикопиемией. Мелиоидоз регистрируется в Юго-Восточной Азии, Индонезии, Австралии, Западной и Восточной Африке, Центральной и Южной Америке. В Европе и США встречаются завозные случаи мелиоидоза. В эндемичных регионах антитела к возбудителю мелиоидоза обнаруживаются у 7-10% местного населения, что свидетельствует о широком распространении инфекции. Мелиоидоз может протекать в латентной, септической, легочной и рецидивирующей форме. Без своевременного этиотропного лечения летальность от заболевания близка к 100%.
Причины мелиоидоза
Инфекция вызывается грамотрицательной палочкой Burkholderia pseudomallei (Pseudomonas pseudomallei, бациллой Уитмора), которая по своим морфологическим и культуральным свойствам близка к возбудителю сапа. Бактерия является факультативным аэробом; подвижна благодаря наличию жгутикового аппарата; имеет длину 2-6 мкм и ширину 0,5-1 мкм. Во внешней среде (воде, влажной почве, гниющих материалах) возбудитель мелиоидоза способен длительно сохранять свою патогенность, однако быстро гибнет при нагревании и воздействии дезинфектантов.
Главными природными резервуарами палочки мелиоидоза служат вода и почва, загрязненные выделениями инфицированных животных. В естественных условиях носителями бациллы являются домашние и дикие животные (кошки, собаки, свиньи, коровы, лошади, козы, овцы, крысы, кенгуру, кролики), среди которых также отмечаются спорадические случаи мелиоидозной инфекции. Человек может заразиться мелиоидозом алиментарным путем при употреблении инфицированной воды и пищи; аэрогенным (воздушно-пылевым) путем при вдыхании бацилл с частицами пыли; контактным путем в случае попадания контаминированного материала на поврежденную кожу. Известны отдельные случаи передачи возбудителя половым путем от больного мелиоидозным простатитом, а также внутрибольничного инфицирования медперсонала при уходе за больными мелиоидозом. Максимальный подъем заболеваемости регистрируется в сельскохозяйственных районах в сезон дождей, а также в периоды войн и стихийных бедствий. Мелиоидоз обычно протекает в виде групповых вспышек и спорадических случаев. 98 % заболевших составляют мужчины.
Преодолев входные ворота, возбудитель мелиоидоза размножается в регионарных лимфатических узлах. Септическая форма инфекции сопровождается выходом бактерий в кровь и гематогенным распространением по организму с образованием множественных гранулем с казеозным некрозом и абсцессов. В большинстве случаев гнойные очаги возникают в легких; в тяжелых случаях – практически во всех органах и тканях (коже, подкожной клетчатке, лимфоузлах, костях, печени, почках, селезенке, головном мозге и мозговых оболочках). Септический вариант мелиоидоза развивается у ослабленных пациентов, больных хроническим гепатитом, сахарным диабетом, туберкулезом, алкоголизмом, наркозависимых (устаревшее название заболевания – «септицемия морфинистов»). У лиц с хорошей иммунной реактивностью обычно возникает легочная форма мелиоидоза, для которой свойственны только абсцессы легких. Описаны случаи латентно протекающей инфекции. Постинфекционный иммунитет длительный, возможно пожизненный.
Симптомы мелиоидоза
Продолжительность инкубационного периода при мелиоидозе может составлять от 2-х до 12-24 дней (иногда до нескольких месяцев). Различают латентную, септическую (молниеносную, острую, подострую, хроническую), легочную (инфильтративную, абсцедирующую) и рецидивирующую форму мелиоидоза. При латентном течении явные симптомы заболевания отсутствуют; инфекция выявляется ретроспективно, при проведении серологического обследования местного населения или лиц, вернувшихся из эндемичных регионов. В случае активизации латентной инфекции может развиваться рецидивирующий мелиоидоз, протекающий по септическому или легочному варианту.
Септическая форма мелиоидоза может носить молниеносное, острое, подострое и хроническое течение. При молниеносном варианте симптоматика развивается бурно: в считанные часы температура прогрессирует до 41°С, возникает рвота, профузный понос, эксикоз. Нарастает одышка, сердечно-сосудистая недостаточность; развивается гепатоспленомегалия и желтуха. На фоне выраженной интоксикации могут возникнуть менингеальные симптомы, нарушение сознания, возбуждение или, напротив, угнетение ЦНС, бред. Гибель пациента от инфекционно-токсического шока наступает на вторые сутки. Течение молниеносной формы мелиоидоза напоминает клинику холеры или септической формы чумы.
Острый мелиоидоз манифестирует с высокой лихорадки и потрясающего озноба. На этом фоне беспокоят сильные головные, суставные и мышечные боли, рвота, диарейный синдром. Одновременно появляется кашель со слизисто гнойной мокротой, боли в груди, кровохарканье, шейный и подмышечный лимфаденит, часто возникает пневмония. На 5-6 е сутки на коже возникает эритема, пустулы или геморрагические пузырьки. В целом клиническая картина острого мелиоидоза соответствует тяжелому течению сепсиса; продолжительность острой фазы составляет 10–15 дней.
Подострое течение мелиоидоза характеризуется картиной септикопиемии с образованием абсцессов в легких, развитием эмпиемы плевры, гнойного перикардита, гнойного артрита, остеомиелита, перитонита, пиелонефрита, цистита, менингоэнцефалита. Интоксикационный и лихорадочный синдромы выражены умеренно. Без этиотропной терапии больные подострой формой мелиоидоза погибают в течение месяца. Хронический мелиоидоз может длиться несколько лет с периодическими с обострениями и ремиссиями. Для этой формы характерна нормальная или субфебрильная температура, абсцессы в подкожной клетчатке с длительно незаживающими свищевыми ходами, абсцессы внутренних органов. Гибель пациентов наступает от кахексии, амилоидоза, вторичной бактериальной инфекции.
Легочная форма мелиоидоза протекает в виде абсцедирующей пневмонии или гнойного плеврита. При этом отмечается интермиттирующая лихорадка с ознобом и потами, кашель с густой зеленовато желтой мокротой, боли в грудной клетке, снижение массы тела. На рентгенограммах легких обнаруживаются крупные полости в верхних долях, напоминающие картину туберкулеза легких.
Диагностика и лечение мелиоидоза
Вне эпидемических очагов диагностика мелиоидоза затруднена. Это объясняется полиморфизмом клинических проявлений, низкой настороженностью специалистов (инфекционистов, пульмонологов, хирургов и др.) в отношении возможных завозных случаев мелиоидоза. Поэтому у больных с неясной лихорадкой и септикопиемией всегда следует выяснять информацию о пребывании в эндемичных по мелиоидозу районах. Лабораторное подтверждение диагноза осуществляется с помощью бактериологического посева крови, мочи, мокроты, экссудатов, содержимого абсцессов и др. на питательные среды. Для экспресс-диагностики и быстрой идентификации возбудителя используется люминесцентная микроскопия. Из серологических методов наибольшей ценностью обладают РСК и РНГА. Возможно проведение биологической пробы – в этом случае у зараженных лабораторных животных возбудители мелиоидоза обнаруживаются в перитонеальном экссудате. В рамках дифференциально-диагностического поиска исключается сап, чума, холера, оспа, брюшной тиф, сепсис, третичный сифилис, туберкулез, системные микозы, дизентерийные абсцессы печени.
Комплексное лечение мелиоидоза складывается из этиотропной антибактериальной терапии, патогенетического и симптоматического лечения и хирургического дренирования абсцессов. Антибиотикотерапия при мелиоидозе проводится длительно (1-2 месяца и дольше). Наибольшую специфическую противомикробную активность показали хлорамфеникол, тетрациклины, цефалоспорины, сульфаниламиды пролонгированного действия и др. При септической форме мелиоидоза одновременно назначается сразу несколько антибактериальных препаратов; антибиотики вводятся парентерально, большими дозами (3-4 г в сутки). При необходимости проводится дренирование плевральной полости, вскрытие абсцессов мягких тканей, чрескожное или открытое дренирование абсцессов внутренних органов.
Прогноз и профилактика мелиоидоза
Без лечения летальность при мелиоидозе составляет 95-100%. При проведении полноценной антибиотикотерапии заболевание излечимо, однако примерно в 20% случаев возникают отдаленные рецидивы. Профилактика мелиоидоза заключается в обеспечении защиты источников водоснабжения и продуктов питания от грызунов, проведении дератизационных мероприятий, лечении или забое инфицированных домашних животных, повышении общегигиенической культуры населения в неблагополучных по мелиоидозу местностях. При выявлении мелиоидоза больные изолируются, все их выделения подлежат дезинфекции; за реконвалесцентами устанавливается длительное наблюдение. Специфическая профилактика мелиоидоза на настоящий момент не разработана.
СИСТЕМНЫЙ АМИЛОИДОЗ: диагноз, дифференциальный диагноз, лечение
«Амилоидоз» — термин, объединяющий группу заболеваний, которые отличаются большим разнообразием клинических проявлений и характеризуются внеклеточным отложением нерастворимых патологических фибриллярных белков в органах и тканях. Впервые эта патология бы
«Амилоидоз» — термин, объединяющий группу заболеваний, которые отличаются большим разнообразием клинических проявлений и характеризуются внеклеточным отложением нерастворимых патологических фибриллярных белков в органах и тканях. Впервые эта патология была описана в XVII в. Боне — саговая селезенка у больного с абсцессом печени. В середине XIX в. Вирхов применил ботанический термин «амилоид» (от греч. amylon — крахмал) для описания внеклеточного материала, обнаруженного в печени при аутопсии, так как полагал, что он близок по структуре к крахмалу. Впоследствии была установлена белковая природа отложений, однако термин «амилоид» сохранился до настоящего времени.
В 20-е гг. XX столетия Бенхольд предложил окрашивать амилоид конго-красным, затем был обнаружен эффект двойного лучепреломления в поляризованном свете — изменение кирпично-красной окраски на яблочно-зеленую. В 1959 г. Коген и Калкинс с помощью электронной микроскопии установили фибриллярную структуру амилоида.
Эволюцию претерпели и клинические представления об амилоидозе: Рокитанский в 1842 г. установил связь «сальной болезни» с туберкулезом, сифилисом, риккетсиозами; Уилкс в 1856 г. описал «жирные органы» у больного, не имевшего никаких сопутствующих заболеваний; Аткинсон в 1937 г. обнаружил амилоидоз у пациентов с миеломной болезнью. Выделены были старческие (Сойка, 1876) и наследственные (Андраде, 1952) формы заболевания, амилоидоз разделяли на генетический, первичный и вторичный, и, наконец, в 1993 г. была принята классификация ВОЗ, построенная на специфичности основного фибриллярного белка амилоида.
В нашей стране большой вклад в развитие представлений об амилоидозе внесли Е. М. Тареев, И. Е. Тареева, В. В. Серов. Огромная роль в изучении первичного и генетических вариантов амилоидоза и периодической болезни принадлежит О. М. Виноградовой, чьи монографии, изданные в 1973 и 1980 гг., не утратили своей актуальности и в наши дни.
В настоящее время амилоидоз принято клинически разделять на системные и локальные формы. Среди системных форм, в зависимости от состава фибриллярных отложений, выделяют четыре типа (табл. 1).
К локальным формам амилоидоза в настоящее время относят болезнь Альцгеймера (A-бета, фибриллы состоят из β-протеина, откладывающегося в головном мозге), амилоидоз островков поджелудочной железы, возможно, имеющий патогенетическую связь с диабетом 2 типа, амилоидоз, возникающий в эндокринных опухолях, амилоидные опухоли кожи, назофарингеальной области, мочевого пузыря и другие редкие виды.
AL-амилоидоз
Развитие AL-амилоидоза возможно при миеломной болезни, болезни Вальденстрема, В-клеточных лимфомах, и оно может быть идиопатическим при первичном амилоидозе. Все эти варианты объединены общим патогенезом, первичный амилоидоз представляет наибольшую трудность для распознавания в связи с отсутствием явных признаков гематологического заболевания, поэтому именно на данной форме стоит остановиться подробно.
При первичном амилоидозе, доброкачественной плазмоклеточной дискразии, родственной множественной миеломе, аномальные клоны плазматических клеток костного мозга продуцируют амилоидогенные иммуноглобулины. Некоторые аминокислоты в вариабельных участках легких цепей этих иммуноглобулинов занимают необычную позицию, что приводит к их нестабильности и обусловливает склонность к фибриллогенезу. У больных с первичным амилоидозом содержание плазматических клеток в костном мозге повышено до 5—10% (в норме их менее 4%, при миеломной болезни — более 12%), и они продуцируют определенный изотип легких цепей иммуноглобулинов, преобладающий при иммуногистохимическом окрашивании. Свободные моноклональные легкие цепи преобладающего лямбда- или (реже) каппа-изотипа определяются в крови и в моче, но содержание их ниже, чем при миеломной болезни.
Клиническая картина первичного амилоидоза многообразна и определяется преимущественным вовлечением в патологический процесс тех или иных органов — сердца, почек, нервной системы, желудочно-кишечного тракта, печени и др. Первыми симптомами являются слабость и потеря веса, но на этой стадии, до появления органных симптомов, диагноз устанавливается крайне редко.
Органами-мишенями при AL-амилоидозе чаще всего становятся почки и сердце. Поражение почек проявляется нефротическим синдромом, персистирующим и при наступлении ХПН, гематурия и артериальная гипертензия не характерны.
При отложении амилоида в миокарде развиваются разнообразные нарушения ритма, прогрессирующая сердечная недостаточность, чему могут предшествовать бессимптомные изменения на ЭКГ в виде снижения вольтажа зубцов. Эхокардиографическое исследование выявляет концентрическое утолщение стенок левого и правого желудочков, уменьшение объема полостей сердца, умеренное снижение фракции выброса, диастолическую дисфункцию миокарда левого желудочка.
Часто отмечаются симптомы вовлечения нервной системы — вегетативной, в виде ортостатической гипотензии, и периферической — в виде расстройств чувствительности. В последние годы стали описывать также поражения ЦНС, хотя ранее считалось, что они не характерны для первичного амилоидоза.
Диспептические явления (ощущение переполнения, запоры, поносы) и синдром нарушенного всасывания могут быть обусловлены как поражением вегетативной нервной системы, так и амилоидозом желудочно-кишечного тракта. Очень характерна гепатомегалия, природу которой следует дифференцировать между застойными явлениями вследствие сердечной недостаточности и амилоидным поражением печени. Последнее подтверждается повышением уровня щелочной фосфатазы сыворотки крови. Селезенка поражается часто, однако спленомегалия обнаруживается не всегда и большого клинического значения не имеет.
Макроглоссия, классический признак первичного амилоидоза, отмечается у 20% пациентов, инфильтрация мягких тканей может приводить к атрофии мышц, кожи, дистрофии ногтей, алопеции и появлению опухолевидных образований — амилоидом.
Реже встречается поражение сосудов, симптомами которого являются периорбитальная пурпура — «глаза енота» и экхимозы. Могут наблюдаться кровотечения, в том числе мочепузырные, обусловленные как изменением сосудистой стенки, так и нарушением свертывающей системы, в первую очередь дефицитом X-фактора, который связывается с амилоидом. Дефицитом факторов свертывания принято объяснять и характерный для амилоидоза тромбоцитоз.
Амилоидоз легких часто обнаруживается лишь при аутопсии. Однако в некоторых случаях одышка, кровохарканье и гидроторакс могут быть обусловлены не только застойной сердечной недостаточностью и нефротическим синдромом, но и амилоидным поражением легких. Возможны отложение амилоида в альвеолах и развитие легочных амилоидом. Рентгенологически могут выявляться сетчатые и нодулярные изменения в легочной ткани.
Поражение надпочечников может привести к надпочечниковой недостаточности, нередко остающейся нераспознанной, так как гипотензия и гипонатриемия рассматриваются как симптомы сердечной недостаточности и поражения вегетативной нервной системы. У 10—20% больных может иметь место гипотиреоз как проявление поражения щитовидной железы, нередко встречается увеличение подчелюстных слюнных желез.
Диагноз первичного амилоидоза помимо указанных клинических черт, которые могут быть сходными и при вторичном амилоидозе, базируется на ряде лабораторных данных. У 85% пациентов при иммуноэлектрофорезе белков сыворотки крови и мочи выявляются моноклональные иммуноглобулины. При рутинных исследованиях те же моноклональные иммуноглобулины обнаруживаются в моче в виде белка Бенс-Джонса. Биопсия костного мозга позволяет провести дифференциальный диагноз с множественной миеломой, а также выявить умеренное повышение количества плазматических клеток и их моноклональность при иммуногистохимическом окрашивании.
Однако даже сочетания характерной клинической картины и наличия моноклональных плазмоцитов и белков еще недостаточно для подтверждения диагноза первичного амилоидоза. Решающую роль здесь играют данные биопсии. Наименее инвазивной является аспирация подкожной жировой клетчатки передней брюшной стенки, дающая 80—90% положительных результатов при AL-амилоидозе (в нашей стране этот метод пока не нашел применения). Определенное диагностическое значение имеет биопсия десны и слизистой оболочки прямой кишки, но процент положительных результатов широко варьирует, в зависимости от стадии процесса, поэтому целесообразно выполнение биопсии одного из пораженных орга-нов — почки, печени, сердца, дающее почти 100% положительных результатов при амилоидозе AL-типа.
В первую очередь биопсийный материал окрашивается конго-красным. При обнаружении конгофилии исследуемого материала необходимо его исследование в поляризованном свете, эффект двойного лучепреломления характерен только для амилоида, другие конгофильные вещества яблочно-зеленой окраски не приобретают. После этого желательно типирование амилоида. Наиболее точным является иммуногистохимический метод с использованием моноклональных антител к белкам-предшественникам амилоида. Однако в настоящее время в нашей стране он практически недоступен. Поэтому для диагностики используется окраска с помощью растворов щелочного гуанидина или перманганата калия, что позволяет, хотя и косвенно, определить тип фибриллярных отложений.
Прогноз при первичном амилоидозе хуже, чем при других формах заболевания, средняя продолжительность жизни не превышает двух лет, при наличии поражения сердца или мультисистемного поражения без лечения больные погибают в течение нескольких месяцев. Наиболее частыми причинами смерти являются сердечная и почечная недостаточность, сепсис, сосудистые осложнения и кахексия. Патогенетическое сходство с миеломной болезнью позволяет рассчитывать на торможение прогрессирования заболевания при химиотерапии, проводимой с целью подавления моноклональных плазмоцитов. Существует несколько схем лечения (табл. 2).
Применение химиотерапии в случае успеха лечения позволяет увеличить продолжительность жизни больных на срок от 10 до 18 мес. Но эффективность терапии невысока, в частности, в связи с тем, что во многих случаях прогрессирование заболевания приводит к гибели больных до завершения курса лечения, а также из-за развития цитопении, инфекционных осложнений, фатальных нарушений ритма при лечении сверхвысокими дозами дексазона. Применение высоких доз мельфолана с трансплантацией аутологичных стволовых клеток позволяет достичь ремиссии более чем в 50% случаев, однако использование этого метода ограничено тяжестью состояния, возрастом больных, функциональными нарушениями со стороны сердца и почек. Во многих случаях возможна лишь симптоматическая поддерживающая терапия.
AA-амилоидоз
Развитие AA-амилоидоза происходит при хронических воспалительных процессах, предшественниками AA-амилоида являются сывороточные острофазовые белки, α-глобулины, продуцируемые клетками разных типов, в основном нейтрофилами и фибробластами. Вторичный амилоидоз развивается при ревматоидном артрите, болезни Бехтерева, псориатическом артрите, различных опухолях, лимфогранулематозе, неспецифическом язвенном колите и болезни Крона, при периодической болезни (семейной средиземноморской лихорадке), а также при туберкулезе, остеомиелите, бронхоэктатической болезни.
Характерными клиническими особенностями АА-амилоидоза является поражение почек у большинства пациентов, а также относительно редкое поражение печени и/или селезенки (около 10%) и сердца (выявляется лишь при эхокардиографии). Макроглоссия для вторичного амилоидоза не характерна. Диагноз основан на сочетании амилоидоза почек и хронического воспалительного заболевания, подтверждением служит иммуногистохимическое окрашивание биопсийного материала, в нашей стране используются уже упомянутые выше косвенные окрасочные методы.
Прогноз во многом зависит от природы основного заболевания, при естественном течении у трети больных через 5 лет от момента выявления протеинурии развивается почечная недостаточность. При периодической болезни пятилетняя выживаемость составляет 25%.
Лечение основано на подавлении очага — источника продукции сывороточных белков-предшественников. Удаление опухолей, секвестрэктомия, резекция кишки, лечение туберкулеза, уменьшение активности ревматоидного артрита (при использовании цитостатиков) приводят к прекращению прогрессирования амилоидоза, а иногда и к обратному развитию клинических проявлений, в частности нефротического синдрома.
Применение колхицина при периодической болезни является методом выбора, эффективность его доказана, лечение предотвращает развитие амилоидоза и тормозит его прогрессирование. При других формах вторичного амилоидоза эффективность колхицина не подтверждена.
Сенильные и наследственные формы системного амилоидоза, так же как и локальные формы, встречаются редко, диализный амилоидоз хорошо известен специалистам, в общей практике с ним сталкиваться практически не приходится.
Симптоматическая терапия зависит не от типа амилоидоза, а от пораженных органов-мишеней (табл. 3).
Амилоидоз, особенно первичный, считается нечастой патологией, однако в действительности он не столько редко встречается, сколько с трудом диагностируется. Адекватная диагностика требует не только знания клиники и патогенеза данного заболевания, но и наличия определенных диагностических возможностей. Чтобы проиллюстрировать это положение, приведем собственные данные (см. таблицу 4). В нефрологическом отделении МГКБ имени С. П. Боткина в 1993—2003 гг. наблюдалось 88 больных, которым был поставлен диагноз амилоидоза.
Диагноз был подтвержден морфологически у всех больных с AL-амилоидозом, старческим и неуточненным по типу амилоидозом, и у 30 пациентов со вторичным амилоидозом — всего в 53 случаях. У 12 больных выполнялась биопсия почки, а у двоих — биопсия печени, у восьми — биопсия кишки, в 12 случаях — десны, еще в 19 случаях диагноз был подтвержден при морфологическом исследовании секционного материала.
В большинстве случаев диагноз амилоидоза был установлен впервые в результате обследования в нефрологическом отделении. Нами было проведено сопоставление среди больных с AL-амилоидозом направительного и клинического диагнозов (табл. 5).
Лишь в двух случаях из 20 (10%) направительным диагнозом был «первичный амилоидоз», причем одному из этих больных он был поставлен в клинике терапии и профзаболеваний ММА, а другому — в зарубежной клинике.
Все больные, у которых диагностировалась миеломная болезнь с развитием AL-амилоидоза, были переведены в гематологические отделения. Из 11 больных с первичным амилоидозом семь пациентов получали химиотерапию комбинацией мельфолана с преднизолоном внутрь прерывистыми курсами, четверо из них — в сочетании с диализным лечением, и еще одна больная — только диализное и симптоматическое лечение. Из числа этих больных пять человек умерли в сроки от двух недель до двух лет от начала лечения (все с почечной недостаточностью и полиорганным поражением), один больной находится на диализе, один больной был направлен на трансплантацию аутологичных стволовых клеток, и одна больная получает лечение до настоящего времени. У одного пациента химиотерапия отложена в связи с наличием длительно не рубцующейся язвы желудка, и еще двое больных отказались от лечения.
Среди больных с вторичным амилоидозом в нашем исследовании преобладали пациенты с ревматоидным артритом, на втором месте среди причин — хронический остеомиелит и псориатический артрит, остальные заболевания встречались реже (табл. 6).
Лечение ревматоидного артрита и псориатического артрита проводилось с применением цитостатиков (метатрексата, азатиоприна), хотя во многих случаях возможности терапии были ограничены из-за наличия ХПН и сопутствующей патологии. Больные с хроническим остеомиелитом были направлены в отделения гнойной хирургии. Пациенты с болезнью Бехтерева и болезнью Крона получали специфическое лечение, больные с ХНЗЛ и туберкулезом также были направлены в профильные стационары. Одна из больных с опухолью желудка была успешно оперирована, и на протяжение четырех лет наблюдения нефротический синдром постепенно регрессировал, в остальных случаях опухолей распространенность процесса позволяла проводить только симптоматическую терапию, больной с лимфогранулематозом поступил в терминальном состоянии. Смертность среди пациентов со вторичным амилоидозом составила 38% (за счет больных с далеко зашедшим поражением на момент постановки диагноза). Все больные с периодической болезнью получали терапию колхицином.
Особенности диагностики и применения современных методов лечения первичного амилоидоза можно проиллюстрировать на следующем примере: больная К., 46 лет, впервые госпитализирована в конце октября 2002 г. с жалобами на отеки на ногах, сердцебиения, аменорею. В анамнезе — простудные заболевания, аппендэктомия, два нормальных срочных родоразрешения, указаний на заболевание почек, какие-либо хронические заболевания нет. В апреле 2002 г. перенесла острую пневмонию в верхней доле правого легкого, лечилась амбулаторно, получала инъекции абактала, линкомицина. В связи с локализацией пневмонии была обследована в туберкулезном диспансере, диагноз туберкулеза исключен. В начале июня впервые появились отеки на ногах, по поводу которых не обследовалась. Отеки через короткое время самостоятельно ликвидировались, затем возобновились. Больная была госпитализирована в терапевтический стационар, при обследовании выявлена протеинурия до 1,65%, гипопротеинемия (общий белок сыворотки крови 52 г/л), артериальное давление в норме (120/80 мм рт. ст.), мочевой осадок без изменений, креатинин плазмы также в пределах нормы. Установлен диагноз «острый гломерулонефрит», проведено лечение ампициллином, курантилом, гепарином, триампуром, выполнена тонзиллэктомия. Протеинурия сохранялась, отеки постепенно нарастали, в связи с чем для дальнейшего обследования и лечения больная с диагнозом «хронический гломерулонефрит» была направлена в больницу им. С. П. Боткина.
При осмотре — кожа чистая, обычной окраски, анасарка, отеки массивные, плотные, определяется асцит, периферические лимфатические узлы не увеличены. АД 110/70 мм рт. ст., тоны сердца звучные, ясные, ритмичные, ЧСС 90 уд/мин, печень и селезенка не увеличены, диурез до 1000 мл/сут, стул регулярный, без патологических примесей. При обследовании выявлен нефротический синдром — протеинурия 3 г/л, мочевой осадок скудный, гиподиспротеинемия, гиперлипидемия (общий белок сыворотки крови 39 г/л, альбумины 12 г/л, глобулины 7-30-15-19% соответственно α1-α2-β-γ холестерин 17,8 ммоль/л, β-липопротеиды 250 ЕД), при анализе мочи на белок Бенс-Джонса — реакция отрицательная, суточная экскреция 17-КС не снижена. Клинический анализ крови и другие биохимические показатели в пределах нормы, коагулограмма — выраженная гиперфибриногенемия, повышение уровня РКФМ. Исследование иммуноглобулинов крови: Ig-A — 0,35, Ig-M — 35,7 (две нормы), Ig-G — 1,96 г/л. Рентгенография органов грудной клетки, костей черепа и таза, УЗИ брюшной полости, почек, щитовидной железы, ЭХО-КГ без патологии, УЗИ малого таза — признаки аденомиоза тела матки, ЭГДС — рефлюкс-эзофагит, хронический гастрит. При осмотре невропатологом патологии не найдено, онкологом установлена фиброзно-кистозная мастопатия.
С целью уточнения генеза нефротического синдрома под местной анестезией под УЗ-наведением выполнена тонкоигольная пункционная биопсия правой почки, осложнений не было. При исследовании биоптата в мезангии клубочков и во внегломерулярных сосудах отмечается отложение амилоида. Амилоид загружает до 25% сосудистых петель клубочков. При иммуногистохимическом исследовании специфической люминисценции не найдено. При обработке препаратов раствором щелочного гуанидина в течение 2 ч конгофилия и их свойства в поляризованном свете сохраняются, что характерно для AL-амилоидоза.
Для выяснения природы AL-амилоидоза выполнено иммунохимическое исследование крови и мочи в лаборатории «Иммунотест». Выявлена М-лямбда парапротеинемия со снижением уровня поликлональных иммуноглобулинов и парапротеинурия Бенс-Джонса лямбда-типа на фоне массивной неселективной протеинурии. Больная была консультирована гематологом, высказано предположение о наличии болезни Вальденстрема, произведена трепанобиопсия костного мозга. Заключение: в имеющихся костно-мозговых полостях видны клетки всех трех ростков нормального гемопоэза, а также лимфоидные клетки, не образующие скоплений. Диагноз болезни Вальденстрема отвергнут в связи с отсутствием лимфоидной инфильтрации костного мозга, увеличения лимфоузлов и селезенки и отсутствием субстрата опухоли.
Установлен диагноз первичного амилоидоза с поражением почек, нефротическим синдромом, сохранной почечной функцией, признаков иных органных поражений не выявлено. С января 2003 г. начата химиотерапия мельфоланом 16 мг/сут и преднизолоном 100 мг/сут, курсами по четыре дня каждые шесть недель. Проводится также симптоматическое лечение: фуросемид, верошпирон, препараты калия, фамотидин, переливания альбумина. К настоящему времени проведено пять курсов химиотерапии с хорошей переносимостью, отеки уменьшились, протеинурия снизилась до 1,8 г/л, несколько уменьшилась выраженность гиподиспротеинемии (общий белок 46 г/л, альбумины 18 г/л, α2-глобулины 20%). Функция почек остается сохранной, креатинин плазмы 1,3 мг/Дл, признаков поражения других органов и систем при контрольных динамических обследованиях не выявлено.
Данный случай наглядно иллюстрирует тот факт, что для диагностики амилоидоза необходимо морфологическое, иммунологическое и иммунохимическое обследование. Так, у нашей пациентки наиболее очевидным клиническим диагнозом был «хронический гломерулонефрит», и в отсутствии возможности выполнения биопсии почки именно этот диагноз, скорее всего, и был бы поставлен. Никаких клинических указаний на системный характер заболевания, хронический воспалительный процесс, заболевание системы крови, за исключением повышения уровня Ig-M, у больной не было. И лишь полученные при исследовании почечного биоптата данные повлекли за собой трепанобиопсию костного мозга и иммунохимическое исследование, что в совокупности позволило поставить диагноз первичного амилоидоза до появления системных повреждений. Патогенетическая терапия была начата хотя и на фоне уже развившегося нефротического синдрома, но до наступления почечной недостаточности и при загрузке лишь 25% клубочков амилоидом, что прогностически относительно благоприятно.
В заключение отметим, что амилоидоз представляет собой тяжелое заболевание с высоким уровнем летальности, которое чрезвычайно трудно диагностировать, однако своевременное и качественное обследование больных позволяет поставить диагноз в более ранние сроки, а своевременное назначение адекватной терапии, в свою очередь, дает возможность улучшить прогноз в этой группе больных.
Литература
Е. В. Захарова
Московская городская клиническая больница им. С. П. Боткина