метасиликат натрия что это такое
Метасиликат натрия
| Метасиликат натрия | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Метасиликат натрия; силикат натрия |
| Традиционные названия | Кремнекислый натрий |
| Химическая формула | Na2SiO3 |
| Физические свойства | |
| Состояние (ст. усл.) | бесцветные или белые кристаллы |
| Молярная масса | 122,06 г/моль |
| Плотность | 2,4; 2,61 г/см³ |
| Термические свойства | |
| Температура плавления | 1088; 1089 °C |
| Энтальпия образования (ст. усл.) | −1535 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 18,8 20 ; 92,3 90 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,52 |
| Классификация | |
| Рег. номер CAS | 6834-92-0 |
| Рег. номер PubChem | 23266 |
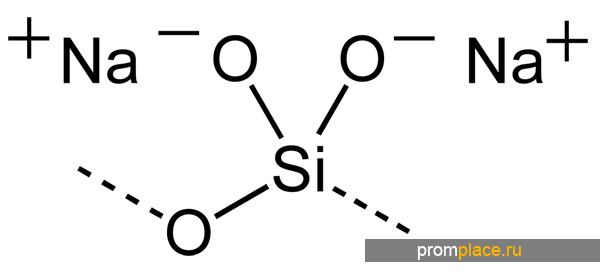
| SMILES | [Na+].[Na+].[O-][Si]([O-])=O |
| Регистрационный номер EC | 229-912-9 |
| RTECS | VV9275000 |
Метасиликат натрия — неорганическое соединение, соль щелочного металла натрия и метакремниевой кислоты с формулой Na2SiO3, бесцветные или белые кристаллы, растворяется в холодной воде, образует кристаллогидрат.
Содержание
Получение
Физические свойства
Метасиликат натрия образует бесцветные или белые кристаллы ромбической сингонии, пространственная группа C cm2, параметры ячейки a = 0,6078 нм, b = 1,053 нм, c = 0,4825 нм, Z = 4.
Хорошо растворим в холодной воде, концентрированные растворы образуют коллоидный раствор «жидкое стекло» гидрозоля SiO2•n H2O.
Из водных растворов выделяется кристаллогидрат Na2SiO3•9H2O, который плавится при 47°С в собственной кристаллизационной воде и начинает разлагаться при температуре выше 100°С.
Разлагается в горячей воде.
Химические свойства
Применение
Литература
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | — | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Метасиликат натрия» в других словарях:
МЕТАСИЛИКАТ НАТРИЯ — разновидность силикатов натрия … Металлургический словарь
метасиликат натрия — метакремнекислый натрий, кремнекислый натрий … Cловарь химических синонимов I
Метасиликат калия — Общие Систематическое наименование Метасиликат калия; силикат калия Традиционные названия Кремнекислый калий Химическая формула K2SiO3 Физические свойства … Википедия
Натрия фосфаты — Известны следующие фосфаты натрия: Дигидрофосфат натрия NaH2PO4 Гидрофосфат натрия Na2HPO4 Ортофосфат натрия Na3PO4 Применение Употребляются для буферных растворов различного назначения, как эмульгаторы в пищевой промышленности … Википедия
Метасиликат марганца(II) — Общие Систематическое наименование Метасиликат марганца(II) Традиционные названия Кремнекислый марганец Химическая формула MnSiO3 Физические свойства … Википедия
натрия метасиликат — natrio metasilikatas statusas T sritis chemija formulė Na₂SiO₃ atitikmenys: angl. sodium metasilicate rus. натрий метакремнекислый; натрия метасиликат ryšiai: sinonimas – dinatrio trioksosilikatas … Chemijos terminų aiškinamasis žodynas
НАТРИЯ СИЛИКАТЫ — соли к т кремния. Бесцв. кристаллы или стеклообразные в ва. Известны: метасиликат Na2SiO3, ортосиликат Na4SiO4, пиросиликат Na6Si2O7, a также пентаоксодисиликат Na2Si2O5, октаоксотрисиликат Na4Si3O8, гептаоксотрисиликат Na2SiO3, октасиликат… … Химическая энциклопедия
Гексафторосиликат натрия — Общие Систематическое наименование Гексафторосиликат натрия Химическая формула Na2[SiF6] Физические свойства Состояние (ст. усл.) Бесцвет … Википедия
Ортосиликат натрия — Общие Систематическое наименование Ортосиликат калия; силикат калия Традиционные названия Кремнекислый калий Химическая формула Na4SiO4 Физические свойства … Википедия
Гексагидроксоплюмбат(IV) натрия — Общие Систематическое наименование Гексагидроксоплюмбат натрия Химическая формула Na2[Pb(OH)6] Физические свойства Состояние (ст. усл.) … Википедия
Метасиликат натрия
| Метасиликат натрия | |
|---|---|
 | |
| Систематическое наименование | Метасиликат натрия; силикат натрия |
| Традиционные названия | Кремнекислый натрий |
| Хим. формула | Na2SiO3 |
| Состояние | бесцветные или белые кристаллы |
| Молярная масса | 122,06 г/моль |
| Плотность | 2,4; 2,61 г/см³ |
| Т. плав. | 1088; 1089 °C |
| Энтальпия образования | −1535 кДж/моль |
| Растворимость в воде | 18,8 20 ; 92,3 90 г/100 мл |
| Показатель преломления | 1,52 |
| ГОСТ | ГОСТ 13079-93 |
| Рег. номер CAS | 6834-92-0 |
| PubChem | 23266 |
| Рег. номер EINECS | 229-912-9 |
| SMILES | |
| Рег. номер EC | 229-912-9 |
| RTECS | VV9275000 |
| ChEBI | 60720 |
| Номер ООН | 3253 |
| ChemSpider | 21758 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
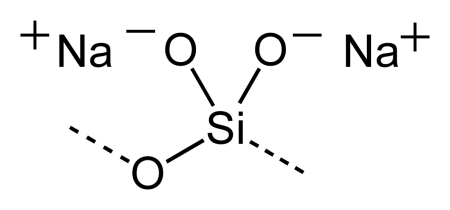
Метасиликат натрия — неорганическое соединение, соль щелочного металла натрия и метакремниевой кислоты с формулой Na2SiO3, бесцветные или белые кристаллы, растворяется в холодной воде, образует кристаллогидрат.
Содержание
Получение
Физические свойства
Метасиликат натрия образует бесцветные или белые кристаллы ромбической сингонии, пространственная группа C cm2, параметры ячейки a = 0,6078 нм, b = 1,053 нм, c = 0,4825 нм, Z = 4.
Хорошо растворим в холодной воде, концентрированные растворы образуют коллоидный раствор «жидкое стекло» гидрозоля SiO2•n H2O.
Из водных растворов выделяется кристаллогидрат Na2SiO3•9H2O, который плавится при 47°С в собственной кристаллизационной воде и начинает разлагаться при температуре выше 100°С.
Разлагается в горячей воде.
Водные растворы имеют щелочную реакцию из-за гидролиза по аниону.
Натрий метасиликат — востребованный в промышленности и строительстве реактив
Вторая статья о метасиликате натрия. Первую статью, в которой рассказывается об основных особенностях и свойствах реактива, и в которой приводятся инетерсные факты о нем, можно прочитать здесь.
Реактив относится ко второму классу опасности. Разъедает кожу 
Хранить натрий метакремнекислый следует в сухих помещениях в герметичной таре, защищенной от попадания влаги и воздуха. В противном случае, в результате поглощения углекислоты из воздуха вещество постепенно разлагается с выделением нерастворимой кремниевой кислоты. Транспортировать натрий метасиликат можно автомобильным и железнодорожным транспортом, в том числе и навалом. В последнем случае следует принять меры, чтобы защитить продукт от влаги. Фасуют реактив, как правило, в герметично запаянные пластиковые водостойкие мешки, которые для надежности помещают во внешние тканевые или многослойные бумажные мешки.
В лабораториях растворы реактива хранят в стеклянных бутылях, герметично укупоренных резиновой или силиконовой пробкой. Пробковые и стеклянные пробки могут очень прочно приклеиться к горловине.
 |  |  |
| Пробка резиновая | Стекло жидкое натриевое | Пробка силиконовая |
Метасиликат натрия: свойства, применение, особенности, различие между безводным и пятиводным натрием кремнекислым

Свойства
Белый порошок с бесцветными кристалликами, без запаха. Технический продукт может быть сероватым или с желтоватым оттенком. Активно поглощает из воздуха влагу и углекислоту. Хорошо растворяется в воде при комнатной температуре, образует кристаллогидраты с пятью и девятью молекулами воды. Разлагается при нагревании и в горячей воде. Вещество не слеживается при хранении, кристаллики механически прочные (не образует пылеобразного порошка).
Применение
Рассматриваемый материал – активный участник множества процессов в различных направлениях.
· Компонент шихты в производстве стекла
· Производство жаростойких кислотоупорных бетонов
· Наполнитель в облегченных цементных растворах для цементирования скважин.
· Обеззараживание грубых поверхностей
· Клей под названием «жидкое стекло».

Силикат натрия нередко вводят в буровые растворы. Задача при этом преследуется следующая: стабилизация скважин и предотвращение разрушения буровых стен. Наибольшая полезность данного материала отмечается при прохождении скважин через глинистые пласты.

· 
Безопасность
Токсичен при проглатывании, требуется защитная одежда. Едкий материал, который является сильным раздражителем для глаз, кожи и слизистой оболочки. Проглатывание вызывает расстройство желудочно-кишечного тракта. При нагревании до разложения он выделяет токсичные пары Na2O.
метасиликат натрия
Стекло в состоянии жидкости или зачастую используемая в производстве добавка для пищевых продуктов Е550 и представляет собой метасиликат натрия.
Получение такого вещества изначально было осуществлено в начале 1818 года в германии. Авторство получение вещества принадлежит немецкому химику Яну Непомук фон Фуксу.
Такому соединению характерно широкое распространение в природных условиях. Содержание силикатов зафиксировано в части равной чуть меньше половины группы, объединяющей все известные соединения минеральных веществ, а именно:
В уравнениях химических реакций метасиликат натрия принято обозначать с помощью следующей молекулярной формулы:
Na2SiO3.
Использование данной формулы актуально для безводного метасиликата натрия или иначе называемого типичным.
Краткая характеристика вещества
Разновидности силикатов
Любая натриевая соль кремниевых кислот, обозначаемая формулой общего типа, на практике и представляет собой силикат натрия.
В общей формульном выражении соединения mNa2O*nSiO2, где определяются отношения чисел молекул SiО2 и Na2О, такое соотношение величин получило название кремнеземного модуля. Смысл такого модуля в том, чтобы точно определять степень растворимости и иные явно выраженные свойства натриевых силикатов.
Колебания значений модуля, как правило, находятся в пределах показателей:
Натрия метасиликат встречается в 2 – х вариантах кристаллической формы:
Натрия метасиликат отображается в химических уравнениях и реакциях формульным выражением:
Основные реакции Nа2SiОЗ
Бороться с нежелательными последствиями и возникновением реакций последнего случая можно с помощью правильно подобранной упаковки вещества, главным критерием отбора которой является ее повышенная непроницаемость в отношении водяного пара и воздушных поступлений.
Также стекло в жидком состоянии отличается хорошо протекающей сильной щелочной реакцией. Это объясняется протеканием их гидролиза, где образуются гидроксид – ионы:
Nа2ОSiО2 + 2Н2О = 2Nа+ +SiО2*Н2О + 2ОН
Способы получения в промышленности
Метасиликат натрия пятиводный доступно получить при осуществлении метода, основой которого является изогидрическая кристаллизация кремнеземистых щелочных растворов.
Основным способом, обеспечивающим гарантированное получение кристаллизованных гидратов в отношении натрия метасиликата пятиводного, шестиводного, девятиводного, является обеспечение успешного протекания следующей реакции:
SiО2 + NаСО3 = NаSiО3 + СО2
Сферы применения натрия метасиликата
Вещество Na2SiO3 широко применяется в следующих производственно – промышленных областях:
Требования к безопасности использования вещества
Метасиликат натрия как пятиводный, так и шести-, девятиводный не представляет опасности в отношении провоцирования взрывов. Следовательно особые повышенные требования к соблюдению пожарной техники безопасности не предъявляются.
Степень воздействия и влияния вещества на человеческий организм позволяет отнести Na2SiO3 к группе веществ II класса опасности.
Правила при транспортировке
При транспортной перевозке натрия метасиликата обязательно наличие маркировочного символа в соответствии с ГОСТ – 14192, где подразумевается нанесение знаков, указывающих на ограждение вещества от влияния влаги и исключение контактов с кожными покровами и слизистыми оболочками.
Виды упаковки и меры хранения
В случае упаковки метасиликата натрия, как правило, используются:
Вне зависимости от того, у кого приобретается продукция, каждому покупателю следует обратить внимание на качество и соответствие метасиликата натрия установленным требованиям.