многоядерные клетки типа инородных тел в гинекологии что это
Многоядерные клетки типа инородных тел в гинекологии что это
Цель исследования, исходя из вышеизложенного, ‒ определить клинико-морфологические и молекулярно-биологические характеристики ЛМС тела матки с большим количеством многоядерных клеток в своем составе и прогноз больных с таким типом неоплазии.
Материалы и методы исследования
Результаты исследования и их обсуждение
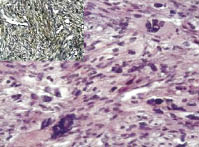
Рис. 1. Лейомиосаркома с большим
количеством многоядерных клеток, степень злокачественности G1. Окраска гематоксилин и эозин; ув. х200; в левом верхнем углу
позитивная иммуногистохимическая
реакция к SMA
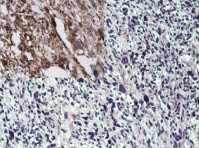
Рис. 2. Лейомиосаркома с большим
количеством многоядерных клеток, степень злокачественности G2. Окраска гематоксилин и эозин; ув. х100; в левом верхнем углу
позитивная иммуногистохимическая
реакция к SMA
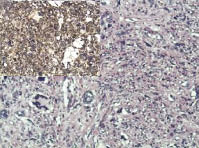
Рис. 3. Лейомиосаркома с большим
количеством многоядерных клеток, степень злокачественности G3. Сложно
дифференцировать с фиброзной
гистиоцитомой. Окраска гематоксилин
и эозин; ув. х200; в левом верхнем углу
позитивная иммуногистохимическая
реакция к SMA
Сравнительные молекулярно-биологические характеристики лейомиосаркомы тела матки и 10-летняя выживаемость при гистологической форме веретеноклеточной
лейомиосаркомы и с большим количеством многоядерных клеток
Медицинский центр
ЮНОНА в Перми
Категории услуг
О медицинском центре
Роль ВПЧ в генезе дисплазии эпителия шейки матки
Неуклонный рост инфекций передаваемых половым путем приковывает к себе внимание врачей различных специальностей. Большое внимание уделяется этому вопросу также акушерами-гинекологами. По данным ВОЗ за 2003-20004 годы количество ИППП увеличилось в среднем на 69%. На одно из первых мест в данной заболеваемости выходят инфекции вирусной этиологии. Так общеизвестно, что вирус папилломы человека является одним из онкогенов в формировании рака шейки матки. Широкое распространение в последние годы получил папилломатоз гортани у детей, по праву считается, что причиной этого является инфицирование дыхательных путей новорожденных во время прохождения через родовые пути инфицированной матери. Именно поэтому лечение заболеваний, обусловленных вирусом папилломы человека, является актуальной проблемой.
Заболевания человека, вызванные папилломавирусами, известны давно и описаны античными авторами как фиги-кондиломы, которые иногда достигают огромных размеров.
Точно также давно известны бородавки разной локализации, наиболее часто наблюдаемые у детей.
Вирусная этиология остроконечных кондилом и бородавок предполагалась давно, но лишь в последние десятилетия накоплены научные данные о строении и свойствах папилломавирусов. Успехи молекулярной биологии создали возможность судить не только о присутствии вируса в ткани бородавок, кондилом, опухолевых образований, но даже произвести разделение папилломавирусов на типы и проследить связь типа вируса с заболеванием той или иной локализации.
Особое внимание привлекли папилломавирусы, связанные с разнообразными поражениями аногенитальной области и передаваемые при половом контакте.
Папилломавирусы вызывают выраженную клеточную пролиферацию эпителия слизистых оболочек и кожи. Заражение происходит при прямом контакте, хотя нельзя полностью отрицать передачу вируса через загрязненные предметы одежды, через банные принадлежности и т.п. На месте внедрения вируса образуется разрастание клеток эпителия в виде разнообразных по форме и величине бородавок, папиллом, кондилом. Нередко присутствие папилломавируса не даёт никаких заметных изменений, хотя вирус присутствует и легко передаётся половому партнёру. Часто имеющиеся разрастания самопроизвольно исчезают, как это наблюдается при кожных юношеских бородавках.
Наряду с доброкачественными опухолевидными разрастаниями папилломавирусы признаны причиной некоторых форм рака половых органов, наиболее часто рака шейки матки. Можно считать доказанной причинную связь рака шейки матки с определёнными типами вируса папилломы человека (ВПЧ). Ряд исследователей полагает, что 10-15% всех раков у человека связаны с папилломавирусами.
Вирус заражает самый нижний глубокий слой кожи или слизистой оболочки, происходит усиленное размножение клеток этого слоя, что и приводит к образованию разрастаний. Сам вирус в глубоких слоях не размножается, его интенсивное размножение происходит в поверхностных слоях — в чешуйчатых клетках, которые по мере оттеснения к поверхности перестают делиться и становятся более пригодными для размножения вируса.
Благодаря молекулярно-гибридизационным методам стало известно, что существует много типов папилломавирусов, 30 из них инфицируют половые органы и область заднего прохода. У женщин инфицируется и покрывается генитальными бородавками область преддверия
влагалища, стенки влагалища, шейка матки, наружное отверстие уретры. У мужчин поражается головка полового члена, крайняя плоть, мошонка, анальная область. В родах папилломавирус передается ново рожденному ребенку.
Источником возникновения дисплазии может являться как многослойный плоский неороговевающий эпителий влагалищной порции шейки матки, так и резервные клетки (аналог базальных клеток в зоне цервикального канала). Значение резервных клеток в генезе дисплазии и рака шейки матки подтверждено длительными систематическими наблюдениями, при которых у большинства пациенток страдающих неоплазией стадией её развития была метаплазия (зрелая и незрелая) и резервно-клеточная гиперактивность, выявляемые при проведении микрокольпоскопии. В свете этих данных «зона трансформации», являющаяся «слабым местом», должна быть предметов особо пристального изучения. Изолированно в цервикальном канале дисплазии и рак наблюдаются редко (за исключением женщин в климактерическом периоде).
Цитологическое исследование в настоящее время чаще используется как метод скрининг-тестирования, поскольку имеют свои недостатки. При неправильном заборе материала, когда в мазке преобладают клетки крови, бактериальная флора, а клеток многослойного плоского эпителия нет цитологическое исследование может не выявить атипических клеток, даже при наличии неоплазии в шейке матки. Для правильного взятия материала с шейки матки необходимо после удаления слизи произвести «соскоб» с поверхности эктоцервикса и из цервикального канала. При исследовании мазков, как эксфолиативного материала в большинстве случаев невозможно оценить степень нарушения стратификации пласта, а следовательно приходиться ориентироваться на качественные и количественные, а не топографические признаки, что создаёт свои трудности, ведь понятие «дисплазия» является тканевым, а не клеточным. К тому же выявить инвазию опухоли в подлежащие ткани и их реакцию вообще невозможно. Кроме того цитологические признаки неопластического процесса и многих урогенитальных инфекций (УГИ) имеют ряд схожих черт: многоядерность клеток, увеличение размеров и объема ядер эпителиоцитов, наличие ядер неправильной формы, гиперхромных, с изрезанными контурами, с конденсацией хроматина диффузно в ядре или у ядерной мембраны. При отсутствии значительного опыта в диагностике УГИ патоморфологом и гинекологом описанные изменения могут быть неправильно интерпретированы. При цитологическом исследовании необходимо учитывать возраст пациентов и особенности гормонального статуса.
Основным методом диагностика остаётся гистологическое исследование биопсийного материала (в идеале взятого прицельно при проведении колъпоскопии). Уточнение морфологических критериев этих поражений шейки матки позволяет морфологу дать полноценное гистологическое заключение, что имеет первостепенное значение для определения рациональной тактики ведения больной и определения прогноза заболевания.
В последние годы российскими и зарубежными авторами активно изучается роль УГИ в онкогенезе. По современным представлениям больные с CIN 1 и 2 наблюдаются у гинеколога, а пациенты с CIN 3 должны обследоваться онкогинекологом. Такое распределение пациентов по нашему мнению вполне оправдано, поскольку дисплазии 1 и 2 степени чаще всего развиваются на фоне различных инфекций (герпетическая, папилломовирусная, хламидийная инфекция), или рассматриваются как их проявление. Роль папиломовирусов (ПВИ) и вирусов простого герпеса (ВПГ) в онкогенезе хорошо освещена как в отечественной, так и в зарубежной литературе. Особое значение имеют микст-инфекции, при которых различные возбудители, взаимодействуя друг с другом и макроорганизмом существенно утяжеляют течение инфекционного процесса и могут ускорят онкогенез. Иммунологические исследования, проведённые в Центре акушерства, гинекологии и перинатологии РАМН, свидетельствуют, что в случаях дисплазии эпителия и эктопий, не связанных с ПВИ, местный иммунитет существенно не страдает, а у больных с выявленной ПВИ отмечается снижение и инактивация местных протективных факторов в цервикальном канале. Некоторые исследователи предлагают также рассматривать инфицирование хламидиями как потенциальный фактор дисплазии и рака шейки матки. При этом в последнее время число сообщений о возможной связи между хламидийной инфекцией и цервикалъной внутриэгштелиальной неоплазией возросло (Heinrich, 1994; Рудакова, 1996; Sanjose, 1994).
При морфологической верификации диагноза могут возникнуть трудности при дафференциации «истинной» и «наведённой» дисплазии, необходимой, поскольку тактика ведения больных может существенно различаться (в одном случае консервативное, в другом оперативное лечение). Однако существуют цитоморфологические признаки позволяющие заподозрить и диагностировать УГИ. К таким признакам можно отнести:
При терапии УГИ и неоплазии следует учитывать особенности клинической, морфологической картины, иммунного статуса, наличие инфекционных микстов, отягощенного акушерскогинекологаческого анамнеза. Основой терапии являются этиотропная (противовирусная и антибиотикотерапия), противовоспалительная и иммунокоррегирующая терапия.
В качестве примера обратимости диспластических изменений эпителия шейки матки и эффективности комплексной терапии приведём несколько наблюдений из практики.
Многоядерные клетки типа инородных тел в гинекологии что это
ФГУ «НИИ пульмонологии» ФМБА России
ФГУ «НИИ пульмонологии» ФМБА России
Гистологическая дифференциальная диагностика гранулематозных болезней легких (часть I)
Журнал: Архив патологии. 2019;81(1): 65-70
Самсонова М. В., Черняев А. Л. Гистологическая дифференциальная диагностика гранулематозных болезней легких (часть I). Архив патологии. 2019;81(1):65-70.
Samsonova M V, Cherniaev A L. Histological differential diagnosis of granulomatous lung diseases (part I). Arkhiv Patologii. 2019;81(1):65-70.
https://doi.org/10.17116/patol20198101165
ФГУ «НИИ пульмонологии» ФМБА России
Гранулематозные болезни — это гетерогенная группа заболеваний различной этиологии, проявляющихся разнообразными клиническими синдромами и вариантами тканевых изменений, неоднородной чувствительностью к терапии и преобладанием общего доминирующего гистологического признака — наличием гранулем, определяющих клинико-морфологическую сущность каждой болезни. Гранулема является хронической воспалительной реакцией, в которой принимают участие клетки макрофагальной системы и другие клетки воспаления. После воздействия антигена происходит активация T-лимфоцитов, макрофагов, эпителиоидных клеток и гигантских многоядерных клеток, приводящая к образованию гранулемы. Гранулема включает также внеклеточный матрикс, продуцируемый фибробластами, позволяющий отграничить и изолировать антиген. Гранулематозные заболевания классифицируются по этиологии на инфекционные и неинфекционные. Однако, согласно последним исследованиям, патогенные микроорганизмы могут быть причиной развития гранулем при заболеваниях, ранее считавшихся неинфекционными. В ряде случаев классифицировать гранулематозный процесс как инфекционный и неинфекционный весьма трудно. Цель настоящего исследования — привлечь внимание читателей к разнообразию гранулематозных заболеваний, описать ключевые моменты патолого-анатомических проявлений различных болезней неинфекционной природы, а также определить подход к дифференциальной диагностике гранулематозов.
ФГУ «НИИ пульмонологии» ФМБА России
ФГУ «НИИ пульмонологии» ФМБА России
Название «гранулема» происходит от латинского слова granulum, означающее «зерно», греческое окончание (—oma) используется для обозначения узелкового образования. Таким образом, гранулема представляет собой узелковое очерченное образование. При микроскопической оценке термин используется для обозначения компактных агрегатов клеток. Микроскопически гранулемы могут состоять из гистиоцитов и/или эпителиоидных клеток, гигантских многоядерных клеток и других клеток воспаления (лимфоциты, нейтрофилы, эозинофилы). Эпителиоидные и гигантские многоядерные клетки являются производными моноцитов/макрофагов, первые являются дифференцированными секреторными клетками, тогда как последние специализированы на функции фагоцитоза [1]. Гигантские многоядерные клетки образуются путем слияния или неполного клеточного деления, что было доказано в экспериментальных исследованиях [2], причем раньше образуются гигантские клетки инородных тел, затем – клетки Пирогова—Лангханса. Лимфоциты располагаются преимущественно по периферии гранулемы и представляют популяцию T-клеток, тогда как B-лимфоциты разрозненно лежат вне гранулемы. В зависимости от заболевания T-лимфоциты представлены преимущественно T-хелперами 1 и 2 или же цитотоксическими T-супрессорами.
Гранулематозные болезни — гетерогенная группа заболеваний различной этиологии, проявляющихся разнообразными клиническими синдромами и вариантами тканевых изменений, неоднородной чувствительностью к терапии, при этом преобладает общий доминирующий гистологический признак — наличие гранулем, определяющих клинико-морфологическую сущность каждой болезни [3]. Настоящая публикация преследует цель привлечь внимание читателей к разнообразию гранулематозных заболеваний легких, описать ключевые моменты патолого-анатомических проявлений различных заболеваний инфекционной и неинфекционной природы, а также определить подход к дифференциальной диагностике гранулематозов.
При гранулематозных заболеваниях неинфекционной природы, как правило, развиваются ненекротические гранулемы, за некоторыми исключениями, о которых будет сказано ниже.
Саркоидоз
Поражение легких при саркоидозе описано в 90% наблюдений. Морфологическим субстратом саркоидоза является эпителиоидно-клеточная гранулема — компактное скопление мононуклеарных фагоцитов — макрофагов и эпителиоидных клеток. Каждая саркоидная гранулема имеет следующие стадии развития: 1) ранняя или лимфогистиоцитарная гранулема иногда с примесью нейтрофилов (рис. 1); 
Процесс организации гранулем начинается с периферии, что придает им четко очерченный, «штампованный» вид (рис. 2). 

Значительное число лимфоцитов в ткани легких при саркоидозе представлено преимущественно Т-клетками. Для дифференциальной диагностики саркоидоза полезно оценивать бронхоальвеолярный смыв, в котором при этом заболевании среди лимфоцитов преобладают Т-хелперы (CD4+), соотношение CD4/CD8 составляет 3,5—10:1 (в норме 1,8:1). Гигантские клетки в составе гранулем могут содержать в цитоплазме включения, такие как астероидные тельца, тельца Шауманна или кристаллоидные структуры. Эти включения характерны для саркоидоза, однако не являются патогномоничными, так как могут присутствовать и при других гранулематозных заболеваниях [5].
При исследовании биоптатов бронхов и легких при гранулематозных заболеваниях, как правило, обнаруживают диссеминированное поражение с васкулитом, периваскулитом, перибронхитом; гранулемы чаще всего локализуются в межальвеолярных перегородках. Гранулематозное поражение бронхов и бронхиол при саркоидозе встречается часто и описано у 15—55% пациентов. Нередко гранулемы располагаются в стенке сосуда, частота гранулематозного васкулита может достигать 69%. В этих наблюдениях следует дифференцировать саркоидоз с некротизирующим саркоидным гранулематозом, который ряд авторов относят к узловой форме саркоидоза [6]. Для последнего характерно развитие некрозов.
В целом для саркоидоза характерными являются наличие четко очерченных, «штампованных гранулем», располагающихся по ходу лимфатических сосудов, концентрический фиброз вокруг гранулем, гиалиноз внутри и между гранулемами, гранулематозный васкулит, отсутствие хронического интерстициального воспаления вне гранулематозного поражения и фокусов организующейся пневмонии.
Помимо саркоидоза, встречается так называемая неспецифическая саркоидная реакция в виде эпителиоидно-клеточного гранулематоза. Она обычно наблюдается в регионарных лимфатических узлах, но может встречаться и в ткани легких при псевдоопухолях, злокачественных новообразованиях, паразитарных заболеваниях, экзогенном аллергическом альвеолите, туберкулезе. Гистологически саркоидная реакция отличается ограниченностью и топической связью с указанными патологическими процессами.
Гиперсенситивный пневмонит
Некротический гранулематоз встречается также при аллергическом ангиите с гранулематозом (ранее — болезнь Черджа—Стросса) в сочетании с некротическим васкулитом и эозинофильной пневмонией. Гранулемы при аллергическом ангиите с гранулематозом хорошо оформленные, с центральным некрозом, содержащим множество эозинофилов, имеет место эозинофильная инфильтрация стенок сосудов и бронхиол, некротический васкулит с наличием эозинофилов и гигантских многоядерных клеток. Однако классическая триада изменений в виде гранулематоза, некротического васкулита и эозинофильной пневмонии в легких встречается нечасто, поэтому для установления диагноза необходимы дополнительные клинические и лабораторные данные.
Некротические гранулемы могут формироваться в легком и при ревматоидном артрите, однако диагноз в этом случае следует формулировать с осторожностью. Прежде всего следует учитывать клинические данные, поскольку узелковые формы ревматоидного артрита развиваются только в активной фазе заболевания, у серопозитивных пациентов с наличием выраженного суставного синдрома. При этом заболевании некроз, как правило, окрашен эозинофильно, клеточный детрит располагается обычно между некрозом и окружающим его гистиоцитарным валом, может сочетаться с васкулитом, однако некротический васкулит нехарактерен (рис. 7) 
При дифференциальной диагностике васкулитов с развитием гранулематозной реакции, описанных выше, следует учитывать специфические серологические признаки того или иного заболевания.
Инфекционный гранулематоз следует также дифференцировать с НСГ. Последний имеет также некоторые сходства с полиангиитом с гранулематозом. При НСГ характерно развитие интерстициального некроза, который чаще эозинофильно окрашен, однако иногда может содержать клеточный детрит. Однако некроз при НСГ сочетается с имеющимися ненекротизирующими гранулемами саркоидного типа, состоящими преимущественно из эпителиоидных и гигантских многоядерных клеток с небольшим числом лимфоцитов, эти гранулемы имеют тенденцию к слиянию, часто располагаются вблизи кровеносных сосудов или в их стенке, не приводя, однако, к развитию васкулита (рис. 8) 
Поскольку некроз при инфекционном гранулематозе может быть коагуляционного типа, его также следует дифференцировать с инфарктом легкого. В стадии организации инфаркты могут быть окружены фибробластами и клетками воспаления, напоминая гранулематозное воспаление. В резецированных кусочках легкого при инфаркте, как правило, можно обнаружить тромбы в ветвях легочной артерии, явившиеся причиной развития инфаркта [13].
Наличие гигантских многоядерных клеток «инородных тел» и выраженной воспалительной реакции при аспирационной пневмонии в ряде случаев может напоминать гранулематозный процесс, для диагностики этого заболевания необходима тщательная оценка гистологических срезов с целью обнаружения различных инородных остатков пищи (растительных клеток, фрагментов поперечнополосатых мышц и др.).
Дифференциально-диагностические признаки основных неинфекционных заболеваний легких приведены в таблице. 
Таким образом, для проведения дифференциальной диагностики гранулематозных заболеваний необходимо оценить форму (очерченность, «зрелось») гранулемы, ее клеточный состав, наличие/отсутствие некроза, цвет некроза, клеточную реакцию по периферии некроза, состояние ткани легкого вне зоны гранулематозного воспаления, а также другие специфические признаки. Дифференциальная диагностика гранулематозных процессов инфекционной природы будет рассмотрена в части II.
Авторы заявляют об отсутствии конфликта интересов.
ГИГАНТСКИЕ КЛЕТКИ
Гигантские клетки нередко образуются при продуктивном воспалении (см.), являясь характерной структурной особенностью многих специфических гранулем, при регенерации (см.), инфекционных процессах вирусной этиологии, в опухолях, в частности — костных (остеобластокластома), при современных методах лечения цитостатическими препаратами, рентгеновскими лучами. При ряде заболеваний (напр., при анемиях различного происхождения, при реактивных эритробластозах, остеомиелосклерозе) в очагах экстрамедуллярного кроветворения встречаются мегакариоциты. При воспалении, регенерации, нарушениях обмена, напр, при остеомиелитах, рахите, системной фиброзной остеодистрофии, костных переломах, встречаются остеокласты. При патологических процессах встречаются преимущественно два морфологических типа Гигантских клеток: инородных тел — некрофаги Подвысоцкого (1889) и Г. к. типа Пирогова—Лангханса (Th. Langhans, 1868).
В Г. к. инородных тел ядра разбросаны группами или расположены в центре клетки; количество их может колебаться в пределах от 3—5 до 100 и более; они светлые, овальные, могут быть и гиперхромными. Цитоплазма клетки гомогенная. Г. к. инородных тел образуются при попадании в организм труднорастворимых инородных тел, напр, кусочков дерева, стекла, обрывков операционного шелка, волокон ваты, нерастворимых газов (напр., при пневматозе кишечника). Иногда они образуются в ответ на скопление труднорастворимых продуктов, появляющихся в результате каких-либо патол. процессов в самом организме, напр, частицы эктопического или избыточного рогового вещества (цветн. рис. 7), хряща, кристаллов жирных кислот, продуктов некроза жировой клетчатки, в атероматозных бляшках при атеросклерозе, при рассасывании амилоида, при распаде эластической ткани артерий и т. д.
Гигантские клетки типа Пирогова—Лангханса характеризуются периферическим расположением овальных ядер; цитоплазма их делится на эндо- и эктоплазму. Характерным считается наличие клеточного центра с многочисленными центриолями, которые соединены между собой центродесмозами, образующими своеобразную сеть внутри клетки; в этих Г. к. также обнаруживается большое количество митохондрий (рис.), канальцы эндоплазматического ретикулума иногда заполнены жировыми вакуолями. В ядре отмечается увеличение размеров или количества ядрышек. Г. к. типа Пирогова—Лангханса могут достигать 300 мкм в диаметре, количество ядер в них ок. 200. Наличие Г. к. типа Пирогова—Лангханса является характерным для туберкулезного продуктивного воспаления; в их цитоплазме можно видеть фагоцитированные кислотоустойчивые туберкулезные микобактерии, хорошо окрашивающиеся по Циля — Нельсена методу (см.). Наличие микобактерий имеет решающее значение для диагноза, т. к. Г. к. типа Пирогова—Лангханса могут образоваться и при других инфекционных и неинфекционных воспалительных процессах, напр, при бруцеллезе, сифилисе, проказе (клетки Вирхова), микозах, склероме (клетки Микулича), симпатической офтальмии, болезни кошачьей царапины, саркоидозе, липогранулематозе и др.
При вирусных инфекциях, помимо Г. к. типа Пирогова Лангханса и Г. к. инородных тел, обнаруживают Г. к. эпителиального происхождения, что зависит от тропизма многих вирусов к эпителиальным клеткам. Образование большого количества Г. к. при вирусных инфекциях наблюдается преимущественно в детском возрасте.
Многоядерные Г. к. с причудливым расположением ядер (чаще гиперхромных) обнаруживают при кори в конъюнктиве глаза, в эпителии бронхов, бронхиол, среди альвеолярных клеток; они образуют так наз. гигантоклеточные пневмонии (цветн. рис. 8). Г. к. макрофагального происхождения находят в миндалинах, в лимфатическом аппарате червеобразного отростка в продромальном периоде кори. При ветряной оспе Г. к. образуются в эпителии кожи на ранних стадиях формирования ветряночной везикулы. При вирусном гепатите среди печеночного эпителия образование много-ядерных Г. к. свидетельствует о начинающихся процессах регенерации.
Диагностический интерес представляет обнаружение так наз. цитомегалических клеток размером 20—30 мкм при вирусном поражении слюнных желез (цветн. рис. 9). Это одноядерные Г. к., характеризующиеся крупным внутриядерным включением, к-рое связывают с наличием самого вируса. При генерализованной цитомегалии Г. к. наблюдаются в эпителии слюнных желез, в легких, печени, почках, поджелудочной железе, надпочечниках и т. д.; возникают они преимущественно из эпителиальных клеток. Однако их можно наблюдать и среди клеток нервной и мезенхимальной ткани (головной мозг, тимус, лимф. узлы).
При лимфогранулематозе наблюдается образование одноядерных и многоядерных Г. к. из макрофагов. Образование Г. к. соединительнотканного, эпителиального, неврогенного и мышечного происхождения часто наблюдается в опухолях. Морфология этих Г. к. разнообразна, гистогенез связан с гистогенезом самих опухолей.
Гигантские клетки были обнаружены в культурах тканей. Так, А. Д. Тимофеевский в 1914 г. в культуре лейкемической крови наблюдал образование Г. к. из гематогенных макрофагов вокруг случайно попавших инородных тел.
При введении в эту культуру тканей туберкулезных бацилл были получены типичные Г. к. типа Пирогова—Лангханса.
В редких случаях наблюдается образование своеобразных миогенных Г. к. в миокарде при патологических процессах, сопровождающихся гибелью мышечных волокон (дистрофии, расстройства кровообращения, воспалительные процессы).
Гистогенез. Г. к. чаще всего возникают из гистио- и гематогенных макрофагов (см.) и из эпителия;
значительно реже они образуются из мышечной и нервной ткани. Г. к. эпителиального происхождения в норме иногда встречаются в эпителии мочевого пузыря. Они бывают двухядерными или многоядерными, причем в некоторых случаях из переходного эпителия мочевого пузыря (при развитии рака) появляется большое количество атипических Г. к. При болезнях накопления (энзимопатиях) образуются Г. к. неврогенного гистогенеза (см. Ниманна — Пика болезнь). Особого рода глобоидные многоядерные Г.к. патогномоничны для болезни Краббе, характеризующейся недостаточностью энзима галактоцереброзидазы (см. Лейкодистрофии); их происхождение возможно из гистиоцитов, т. к. эти Г.к. располагаются преимущественно вокруг мелких сосудов.
Условно к Г. к. неврогенного происхождения могут быть отнесены подошвы двигательных бляшек, которые представляют собой цитоплазменные образования, содержащие несколько ядер двух типов — более вытянутые, напоминающие ядра мышечных волокон, и округлые, напоминающие ядра клеток шванновской оболочки.
Гигантские клетки мезенхимального происхождения встречаются в норме у человека в костном мозге; к ним относят мегакариоциты и остеокласты. Остеокласты возникают из камбиальных элементов надкостницы; их образование регулируется гормоном околощитовидной железы. Они в большом количестве обнаруживаются в растущих костях.
Г. к. типа Пирогова—Лангханса и Г. к. типа инородных тел образуются из эпителиоидных клеток (гистиогенных макрофагов).
Причины образования Г. к. типа Пирогова—Лангханса и Г. к. инородных тел еще недостаточно выяснены. Имеются наблюдения, что некоторые хим. фракции туберкулезных палочек (А3-фосфатид, фосфорная к-та), особенно в сочетании со смесью жирных кислот, дают в эксперименте образование особенно большого количества Г. к. Высказывается точка зрения, что образование Г. к. типа Пирогова—Лангханса обратно пропорционально вирулентности самого возбудителя: при введении маловирулентной культуры у экспериментальных животных образуется большое количество Г. к. и малое число Г. к. при введении вирулентной культуры.
При лечении антибиотиками, когда падает вирулентность туберкулезной палочки, отмечается повышенное образование Г. к. типа Пирогова—Лангханса. Эти клетки с очень высокой ферментативной активностью и большим содержанием функциональных групп белка. Однако локализация и интенсивность реакций на белки и ферменты зависит от степени зрелости Г. к. Пирогова—Лангханса. Увеличение объема ядрышек в этих клетках является свидетельством медленного синтеза РНК, увеличение числа митохондрий свидетельствует о высоком уровне окислительных процессов. Известно, что Г. к. инородных тел и Г. к. типа Пирогова—Лангханса не возникают в условиях острого воспаления. Их появление связано с пролиферативными длительно текущими воспалительными процессами.
Причины образования Г. к. при вирусных инфекциях также изучены недостаточно. Частота обнаружения их в детском возрасте связана, по-видимому, с высокой пролиферативной способностью тканей именно в этом возрастном периоде. С другой стороны, на возникновение Г. к., очевидно, оказывают влияние сами вирусы, а большинство вирусных инфекций возникает именно в детском возрасте.
Механизм образования Г. к. трактуется различными авторами по-разному. Существует мнение, что они образуются синцитиальным путем, т. е. в результате слияния одноядерных клеточных форм; некоторые авторы считают, что они образуются пролиферативным путем, т. е. благодаря делению ядра с одновременным ростом цитоплазмы. Ряд авторов признает возможность образования Г. к. и тем, и другим способом.
Установлено, что оба способа образования Г. к. имеют место как в живом организме, так и в культуре тканей. Так, напр., образование Г. к. в культуре тканей из макрофагов идет путем слияния, образование Г. к. из эпителия и эндотелия сосудов — путем амитотического деления ядер и роста цитоплазмы, не сопровождающегося плазмотомией. В организме, напр., Г. к. типа Пирогова—Лангханса при туберкулезе образуются путем амитотического деления ядра с последующим ростом цитоплазмы; из печеночного эпителия при вирусном гепатите Г. к. образуются путем слияния клеточных тел.
Функциональное значение. Значение и роль Г. к. как активных фагоцитов впервые была выявлена И. И. Мечниковым. Все последующие наблюдения подтвердили фагоцитарную способность многих Г. к. Наличие Г. к. при инфекционных заболеваниях расценивается как проявление иммунной реакции клеточного типа; их образование зависит от высокой потребности организма в фагоцитарной деятельности. При этом фагоцитоз (см.) в Г. к. часто носит незавершенный характер (эндоцитобиоз), от к-рого зависит нестерильный иммунитет, напр, при туберкулезе. Очевидно, такого же характера роль Г. к. при вирусных инфекциях, особенно когда в Г. к. обнаруживаются вирусные включения (напр., при ветряной оспе, цитомегалии). Надо полагать, что здесь имеет место своеобразная форма внутриклеточного существования вируса.
Образование Г. к. в лейкемических инфильтратах при лечении цитостатическими средствами и рентгеновскими лучами, в частности при хроническом миелолейкозе, не имеет пока должного объяснения, предполагают, что здесь играет роль проявление клеточного иммунного ответа.
Г. к. могут фагоцитировать не только микробы, но всевозможные продукты распада и обмена (белкового, липоидного, минерального, пигментного) в организме. А. В. Немилов обнаружил Г. к. у животных и человека в селезенке и в лимфатических узлах, где они возникали в старческом возрасте в ответ на появление продуктов распада. Следовательно, Г. к. играют в организме роль не только активных фагоцитов при разного рода инфекционных процессах, но принимают активное участие в обменных процессах.
Образование Гигантских клеток имеет значение при регенерации тканей, о чем свидетельствует появление их при регенерации скелетной мускулатуры, печеночной ткани, при проявлениях регенераторных процессов со стороны мышечных волокон миокарда.
Библиография: Ван Фюрт Р. и др. Система мононуклеарных фагоцитов, новая классификация макрофагов, моноцитов и их клеток предшественников, Бюлл. ВОЗ, т. 46, № 6, с. 814, 1973, библиогр.; Гистология, под ред. В. Г. Елисеева и др., М., 1972; Подвысоцкий В. В. О разъедании омертвевших участков печеночной ткани гигантскими клетками гепатофагами, Врач, № 3, с. 1,1889; Струков А. И. Патологическая анатомия, М., 1971; Шройт И. Г. Экспериментальная корь, патоморфология и патогенез, Кишинев, 1961, библиогр.; Fаllis В. D. Textbook of pathology, N. Y., 1964; Langhan s T. Uber Riesenzellen mit wand-standigen Kernen in Tuberkeln und die fibrose Form des Tuberkels, Virchows Arch. path. Anat., Bd 42, S. 382, 1868.