калий оаш что это
Гидроксид калия: способы получения и химические свойства
Гидроксид калия KOH — неорганическое соединение. Белый, гигроскопичный, плавится и кипит без разложения. Хорошо растворяется в воде.
Относительная молекулярная масса Mr = 56,11; относительная плотность для тв. и ж. состояния d = 2, 044; tпл = 404º C; tкип = 1324º C
Способы получения
1. Гидроксид калия получают электролизом раствора хлорида калия :
2KCl + 2H2O → 2KOH + H2 + Cl2
2. При взаимодействии калия, оксида калия, гидрида калия и пероксида калия с водой также образуется гидроксид калия:
2K + 2H2O → 2KOH + H2
2KH + 2H2O → 2KOH + H2
3. Карбонат калия при взаимодействии с гидроксидом кальция образует гидроксид калия:
Качественная реакция
Химические свойства
1. Гидроксид калия реагируют со всеми кислотами (и сильными, и слабыми, и растворимыми, и нерастворимыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов:
в растворе образуется комплексная соль — тетрагидроксоалюминат:
4. С кислыми солями гидроксид калия также может взаимодействовать. При этом образуются средние соли, или менее кислые соли:
5. Гидроксид калия взаимодействует с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода).
При этом кремний окисляется до силиката и выделяется водород:
Фтор окисляет щелочь. При этом выделяется молекулярный кислород:
Другие галогены, сера и фосфор — диспропорционируют в растворе гидроксида калия:
Сера взаимодействует с гидроксидом калия только при нагревании:
В растворе образуются комплексная соль и водород:
2KOH + 2Al + 6Н2О = 2K[Al(OH)4] + 3Н2
Хлорид меди (II) реагирует с гидроксидом калия с образованием хлорида калия и осадка гидроксида меди (II):
2KOH + CuCl2 = Cu(OH)2↓+ 2KCl
NH4Cl + KOH = NH3 + H2O + KCl
KOH ↔ K + + OH —
4KOH → 4K + O2 + 2H2O
Гидроксид калия
Гидроксид калия – это щелочь, которую в пищевой промышленности называют добавкой Е525.

Применение гидроксида калия в качестве пищевой добавки разрешено в странах ЕС, в России, Украине.
Свойства гидроксида калия
Внешне гидроксид калия представляет собой кристаллические бесцветные палочки, шарики, хлопья.
Добавка Е525 плавится при температуре 404 °C, быстро впитывает влагу и поэтому требует создания особых условий хранения, растворяется в метаноле, этаноле и воде.
Гидроксид калия может растворять органические материалы.
Получение гидроксида калия проводят методом электролиза раствора калий хлора. На вещество воздействуют полимерным, асбестовым или ртутным катодом. Последний способ применяется чаще всего, хотя более безопасными считаются первые два способа получения гидроксида калия, не использующие ртуть.
Добавка Е525 считается сильным веществом, вступающим в бурную реакцию с оловом, алюминием, цинком, свинцом и кислотами.
В пищевой промышленности используют такое свойство гидроксида калия как способность влиять на кислотность продуктов. По сути, добавка Е525 – это регулятор кислотности.
Применение гидроксида калия
Если брать во внимание исключительно пищевую промышленность, то здесь, чаще всего, Е525 используют производители шоколада, какао и продукции из них.
Помимо этого, гидроксид калия может встречаться в составе продуктов детского питания, им обрабатывают замороженный картофель.

В косметической промышленности гидроксид калия применяют для производства шампуней, мыла, отбеливателей, средств для бритья.
Вред гидроксида калия
Работая на производстве с добавкой Е525 нельзя забывать о том, что это все-таки щелочь, которая относится ко второму классу опасности. Гидроокись калия может разъедать кожу и слизистые, вызывая химические ожоги. Избыток гидроксида калия, то есть длительный контакт с веществом провоцирует появление хронических кожных заболеваний.
На производстве, применяющем гидроксид калия, должны быть предприняты серьезные меры предосторожности. Особенно опасен контакт щелочи с глазами человека – зафиксированы случаи полной потери зрения.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Американские ученые провели опыты на мышах и пришли к выводу, что арбузный сок предотвращает развитие атеросклероза сосудов. Одна группа мышей пила обычную воду, а вторая – арбузный сок. В результате сосуды второй группы были свободны от холестериновых бляшек.
Средняя продолжительность жизни левшей меньше, чем правшей.
Печень – это самый тяжелый орган в нашем теле. Ее средний вес составляет 1,5 кг.
Большинство женщин способно получать больше удовольствия от созерцания своего красивого тела в зеркале, чем от секса. Так что, женщины, стремитесь к стройности.
Препарат от кашля «Терпинкод» является одним из лидеров продаж, совсем не из-за своих лечебных свойств.
Если улыбаться всего два раза в день – можно понизить кровяное давление и снизить риск возникновения инфарктов и инсультов.
Человек, принимающий антидепрессанты, в большинстве случаев снова будет страдать депрессией. Если же человек справился с подавленностью своими силами, он имеет все шансы навсегда забыть про это состояние.
Вес человеческого мозга составляет около 2% от всей массы тела, однако потребляет он около 20% кислорода, поступающего в кровь. Этот факт делает человеческий мозг чрезвычайно восприимчивым к повреждениям, вызванным нехваткой кислорода.
В течение жизни среднестатистический человек вырабатывает ни много ни мало два больших бассейна слюны.
Кроме людей, от простатита страдает всего одно живое существо на планете Земля – собаки. Вот уж действительно наши самые верные друзья.
74-летний житель Австралии Джеймс Харрисон становился донором крови около 1000 раз. У него редкая группа крови, антитела которой помогают выжить новорожденным с тяжелой формой анемии. Таким образом, австралиец спас около двух миллионов детей.
Раньше считалось, что зевота обогащает организм кислородом. Однако это мнение было опровергнуто. Ученые доказали, что зевая, человек охлаждает мозг и улучшает его работоспособность.
Во время работы наш мозг затрачивает количество энергии, равное лампочке мощностью в 10 Ватт. Так что образ лампочки над головой в момент возникновения интересной мысли не так уж далек от истины.
Общеизвестный препарат «Виагра» изначально разрабатывался для лечения артериальной гипертонии.
Каждый из нас слышал истории о людях, которые никогда не чистили зубы и не имели при этом проблем. Так вот, скорее всего, эти люди либо не знали о наличии у себ.
Гидроксид калия ГОСТ 24363-80
| Гидроксид калия | |
|---|---|
 | |
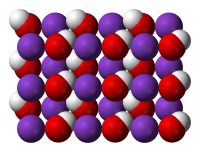 | |
| Систематическое наименование | Гидроксид калия |
| Традиционные названия | Кали едкое, каустический поташ |
| Хим. формула | KOH |
| Состояние | твёрдое |
| Молярная масса | 56,1056 г/моль |
| Плотность | 2,044−2,12 г/см³ |
| Т. плав. | 380−406 °C |
| Т. кип. | 1327 °C |
| Энтальпия образования | −425,8 кДж/моль |
| Энтальпия плавления | 7,5 кДж/моль |
| Энтальпия кипения | 128,9 кДж/моль |
| Давление пара | 1 ± 1 мм рт.ст. |
| Растворимость в воде | 117,9 г/100 мл |
| Растворимость в спирте | 38,7 (28 °C) |
| Показатель преломления | 1.409 |
| Рег. номер CAS | ГОСТ 24363-80 ГОСТ 9285-78 |
| Рег. номер CAS | 1310-58-3 |
| PubChem | 14797 |
| Рег. номер EINECS | 215-181-3 |
| SMILES | |
| Кодекс Алиментариус | E525 |
| RTECS | TT2100000 |
| ChEBI | 32035 |
| Номер ООН | 1813 |
| ChemSpider | 14113 |
| Пиктограммы СГС |  |
| NFPA 704 | |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Тривиальные названия: едкое кали, каустический поташ, а также гидрат окиси калия, гидроокись калия, калиевая щёлочь, калиевый щёлок.
Бесцветные, очень гигроскопичные кристаллы, но гигроскопичность меньше, чем у гидроксида натрия. Водные растворы KOH имеют сильнощелочную реакцию. Получают электролизом растворов KCl, применяют в производстве жидких мыл, для получения различных соединений калия.
Содержание
Химические свойства
Гидроксид калия получают электролизом растворов KCl, обычно с применением ртутных катодов, что дает продукт высокой чистоты, не содержащий примеси хлоридов:
2KCl + 2H2O ⟶ 2KOH + H2↑ + Cl2↑
Применение
Гидроксид калия является практически универсальным химическим соединением. Ниже приведены примеры материалов и процессы в которых он используется:
В пищевой промышленности обозначается как пищевая добавка E525. Используется как регулятор кислотности, в качестве осушителя и средства для снятия кожицы с овощей, корнеплодов и фруктов. Он также используется в качестве катализатора в некоторых реакциях.
Также используется для получения метана, поглощения кислотных газов и обнаружения некоторых катионов в растворах.
Популярное средство в производстве косметической продукции, вступая в реакцию с жирными маслами расщепляется и омыливает при этом масла.
В циркониевом производстве используется для получения обесфторенного гидроксида циркония.
В сфере промышленной мойки продукты на основе гидроксида калия, нагретые до 50-60 °С, применяются для очистки изделий из нержавеющей стали от жира и других масляных веществ, а также остатков механической обработки.
Используется в качестве электролита в щелочных (алкалиновых) батарейках.
Также применяется в ресомации — альтернативном способе «захоронения» тел.
5 % раствор гидроксида калия используется в медицине для лечения бородавок.
В фотографии используется как компонент проявителей, тонеров, индикаторов тиосульфатов и для удаления эмульсии с фотографических материалов.
Производство
В промышленном масштабе гидроксид калия получают электролизом хлористого калия.
Возможны три варианта проведения электролиза:
В ряду электрохимических методов производства самым легким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути. Мембранный метод производства самый эффективный, но и самый сложный.
В то время как диафрагменный и ртутный методы были известны соответственно с 1885 и 1892 гг., мембранный метод появился сравнительно недавно — в 1970 гг.
Основной тенденцией в мировом производстве гидроксида калия в последние 10 лет является переход производителей на мембранный метод электролиза. Ртутный электролиз является устаревшей, экономически невыгодной и негативно действующей на окружающую среду технологией. Мембранный электролиз полностью исключает использование ртути. Экологическая безопасность мембранного метода заключается в том, что сточные воды после очистки вновь подаются в технологический цикл, а не сбрасываются в канализацию.
При использовании данного метода решаются следующие задачи:
Мировым лидером в области мембранных технологий является японская компания «Асахи Касэй».
В России производство гидроксида калия осуществляется мембранным (ООО «Сода-Хлорат») методом.
Особенностью технологического оформления производства гидроксида калия является тот факт, что на аналогичных установках электролиза можно выпускать как едкое кали, так и каустическую соду. Это позволяет производителям без существенных капиталовложений переходить на производство гидроксида калия взамен каустической соды, производство которой не столь рентабельно, а сбыт в последние годы усложняется. При этом в случае изменений на рынке возможен безболезненный перевод электролизёров на производство ранее выпускавшегося продукта.
Примером перевода части мощностей с производства гидроксида натрия на гидроксид калия может служить ОАО «Завод полимеров КЧХК», начавший промышленный выпуск едкого кали на пяти электролизерах в 2007 году.
Опасность
Очень сильная щёлочь. В чистом виде действует на кожу и слизистые оболочки прижигающим образом. Особенно опасно попадание даже малейших частиц гидроксида калия в глаза, поэтому все работы с этим веществом должны проводиться в резиновых перчатках и очках. Гидроксид калия разрушает бумагу, кожу и др. материалы органического происхождения.
Едкий калий или «Едкое кали» — реактив с говорящим названием
Едкий калий (гидроксид калия) — сильная щелочь, которая получила 
Свойства
Гидроокись калия (КОН) — бесцветный порошок, состоящий из чешуек или мелких кристаллов. Запаха не имеет, очень гигроскопичный. На воздухе кристаллы быстро «оплывают», поэтому хранить вещество необходимо в герметично укупоренной таре. Реактив хорошо растворяется в воде, спиртах. Активно вступает в реакции с металлами, кислотными оксидами и газами, органическими и неорганическими кислотами, органическими соединениями.
Калиевая щелочь негорюча и взрывобезопасна, но опасна для человека. При попадании на кожу или в глаза вызывает долго незаживающие ожоги и даже потерю зрения, поэтому работать с ней допускается только в резиновых перчатках, прорезиненном костюме и специальных очках, защищающих от случайных брызг опасного реактива.
Гидроксид калия способен разрушать стекло (растворы) и фарфор (расплавы). Хранят и транспортируют растворы и твердое вещество в стальных емкостях или полиэтиленовых мешках.
Калиевую щелочь получают гидролизом хлорида калия.
Гидроксид калия выпускается как в виде растворов, так и в твердой форме (хлопья, гранулы).
Применение едкого кали

— В химической промышленности — в органическом и неорганическом синтезе; как сырье для получения соединений калия (например, двуокиси калия, перманганата калия), красителей; в качестве катализатора; в производстве удобрений и пестицидов, инсектицидов, гидроокиси циркония, метана, искусственного каучука; для осушения жидкостей, а также газов, с которыми KOH не вступает в реакцию.
— Поглощение кислых газов (углекислоты, сероводорода, диоксида серы).
— В лабораторной практике калиевая щелочь используется в титровании для обнаружения некоторых катионов, для определения концентрации кислот; для нейтрализации кислот.
— Обработка целлюлозы в производстве синтетических волокон; используется для придания хлопковым тканям лучшей впитываемости.
— В качестве пеногасителя на предприятиях производства бумаги.
— В резиновой промышленности — для обработки крошки каучука.
— В пищевой индустрии — в качестве регулятора кислотности (разрешенная в РФ и ЕС добавка Е 525) при изготовлении шоколада и шоколадных изделий; для обработки замороженного картофеля; для чистки овощей, корнеплодов и фруктов, в том числе для детского питания.
— В электротехнике хим. реактив применяют в щелочных аккумуляторах и в 
— В нефтехимии — для приготовления буровых растворов; в перегонке нефти.
— Для выщелачивания отливок на сталелитейных предприятиях.
— Используется для регулирования рН, очистки сточных вод.
— В промышленной очистке изделий из нержавеющей стали от жиросодержащих загрязнений, следов механической обработки.
— В быту — входит в состав средств для мытья нержавейки.
— Для ресомации (метод аналогичный кремации, но на химической основе).
— Применяется для травления кристаллов кремния в микроэлектронике.
— В фармацевтике, стоматологии, медицине (нейтрализация кислотных ожогов).
— В строительстве — при изготовлении штукатурок, побелок, гипсовых растворов.
Наш интернет-магазин предлагает купить калий гидроокись производства Франции, а также другие химические реактивы в розницу и оптом. Широкий ассортимент и доступные цены, при необходимости быстрая доставка по Москве и Московской области — все это делает сотрудничество с «ПраймКемикалсГрупп» удобным.
Гидроксид калия: описание, вред и польза, применение
Гидроксид калия – это вещество, принадлежащее к классу соединений, не включающих в свою структуру углерод: то есть, неорганических. В различных сферах гидроксид калия носит разные названия: едкое кали, каустический поташ, гидроокись калия, калиевая щелочь и калиевый щелок.
Внешне вещество похоже на кокосовую стружку: как правило, его реализуют в виде белых плотных хлопьев. Вещество обладает высокой способностью к впитыванию влаги, а водные растворы гидроокиси калия имеют сильную щелочную реакцию. Помимо влаги, калиевая щелочь с легкостью поглощает воздух. Вещество получают посредством электролиза раствора хлорида калия. Наибольшую популярность гидроксид калия заработал в производстве уходовой косметики, в частности – жидкого мыла.
При растворении кристаллов происходит выделение большого количества тепла. Стоит отметить, что данное соединение принадлежит к категории токсичных веществ и относится ко второму классу опасности. В работе с кристаллами важно соблюдать определенные правила, дабы уберечься от негативного воздействия. В случае контакта гидроксида калия с кожей образуются серьезные ожоги. При попадании кристаллов в глаза, велик риск потери зрения.
Что такое гидроксид калия: его особенности
Гидроксид калия – это щелочь, заработавшая большую популярность в пищевой промышленности. В производстве продуктов питания она известна под индексом Е525. Использование добавки официально разрешено на всей территории Европейского Союза и в России.
Как правило, гидроксид калия представлен небольшими плотными хлопьями белого цвета, но это не единственная его форма. Выпускают соединение также в форме бесцветных палочек и шариков.
В пищевой промышленности вещество получают посредством электролиза хлористого калия. Вещество используется в производстве продуктов питания в роли регулятора кислотности и осушителя. Оно необходимо для упрощения процедуры снятия кожицы с плодов и ускорения протекания некоторых реакций.
Рассматриваемое вещество применяется для производства метана, поглощения кислотных газов и определения присутствия катионов в растворах. Часто его можно встретить в косметических продуктах: вещество легко вступает в реакцию с жирами.
Лидерами по производству гидроксида калия считаются Франция, Южная Корея и Китай.
Формула гидроксида калия и его свойства
Формула рассматриваемого вещества выглядит следующим образом: KOH.
Молекула гидроксида калия
Физические свойства гидроксида калия
Для вещества характерно твердое агрегатное состояние, но оно может изменяться в определенных условиях. Визуально вещество выглядит как небольшие кристаллы или хлопья, не имеющие ни цвета, ни запаха.
Вещество может выглядеть и иначе – все зависит от конкретной марки и сорта. Так, твердая добавка высшего сорта представляет собой зеленоватые или сиреневатые чешуйки, соединение первого сорта может иметь серый цвет. Жидкая калиевая щелочь первого и второго сорта – голубоватый, зеленоватый или сероватый раствор, в некоторых случаях допускается присутствие осадка.
Гидроксид калия обладает крайне высокой гигроскопичностью – он моментально впитывает воздух и жидкость. При долгом нахождении на открытом воздухе вещество принимает вид раствора – такой эффект достигается благодаря поглощению влаги из окружающей среды. Аналогично ведет себя и каустическая щелочь – ее гигроскопичность даже выше.
Порошок и хлопья начинают плавиться при температуре в 404 градуса. Прекрасно растворяется в спиртосодержащей среде и в обычной питьевой воде.
Химические свойства
Гидроксиду калия присущи те же свойства, что и основаниям. Особенно ярко выражены щелочные свойства рассматриваемого соединения. В процессе горения образуются оксид и обычная вода. Оксид обладает характерным желтым цветом.
Соединение не воспламеняется и не взрывается. Однако по степени отрицательного воздействия на организм человека принадлежит ко 2 классу. При попадании на кожу гидроксид калия вызывает тяжелые химические ожоги, а при контакте со слизистой глаз – нарушение зрения. Кроме того, гидроксид калия способен провоцировать развитие кожных заболеваний.
Получение гидроксида калия
Существует несколько способов получения пищевой добавки. Наиболее часто в промышленности используют метод электролиза водных растворов хлорида калия. Выделение электродов может происходить с добавлением твердого асбестового катода или ртутного катода. Твердый асбестовый катод используют при мембранном способен получения рассматриваемого соединения.
Ртутные катоды применяются в разы чаще, поскольку они дают возможность получить более чистое вещество с минимальным количеством примесей. Однако безопасным данный метод назвать тяжело – если выбирать способ производства с точки зрения безопасности, предпочтение лучше отдавать мембранному. Несмотря на сложность процесса, риск для работников сводится к минимуму.
Мембранный метод появился в конце 20 века, а вот ртутный способ использовался намного дольше – впервые его применили еще в конце 19 века. Впрочем, в последнее время ртутный способ утрачивает свою популярность: применение ртутных катодов не только не выгодно с точки зрения экономии, но и опасно для окружающей среды.
С точки зрения экологии мембранный метод лучше: технологический процесс подразумевает поступление сточных вод с новый цикл, а не их сброс в канализацию. Соответственно, окружающая среда не испытывает абсолютно никакого вреда. Мембранная методика позволяет решить следующие вопросы: исключить стадию сжижения и испарения хлора, исключение газовых выбросов хлора.
Получение гидроксида калия электролизом раствора хлорида калия:
Гидроксид калия можно выделить посредством соединения оксида калия, гидрида калия и пероксида калия в водном растворе:
Реакции с гидроксидом калия
Калиевая щелочь легко вступает в реакцию с кислотными оксидами. По завершению образуются средние или кислые соли – финальный продукт зависит от соотношения реагентов. Так, если преобладает гидроксид калия: реакция выглядит следующим образом:
В случае преобладания оксида углерода уравнение выглядит так:
Помимо этого, гидроксид калия легко реагирует с амфотерными оксидами и гидроксидами. Конечным продуктом реакции являются соли – средние и комплексные:
Калиевая щелочь взаимодействует и с кислыми солями, в результате образуются менее кислые и средние соли:
Рассматриваемый химикат вступает в реакцию с простыми веществами. Исключение составляют только инертные газы азота, кислорода, водорода и углерода, в результате выделяется водород:
При добавлении щелочи происходит реакция окисления, по заверению которой выделяется кислород:
С серой вещество начинает взаимодействовать только при повышении температуры – в нормальных условиях вещества никак не реагируют друг с другом:
Рассматриваемое вещество вступает в обменные реакции с растворимыми солями. Так, например, при добавлении к щелочи хлорида меди происходит образование хлорида калия и осадка гидроксида меди:
Допустимые нормы употребления гидроксида калия
Допустимые дозировки указаны в нормативных документах, в частности – в СанПиН 2.3.2.1293-03 от 26.05.2008. Так, в продукты питания, как правило, добавляют совсем небольшое количество калиевой щелочи – в том объеме, в котором она присутствует в пище, добавка неспособна спровоцировать ухудшение состояния здоровья.
Гидроксид калия официально разрешен к использованию в производстве продуктов питания для разных групп населения в странах Европы, России, Канаде и Соединенных Штатах.
Сферы применения гидроксида калия
Гидроксид калия – это не только достаточно востребованная в современном мире пищевая добавка. Данное соединение применяется в самых разных сферах: диапазон настолько широк, что начинается промышленными масштабами и заканчивается бытовыми нуждами обычных людей.
Производство бумаги и уходовой косметики
Так, например, гидроксид калия востребован при производстве бумаги и картона, ещё его используют для улучшения протекания процесса омыления жиров. Благодаря этому свойству вещество часто используется производителями уходовой косметики и бытовой химии. Применять гидроксид калия в мыловарении начали очень и очень давно – примерно в 385 году до нашей эры. Тогда мыло варили из различных ароматных масел, соды и гидроксида калия.
Химическая промышленность
В химической промышленности вещество нужно для нейтрализации кислот, даже самых сильных, а также для ускорения протекания различных реакций. В нефтеперерабатывающей промышленности гидроксид калия важен для производства жиров.
Производство биодизельного топлива
Огромную популярность гидроксид калия получил в производстве биодизельного топлива, основой которого сложат растительные масла.
Устранение засоров в трубах
Гидроксид калия необходим для устранения засоров в трубах – он ускоряет процесс движения содержимого труб, частично растворяя его.
Гражданская оборона
В гражданской обороне гидроксид калия необходим для нейтрализации отравляющих веществ – он позволяет очистить вдыхаемый воздух и предотвратить отравление людей.
Развлекательная сфера (фокусы)
У рассматриваемого соединения есть и менее серьезные способы использования. Так, например, его часто применяют фокусники: благодаря способности изменять цвет меди, гидроксид натрия пользуется большой популярностью в фокусе с монеткой.
Пищевая промышленность
В пищевой промышленности гидроксид калия необходим для правильного мытья и очистки плодов. Ещё его используют в ходе производства
кондитерских изделий, размягчения маслин и оливок, выпечке хлеба.
Использование гидроксида калия в разных отраслях промышленности:
| Сфера промышленности | Назначение гидроксида калия |
| Целлюлозно-бумажная промышленность | Добавка отвечает за подготовку целлюлозы для дальнейшей работы: благодаря ей можно получить бумагу и картон высокого качества |
| роизводство бытовой химии и уходовой косметики | Гидроксид калия позволяет добиться устойчивой пены и улучшить процесс омыления жиров. Его часто можно встретить в составе моющих средств, мыла, шампуней и гелей для душа |
| Химическая промышленность | Вещество необходимо для нейтрализации кислот, оно также выступает в роли ускорителя процесса протекания реакций, применяется в химическом анализе |
| Производство биотоплива | Вещество регулирует правильность протекания химических реакций |
| Устранение засоров в трубах | Гидроксид калия растворяет застоявшиеся массы, упрощая процесс их движения по трубам |
| Гражданская оборона | Нейтрализация отравляющих веществ |
| Фокусы | Рассматриваемое вещество применяется в фокусе, в ходе которого медная монетка изменяет цвет |
| Пищевая промышленность | Приготовление десертов, хлеба, размягчение маслин и придание им насыщенного черного цвета, очистка овощей и фруктов от кожицы |
Влияние гидроксида калия на человека
Гидроксид калия может быть достаточно опасен в работе, но при его употреблении в составе продуктов питания никакого вреда организм получить не должен. Впрочем, о пользе добавки говорить тоже не приходится.
Исследования, проведенные зарубежными учеными на животных, показали, что чрезмерное употребление пищевой добавки может повлечь за собой развитие заболеваний кожного покрова. Несмотря на этом, все сведения о рекомендуемых объемах потребления рассматриваемого вещества довольно расплывчаты.
Гидроксид калия – это вещество, которое разрешено к применению в производстве продуктов питания во многих странах, Россия и Украина входят в их число, с ними в списке соседствуют все страны ЕС, США и Канада. Более того, соединение разрешено к применению в производстве детского питания, что говорит о его безопасности при употреблении в небольших количествах.
При контакте гидроксида калия с кожным покровом образуются глубокие химические ожоги, поэтому при работе с веществом необходимо использовать средства индивидуальной защиты.
Польза гидроксида калия
Рассматриваемая добавка не оказывает положительного влияние на организм человека.
Вред гидроксида калия
При употреблении вовнутрь в разумных количествах гидроксид калия безопасен. А вот при неосторожной работе с ним вы рискуете заработать ожоги, раздражение, нарушение работы органов зрения и т.д.
Где можно приобрести гидроксид калия и сколько он стоит
Проще всего приобрести гидроксид калия в режиме онлайн – в сети доступна масса интернет-магазинов, предлагающих широкий ассортимент пищевых добавок от самых разных производителей.
Онлайн-магазины предлагают своим клиентам различные способы оплаты: через Киви кошелек, банковским переводом и наличным расчетом.
1 кг добавки обойдется вам приблизительно в 300 рублей, за 5 кг гидроксида калия придется заплатить 1400 рублей, а за 10 кг – 2500 рублей.
Заключение
Гидроксид калия – это неорганическое вещество, широко применяющееся в разных отраслях промышленности. Внешне добавка представляет собой белый порошок или белые плотные хлопья. Наиболее крупные производства гидроксида калия расположены на территории Франции, Южной Кореи и Китая. Приобрести вещество проще всего в режиме онлайн: в интернет-магазинах представлены пищевые добавки от разных производителей.
Основным методом получения гидроксида калия считается электролиз. В зависимости от реагентов выделяют три основные методики получения добавки: с твердым асбестовым катодом, с полимерным катодом и с ртутным катодом. Последние два способа применяются реже, поскольку более затратны, менее экологичны и несут опасность для работников. Ртутный метод использовался в промышленности с 19 века и когда-то считался единственно верным, однако развитие науки и совершенствование химической отрасли позволило открыть другие способы. Однако, в некоторых странах ртутный метод все так же популярен. Так, например, его до сих пор используют в России.
В больших объемах гидроксид калия получают посредством электролиза хлористого калия. При этом существует три способа проведения реакции (они аналогичны тем, что описаны выше)
Гидроксид калия обознается в составе продуктов питания как Е525. Он считается относительно безопасной добавкой и разрешен к использованию на территории бывшего Советского Союза, США, Канады и всех стран Европы. Более того, на данный момент отсутствуют ограничения, запрещающие использовать рассматриваемое соединение в производстве детского питания.
А вот в работе с гидроксидом калия необходимо строго следовать правилам безопасности. Дело в том, что при попадании на открытые участки тела порошок способен провоцировать сильные ожоги. Он также является причиной развития высыпаний, раздражений и прочих кожных заболеваний. При попадании на слизистую оболочку глаз порошок и вовсе способен привести к потере зрения. Ощутить негативные последствия можно также при чрезмерном употреблении гидроксида калия.
Несмотря на это, бояться присутствия гидроксида калия в составе продуктов питания не стоит – в пищевой продукции его настолько мало, что ощутить хоть какой-то вред практически невозможно. Негативные последствия дадут о себе знать только в том случае, если вы будете употреблять в пищу чистую пищевую добавку.
Никакой пользы организму гидроксид калия не несет.
Помимо пищевой промышленности вещество применяют также для производства бумаги и картона – им обрабатывают целлюлозу; изготовления мыла, гелей для душа и бытовой химии – гидроксид натрия отвечает за их способность к образованию устойчивой пены. Встретить гидроксид натрия можно также в химической промышленности, во время прочистки труб, в гражданской обороне и других отраслях. Соединение применяют для нейтрализации кислот, изготовления буровых растворов, красителей и удобрений, очистки газов, перегонки нефти, регулирования кислотности раствором и производства синтетического каучука.



