кардиодиафрагмальная спайка справа что это
Кардиодиафрагмальная спайка справа что это
Диагностика образований, расположенных в проекции кардио-диафрагмальных углов.
Гренков Г. И., Медведский В. Е.
Витебский медицинский институт.
В проекции кардиодиафрагмальных углов может локализоваться достаточно большое количество патологических образований. Диагностическая значимость клинических проявлений этих образований, особенно на начальном этапе, незначительна. Только при увеличении их размеров появляются симптомы компрессионного медиастинального синдрома.
Среди разнообразных методов лучевой диагностики рентгенологический метод является ведущим в выявлении новообразований этой области. Он позволяет уточнить локализацию, форму и размеры образования, выявить взаимосвязь с окружающими органами. Однако детальный анализ патологии кардиодиафрагмального угла при обычной рентгенографии затруднителен. Это связано со своеобразием анатомо-топографических взаимоотношений органов этой области и большим числом заболеваний, локализующихся здесь. Применение дополнительных специальных методик рентгенологического исследования позволяет в большинстве случаев поставить правильный диагноз. Наибольшую диагностическую значимость имеет пневмомедиастинография, выполняемая в различные фазы дыхания. В отдельных случаях показана томография. Заслуживает интерес применение методики встречного контрастирования, когда газ вводится в средостение и брюшную полость одновременно. Определенный успех в диагностике опухолей и опухолевидных образований кардиодиафрагмального угла связан с внедрением в практику рентгеновской компьютерной томографии. Она значительно расширяет объем диагностической информации и у отдельных больных отпадает надобность в проведении сложных методов исследования, связанных с наложением пневмоперитонеума и пневмомедиастинума. Однако отсутствие достаточного количества подобной аппаратуры ограничивают широкое использование этой методики.
В проекции кардиодиафрагмального угла встречаются медиастинальные и абдоминомедиастинальные липомы, целомические кисты перикарда, парастернальные грыжи, лейомиомы пищеводно-желудочного соустья. Значительно реже находят гигантские опухоли вилочковой железы, тератодермоидные кисты. Симулировать опухолевые процессы кардиодиафрагмального угла могут кардиодиафрагмальные грыжи, ограниченная релаксация диафрагмы. С наибольшей частотой встречается правосторонняя локализация патологического процесса в области переднего кардиодиафрагмального угла.
Рентгенологическая семиотика липом разнообразна и зависит от их размеров Медиастинальные липомы чаще встречаются в проекции правого кардиодиафрагмального угла. Они имеют грушевидную форму, однородную структуру, четкие контуры. Газ, введенный в средостение, смещает патологическое образование и позволяет увидеть его дольчатую структуру, уточнить взаимоотношение с окружающими органами и тканями.
Абдоминомедиастинальные липомы (Рис. 1), проникая через щель Ларрея, располагаются в правом сердечно-диафрагмальном синусе. Это наиболее распространенная опухоль средостения. При рентгенологическом обследовании определяется тень полукруглой формы, средней интенсивности с ровным и четким краем. В боковой проекции тень прилежит к контуру передней грудной стенки. На пневмомедиастинограммах газ расслаивает опухоль на дольки. У отдельных больных может быть видна ножка опухоли, соединяющая медиастинальное и абдоминальное пространства. При дополнительном введении газа в брюшную полость наблюдается симптом “погружения”, когда расположенная выше медиастинальная часть липомы вследствие высокого стояния купола диафрагмы, как бы смещается в брюшную полость.

| Рис. 1. Абдомино-медиастинальная липома. |
Злокачественные жировые опухоли этой локализации встречаются редко и их симптоматика мало отличается от доброкачественных липом.
Целомические кисты перикарда (Рис. 2) — тонкостенные образования, развившиеся от отшнуровавшегося дивертикула. Содержанием кист является жидкость, подобная перикардиальной. Диаметр кист колеблется от 3-4 см до 10-15 см. Типичным признаком является тень полукруглой или полуовальной формы, связанная с куполом диафрагмы, сердцем или передней грудной стенкой. При многопроекционном исследовании они не отделяются от тени сердца. Контуры кист всегда четкие. Только наличие жировых включений, спаек приводит к неровности и угловатости контура. Для них характерна передаточная пульсация сердца. Они часто меняют форму при дыхании: удлиняются при вдохе, уплощаются при выдохе. В условиях пневмомедиастинума эти образования отчетливо отделяются от всех окружающих органов и тканей полоской газа. Серьезные дифференциально-диагностические трудности возникают в случаях, когда кисты достигают больших размеров. Их дифференцируют с липомами, диафрагмальной грыжей, осумкованным плевритом, релаксацией купола диафрагмы.

| Рис. 2. Целомическая киста перикарда. |
В парастернальных грыжах находят фрагменты тонкой или толстой кишок, желудка, сальника, печени. В тех случаях, когда грыжевой мешок содержит полые органы, основным признаком грыжи становится появление тени ячеистого, неоднородного образования, связанного с передней грудной стенкой. Исследование желудочно-кишечного тракта в таких случаях дает возможность увидеть контрастированные кишечник или желудок, расположенные в грыжевом мешке. Газ, введенный в брюшную полость, проникает в грыжевой мешок и на его фоне становится хорошо видимой тень сальника или фрагмент печени.
Лейомиомы пищеводно-желудочного соустья, достигнув больших размеров, могут быть видимыми в проекции кардиодиафрагмальных углов. Контрастное исследование пищевода разрешает диагностические трудности. Лейомиомы дают овальной формы дефект наполнения с неровными, но четкими контурами на фоне сохраненного рельефа слизистой оболочки.
Тимомы больших размеров могут занимать все средостение и выходить в проекцию кардиодиафрагмальных углов. При этом находят затемнение сравнительно однородной структуры с волнистыми с волнистыми очертаниями, что отражает дольчатое строение опухоли. На пневмомедиастинограммах уточняют форму и размеры опухоли и ее загрудинную локализацию. Определенное значение имеет своеобразная клиническая картина течения заболевания.
Тератодермоидные образования (Рис. 3) содержат разнообразные ткани. Очень важным признаком, позволяющим установить правильный диагноз, является наличие в толще опухоли плотных включений и краевых обызвествлений. Эти новообразования часто инфицируются и нагнаиваются, в связи с чем формируются спайки, которые связывают опухоль с окружающими тканями.

| Рис. 3. Терато-дермоидная киста средостения. |
Рентгенологическая картина затемнений, обусловленных диафрагмальными грыжами, зависит от того, какие органы содержатся в грыжевом мешке. Патологическая тень при диафрагмальных грыжах прилежит к диафрагме и смещается вместе с ней. При этом возможно изменение формы тени. Выпадение кишечника (Рис. 4) или желудка позволяют увидеть на фоне неравномерного затемнения участки просветлений, горизонтальные уровни жидкости. Контрастное исследование желудка и кишечника обнаруживает эти органы в грудной полости. Наличие в грыжевом мешке паренхиматозных органов дает гомогенное затемнение. Решающее диагностическое значение в таких случаях имеет наложение диагностического пневмоперитонеума. Введенный газ проникает в грыжевой мешок и располагается между диафрагмой и паренхиматозным органом.

| Рис. 4. Диафрагмальная грыжа слева. Содержит петлю толстой кишки. |
При ограниченных релаксациях купола диафрагмы определяется ее полуовальное выпячивание с ровным и четким контуром, нередко можно обнаружить так называемый симптом “пересекающихся дуг” различных мышечных групп диафрагмы. Возможно наблюдать парадоксальное движение релаксированного участка диафрагмы по отношению к остальному.
Хронический адгезивный перикардит (I31.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Этиология и патогенез
Клиническая картина
Cимптомы, течение
Диагностика
Рентгенологический и рентгенокимографический методы исследования позволяют подтвердить наличие перикардиальных спаек и спаек между перикардом и соседними органами.
Диагностике слипчивого перикардита может помочь выявление грубых экстраперикардиальных сращений или отложений в рубцовой ткани извести. Обызвествление перикарда происходит обычно в определенной последовательности: коронарная борозда, правый желудочек, правое предсердие, левые желудочек и предсердие. В случае несдавливающих форм адгезивного перикардита участки обызвествления встречаются в 5-10% случаев. Они могут быть мелкими или парциальными.
При обычной рентгеноскопии грудной клетки возможно установить только распространенное обызвествление перикарда, когда оно охватывает также левую половину сердца. Частичное обызвествление обнаруживается только при целеустремленном исследовании со снимками сердца в разных проекциях, обычно в виде тонкой полоски по контуру сердца.
При рентгенологическом исследовании обычно хорошо видны спайки перикарда с плеврой и диафрагмой. Контур сердца приобретает зубчатый характер. Сращение сердца с диафрагмой образует лентообразную тень, сердце опущено и тесно прилежит к диафрагме. При дыхательных экскурсиях сердце оказывается фиксированным и не меняет конфигурации.
Лабораторная диагностика
Дифференциальный диагноз
По данным ЭхоКГ объем желудочков при перикардите нормальный, фракция выброса близка к норме или незначительно снижена. Раннее диастолическое наполнение желудочков резко преобладает над систолой предсердий. Ранний кровоток через митральное отверстие снижается на вдохе.
При рестриктивной кардиомиопатии колебаний диастолического кровотока в зависимости от фаз дыхания нет. Отсутствуют признаки утолщения перикарда и его обызвествления.
На компьютерной томографии при перикардите определяется утолщение перикарда более чем на 3 мм. При рестриктивной кардиомиопатии перикард не изменен.
Осложнения
Лечение
При развитии слипчивого перикардита с признаками венозного застоя, в случае неэффективности лекарственной терапии в течение 2-3 месяцев, проводят операцию по удалению сращений перикарда (перикардэктомия).
Для устранения острых проявлений заболевания и профилактики рецидивов эффективен также колхицин в дозе 0,5 мг 2 раза/сутки. Назначается в качестве монотерапии или в сочетании с НПВС. Он лучше переносится и дает меньше побочных эффектов, по сравнению с НПВС.
Системное использование кортикостероидов должно быть ограничено у больных с заболеваниями соединительной ткани, аутореактивным или уремическим перикардитом. Высокоэффективно внутриперикардиальное введение кортикостероидов, позволяющее избежать побочных эффектов, возникающих при системном применении. При постепенном уменьшении дозы преднизолона необходимо рано назначить ибупрофен или колхицин. Если необходимы антикоагулянты, рекомендуется гепарин под строгим контролем.
Заболевания плевры: диагностика и лечение
Заболевания плевры часто встречаются в общей практике и могут отражать широкий диапазон лежащих в их основе патологических состояний, затрагивающих легкие, грудную стенку, а также системных болезней. Самое распространенное их проявление
Заболевания плевры часто встречаются в общей практике и могут отражать широкий диапазон лежащих в их основе патологических состояний, затрагивающих легкие, грудную стенку, а также системных болезней. Самое распространенное их проявление заключается в образовании плеврального выпота, и у подавляющего большинства таких больных необходимы рентгенологическое подтверждение и дальнейшее обследование. Последние достижения, касающиеся методов получения изображения органов грудной клетки, терапии и хирургии, позволили усовершенствовать диагностику и лечение больных с патологией плевры.
Плевра дает грудной клетке возможность придавать легким необходимую форму и приводить их в движение с минимальными затратами энергии. Для чего два плевральных листка (париетальный и висцеральный) должны скользить один по другому — этому процессу способствует небольшое количество (0,3 мл/кг) жидкости.
Плевральная жидкость фильтруется из мелких сосудов париетальной плевры в плевральную полость и реабсорбируется лимфатическими сосудами этого же листка. Экспериментальные данные показывают, что объем и состав плевральной жидкости в норме очень стабильны, и выпот возникает только в тех случаях, если скорость фильтрации превышает максимальный отток лимфы либо нарушено обратное всасывание [1].
Плевральный выпот
Плевральные выпоты традиционно подразделяются на транссудаты (общий белок 30 г/л). В промежуточных случаях (а именно, когда содержание протеина составляет 25–35 г/л) разграничить экссудат и транссудат помогает определение содержания в плевральной жидкости лактатдегидрогеназы (ЛДГ) и градиента альбумина между сывороткой и плевральной жидкостью.
Наиболее часто встречающиеся причины и характерные признаки плевральных выпотов приведены в таблицах 1 и 2. Их дифференциация важна потому, что «низкобелковые» выпоты (транссудаты) не требуют дальнейших диагностических мероприятий; необходимо лишь лечение вызвавшей их патологии, в то время как при обнаружении плеврального экссудата, безусловно, нужна дополнительная диагностика.
Выпоты могут быть односторонними или двусторонними. Последние часто выявляются при сердечной недостаточности, но могут также возникать при гипопротеинемических состояниях и при коллагенозах с поражением сосудов. Имеют очень большое значение тщательный сбор анамнеза, включая профессию, данные о путешествиях за границу и о факторах риска тромбоэмболии, а также внимательное полноценное физикальное обследование.
При физикальном обследовании обнаруживается ограничение дыхательных движений грудной клетки, «каменная» тупость при перкуссии, приглушение дыхания при аускультации и часто — зона бронхиального дыхания сверху от уровня жидкости.
Небольшие выпоты следует дифференцировать с утолщением плевры. Помочь в этом может выполнение рентгенограммы в положении лежа (при этом жидкость движется под действием силы тяжести), а также ультразвуковое исследование (УЗИ) или рентгеновская компьютерная томография (КТ).
И УЗИ, и КТ являются ценными методами, которые все чаще используются для дифференциации между плевральной жидкостью, «окутанным» легким (плевральными бляшками, обычно возникающими при воздействии асбеста) и опухолью. Эти методы позволяют также выяснить, является ли плевральная жидкость осумкованной, и наметить оптимальное место для плевральной пункции и биопсии.
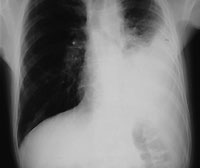 |
| Рисунок 1. Рентгенограмма органов грудной клетки: виден расширенный пищевод с уровнем жидкости и левосторонний плевральный выпот. Эти изменения были расценены как вторичная эмпиема, возникшая на фоне аспирационной пневмонии |
Плевральная пункция с аспирацией и биопсия показаны всем больным с выпотом, при этом удается получить гораздо больше диагностической информации, чем только при аспирации, и избежать проведения повторной инвазивной процедуры (см. рис. 1).
Другие исследования, помогающие в установлении диагноза, включают повторную рентгенографию органов грудной клетки после аспирации для выявления лежащей в основе выпота патологии легких, КТ, изотопное сканирование легких (с определением соотношения вентиляции и перфузии), внутрикожные пробы с туберкулином, серологические исследования на ревматоидные и антиядерные факторы.
Если вышеперечисленные методы не позволяют выявить причину возникновения плевральных выпотов, проводится торакоскопия с помощью видеотехники. Она позволяет не только осмотреть плевру, но также выявить опухолевые узлы и осуществить прицельную биопсию. Эта процедура наиболее ценна для диагностики мезотелиомы. Как бы то ни было, у 20% больных с экссудативными плевральными выпотами посредством обычных исследований не удается диагностировать причину развития данного состояния.
Лечение патологии, провоцирующей развитие плеврального выпота, например сердечной недостаточности или тромбоэмболии легочных артерий, часто приводит к его исчезновению. Некоторые состояния, включая эмпиему и злокачественные опухоли, требуют особых мер, о которых речь пойдет ниже.
Парапневмонические выпоты и эмпиема
Приблизительно у 40% больных с бактериальными пневмониями развивается сопутствующий плевральный выпот [11]; в таких случаях необходимо провести плевральную пункцию, чтобы удостовериться, что нет эмпиемы, и предотвратить либо уменьшить степень последующего утолщения плевры.
Однако у 15% пациентов парапневмонические выпоты вторично инфицируются, развивается эмпиема, то есть образуется гной в плевральной полости (см. рис. 2).
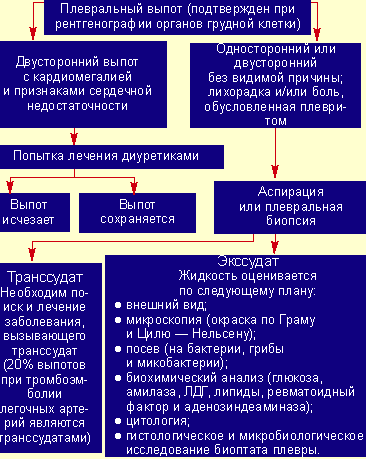 |
| Рисунок 2. Исследования при плевральном выпоте |
Другие причины эмпиемы включают хирургические вмешательства (20%), травмы (5%), перфорации пищевода (5%) и субдиафрагмальные инфекции (1%) [12].
 |
| Таблица 3. Микроорганизмы: возбудители эмпиемы |
При эмпиемах большая часть высеваемых культур представлена аэробными микроорганизмами. Анаэробные же бактерии высеваются в 15% случаев эмпием, обычно являющихся осложнением аспирационных пневмоний; остальные случаи обусловлены разнообразными другими микроорганизмами (см. табл. 3). Если до плевральной пункции назначались антибиотики, посевы часто не дают роста.
Диагноз подтверждается на основании рентгенологических признаков осумкованного плеврита или в случае обнаружения гноя в плевральном пунктате (см. табл. 2).
Кроме того, под контролем УЗИ или КТ следует наладить дренаж из наиболее низкой части эмпиемы и соединить его с подводным клапанным механизмом. В прошлом рекомендовалось использовать дренажи относительно большого диаметра, однако сегодня применение более узких трубок признано эффективным при меньшей травматичности для пациентов.
Рекомендации относительно целесообразности применения фибринолитиков основаны на результатах небольших неконтролированных исследований, согласно которым частота ликвидации спаек составила 60–95% [13, 14], а потребность в хирургических вмешательствах значительно уменьшилась. Тем, что до сих пор не проведено контролированных исследований, объясняется некоторая неопределенность относительно того, когда, как долго и в каких дозах следует применять фибринолитические препараты. В настоящее время под эгидой Совета медицинских исследований (Medical Research Council) проводится работа, результаты которой позволят ответить на эти вопросы.
Если в результате дренирования из межреберного доступа (с фибринолитиками или без них) не удается добиться адекватного отведения жидкости, если эмпиема сохраняется, организуется и сопровождается утолщением плевры и сдавлением легкого, то показано хирургическое вмешательство.
Торакоскопия обычно успешна на ранних стадиях заболевания, но при обширных плевральных спайках может окончиться неудачей. В этих случаях показана торакотомия и декортикация. Хотя такое хирургическое вмешательство высокоэффективно в отношении лечения эмпиемы (>90%), с ним связан существенный операционный риск, особенно у ослабленных больных.
Открытый дренаж, при котором требуется резекция ребра, — довольно малопривлекательная процедура, она проводится только в том случае, когда больной не может перенести более инвазивную операцию.
Без лечения эмпиема может прорваться наружу через грудную стенку («прободающая» эмпиема) или в бронхиальное дерево с образованием бронхоплеврального свища либо вызвать обширный плевральный фиброз, который ограничивает подвижность легких. К редким осложнениям относятся абсцесс головного мозга и амилоидоз, может также возникнуть деформация фаланг типа «барабанных палочек».
Поражение плевры при злокачественных новообразованиях
Рак легких — это наиболее частая причина возникновения злокачественного плеврального выпота, особенно у курильщиков. Лимфома может возникнуть в любом возрасте и составляет 10% от всех злокачественных выпотов. Метастазы в плевру наиболее часто встречаются при раках молочной железы (25%), яичников (5%) или желудочно-кишечного тракта (2%) (см. рис. 3). В 7% случаев первичная опухоль остается неизвестной.
Важно понимать, что при первичном бронхогенном раке наличие плеврального выпота не обязательно исключает операбельность. У 5% таких больных выпот развивается вследствие обструкции бронхов и дистальной инфекции, и заболевание остается потенциально излечимым.
Поэтому, когда встает вопрос о возможности проведения операции, чрезвычайно важно установить причину плеврального выпота.
Выпоты, обусловленные злокачественной инфильтрацией плевры, обычно быстро накапливаются вновь. Для того чтобы избежать необходимости проведения повторных плевральных пункций, выпот необходимо полностью («насухо») удалить при первичном дренировании через межреберную трубку, а плевральная полость должна быть облитерирована путем введения вызывающих воспаление препаратов, например талька, тетрациклина или блеомицина, при этом в конце концов развивается плевродез. В настоящее время наиболее эффективным средством в этом отношении считается тальк: при его применении успех достигается у 90% больных [17].
Однако эффективный плевродез приводит к значительному болевому синдрому в послеоперационном периоде, который часто требует применения сильных анальгетиков; рекомендуется при этом избегать нестероидных противовоспалительных препаратов, поскольку они снижают эффективность операции.
Непосредственная абразия плевры во время операции с плеврэктомией или без нее применяется у молодых пациентов с довольно длительным сроком выживания, у которых не удался химический плевродез.
При обширном, мучительном для больного плевральном выпоте и неэффективности химического плевродеза альтернативным методом является установка плевроперитонеального шунта по Denver. Удивительно то, что при такой операции не наблюдается обсеменения опухоли по брюшине, однако в реальную проблему могут вылиться развитие инфекции и окклюзия шунта.
Патология плевры, связанная с асбестом
В 2002 году в Великобритании смертность от мезотелиомы, согласно прогнозам, достигнет пика в 2020 году и составит 3000 [5].
В большинстве стран среди заболевших преобладают мужчины, что подтверждает ведущую роль профессионального фактора в развитии этого заболевания.
Возраст на момент контакта с асбестом, а также продолжительность и интенсивность этого контакта тоже имеют важное значение. Наибольшему риску подвергаются представители профессий, требующих непосредственного контакта с асбестом, особенно рабочие строительной индустрии, в то время как для людей, проживающих в зданиях, содержащих асбест, риск гораздо ниже.
Заболевание проявляется болями в груди и плевральным выпотом, который имеет кровянистую окраску и вызывает одышку. В Великобритании пациенты с этой болезнью имеют право на компенсацию, как и при других заболеваниях и увечьях, полученных на производстве (см. табл. 4).
Во всех случаях необходимо гистологическое исследование, в ходе которого используются либо материал, получаемый при аспирации плеврального содержимого и биопсии под контролем УЗИ (что позволяет подтвердить диагноз у 39% таких больных), либо ткань, взятая при торакоскопии (диагноз подтверждается у 98% пациентов) [6]. Торакоскопия также позволяет определить степень распространенности опухоли в плевральной полости, поскольку очень ограниченное заболевание на ранней стадии может быть излечено хирургическим путем, в то время как при поражении висцеральной плевры прогноз неблагоприятный.
После таких диагностических вмешательств часто наблюдается обсеменение опухоли по плевре, профилактика этого состояния предполагает облучение области биопсии или дренажа.
Большинство пациентов впервые поступают к врачу уже с неоперабельной опухолью. В такой ситуации ни один из методов не обеспечивает возможности излечения больного, однако сегодня проводятся попытки применения радикальной операции, фотодинамической терапии, внутриплевральной системной химиотерапии и лучевой терапии. И хотя генная терапия пока не приносит успеха, иммунотерапия может признана перспективной. Неблагоприятными диагностическими факторами являются: низкие функциональные резервы сердечно-сосудистой и дыхательной систем, лейкоцитоз, перерождение в саркому (по данным гистологического исследования) и мужской пол. В течение одного года выживают от 12 до 40% больных, в зависимости от перечисленных прогностических факторов.
Спонтанный пневмоторакс
Спонтанный пневмоторакс может быть первичным (без явного предшествующего заболевания легких) или вторичным (когда имеются признаки легочного заболевания, например легочного фиброза). К малораспространенным причинам пневмоторакса относятся: инфаркт легкого, рак легкого, ревматоидные узелки или абсцесс легкого с образованием полости. Субплевральные эмфизематозные буллы, обычно расположенные в области верхушек легкого, или плевральные буллы обнаруживаются у 48–79% больных с якобы спонтанным первичным пневмотораксом [18].
Среди курильщиков частота пневмоторакса гораздо выше. Относительный риск развития пневмоторакса в девять раз выше у женщин-курильщиц и в 22 раза — у курящих мужчин. Более того, выявлена зависимость «доза — эффект» между числом выкуренных за день сигарет и частотой пневмоторакса [19].
В диагностике небольших по объему, преимущественно верхушечных, пневмотораксов могут помочь снимки на выдохе, которые, однако, используются редко. Следует различать большие эмфизематозные буллы и пневмоторакс.
Алгоритм лечения представлен на рисунке 5. Чрескожная аспирация — это простая, хорошо переносимая, альтернативная по отношению к межреберному дренажу по трубке процедура, в большинстве случаев ей следует отдавать предпочтение. Аспирация позволяет достичь удовлетворительного расправления легкого у 70% больных с нормальной легочной функцией и только у 35% пациентов с хроническими заболеваниями легких [20].
Средняя частота рецидивов после единственного первичного спонтанного пневмоторакса, независимо от первичного лечения, составляет 30%, большинство их возникает в первые 6–24 месяцев.
Пациентов следует предупреждать о возможности развития повторных пневмотораксов: в частности, им не рекомендуется летать на самолетах в течение шести недель после полного разрешения пневмоторакса. Операция обычно требуется в тех случаях, когда в течение недели наблюдается упорное накопление воздуха.
Рецидивирующий пневмоторакс, особенно если поражены оба легких, следует лечить либо путем химического плевродеза или, что более предпочтительно, с помощью париетальной плеврэктомии либо плевральной абразии.
Последние из названных операций можно проводить с помощью торакоскопии под контролем видеоизображения, которая позволяет проследить за ходом процедуры с помощью монитора, сократить пребывание в стационаре и ускорить возвращение пациента к нормальному образу жизни. Хирургическое лечение позволяет уменьшить частоту рецидивов до 4% в сравнении с 8% после плевродеза тальком [22].
В представленной статье мы рассказали о нескольких аспектах, связанных с заболеваниями плевры, в том числе о последних достижениях в этой области. Плевральный выпот — это самое частое проявление патологии плевры, требующее тщательного обследования. Если после обычных методов исследования причина заболевания остается неясной, нужно предпринять все необходимые меры для исключения тромбоэмболии легочных артерий, туберкулеза, реакции на введение лекарств и поддиафрагмальных патологических процессов.
Хелен Парфри, бакалавр медицины, бакалавр химии, член Королевской коллегии врачей
Больница Западного Саффолка
Эдвин Р. Чайлверс, бакалавр медицины, бакалавр естественных наук, доктор философии, профессор
Кембриджский университет, Школа клинической медицины, отделение терапии больницы Адденбрука и Папворта

