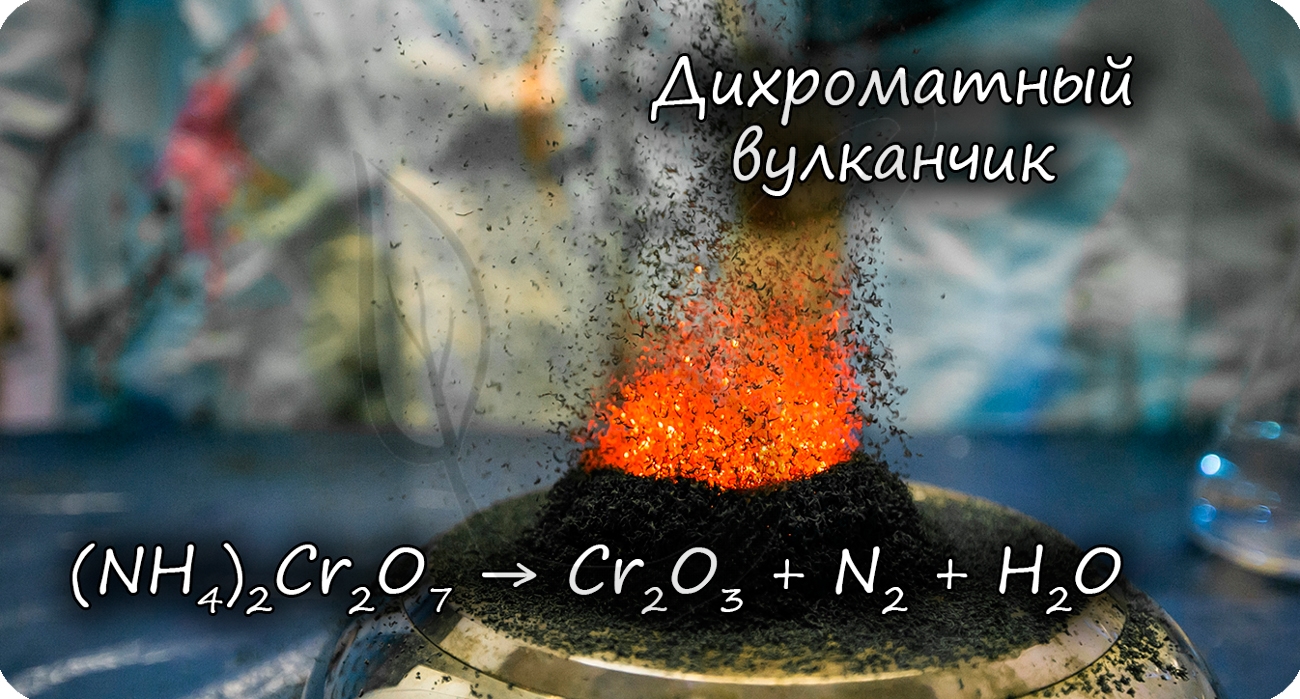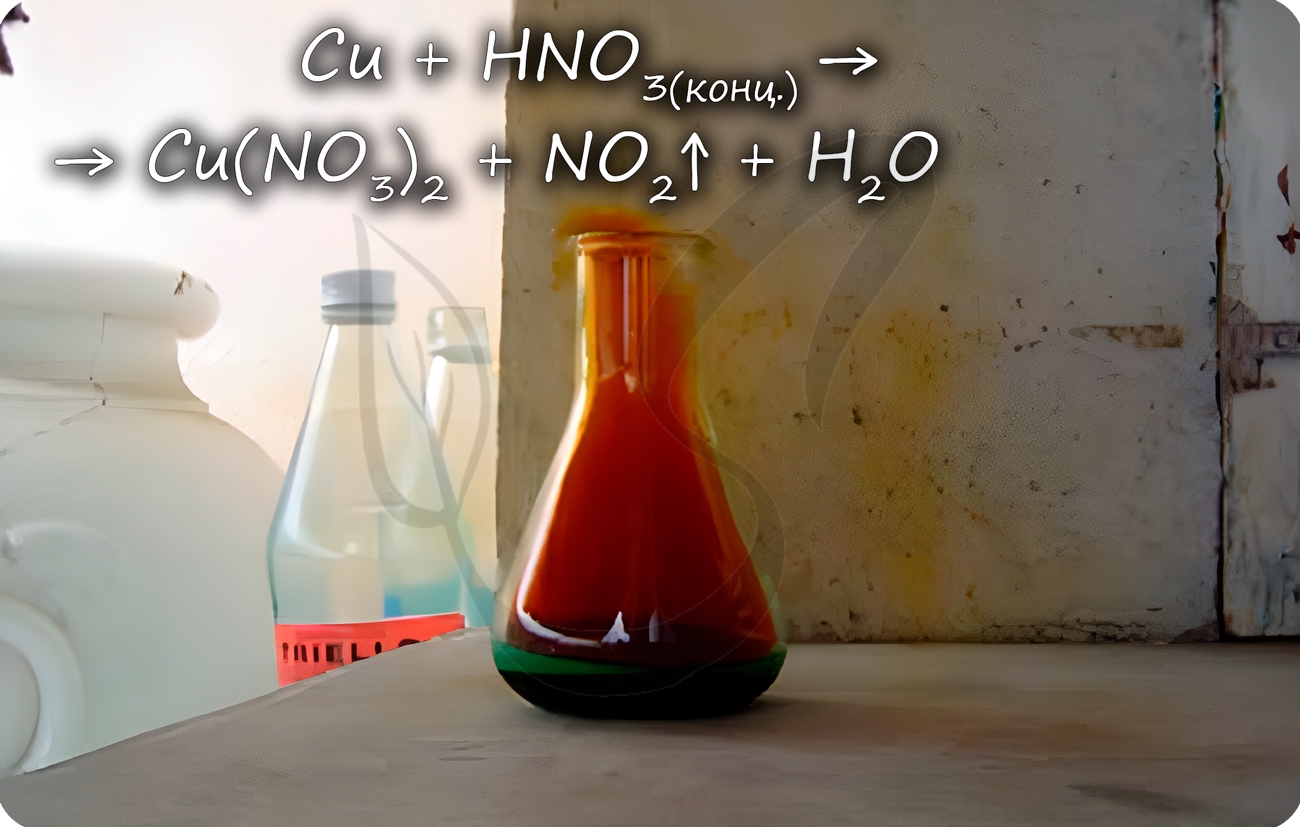кто с чем реагирует химия
Классификация реакций
Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно сложное вещество. Примеры:
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами. Часто обмен происходит анионами/катионами:
AgF + NaCl = AgCl↓ + NaF
Окислительно-восстановительные реакции (ОВР)
Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО, принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе «Решения задач».
Обратимые и необратимые реакции
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
Примеры необратимых реакций:
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)
Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой, твердой и газообразной.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество, твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ. Примером такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.
Реакции и их тепловой эффект
NaOH + HCl = NaCl + H2O + 56 кДж
К экзотермическим реакциям часто относятся реакции горения, соединения.
Исключением является взаимодействие азота и кислорода, при котором тепло поглощается:
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью «запутывания» в реакции вместо явного +Q при экзотермической реакции могут написать ΔH 0, так как внутренняя энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)
Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония («вулканчик») является примером экзотермического разложения, при котором тепло выделяется.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Кто с чем реагирует химия
Когда химические вещества вступают во взаимодействие, химические связи между их атомами разрушаются и образуются новые, уже в других сочетаниях. В результате одни вещества превращаются в другие.
Рассмотрим реакцию горения метана, происходящую в конфорке газовой плиты:
Молекула метана (CH₄) и две молекулы кислорода (2O₂) вступают в реакцию, образуя молекулу углекислого газа (CO₂) и две молекулы воды (2H₂O). Связи между атомами углерода (С) и водорода (H) в метане, а также между атомами кислорода (O) разрываются, и образуются новые связи между атомами углерода и кислорода в молекуле углекислого газа (CO₂) и между атомами водорода и кислорода в молекуле воды (H₂O).
Картинка даёт наглядное представление о том, что произошло в ходе реакции. Но зарисовывать сложные химические процессы такими схемами неудобно. Вместо этого учёные используют уравнения химических реакций.
Химическое уравнение — это условная запись химической реакции с помощью формул и символов.
Их записывают в виде схемы, в которой отражён процесс превращения. В левой части располагаются формулы реагентов — веществ, вступающих в реакцию. Завершается уравнение продуктами реакции — веществом или веществами, которые получились в результате.
Новые вещества образуются потому, что изменяются связи между атомами, но сами атомы не возникают из ниоткуда и не исчезают в никуда. На рисунке видно, что атом углерода из состава метана перешёл в состав углекислого газа, атом водорода — в состав воды, а атомы кислорода распределились между молекулами углекислого газа и воды. Число атомов не изменилось.
Согласно закону сохранения массы, общая масса реагентов всегда равна общей массе продуктов реакции. Именно поэтому запись химической реакции называют уравнением.
Виды химических реакций
Вещества вступают в реакции по-разному, можно выделить четыре наиболее частых варианта:
Сложное вещество негашёная известь соединяется с водой, и образуется новое сложное вещество — гашёная известь:
Стрелка вверх означает, что образовался газ. Он улетучивается и больше не участвует в реакции.
В примере атомы цинка замещают атомы водорода в составе хлороводорода, и образуется хлорид цинка:
Стрелка вниз означает, что вещество выпало в осадок, поскольку оно нерастворимо.
Коэффициенты в уравнениях химических реакций
Чтобы составить уравнение химической реакции, важно правильно подобрать коэффициенты перед формулами веществ.
Коэффициент в химических уравнениях означает число молекул (формульных единиц) вещества, необходимое для реакции. Он обозначается числом перед формулой (например, 2NaCl в последнем примере).
Коэффициент не следует путать с индексом (числом под символом химического элемента, например, О₂). Индекс обозначает количество атомов этого элемента в молекуле (формульной единице).
Чтобы узнать общее число атомов элемента в формуле, нужно умножить его индекс на коэффициент вещества. В примере на картинке (2H₂O) — четыре атома водорода и два кислорода.
Подобрать коэффициент — значит определить, сколько молекул данного вещества должно участвовать в реакции, чтобы она произошла. Далее мы расскажем, как это сделать.
Алгоритм составления уравнений химических реакций
Для начала составим схему химической реакции. Например, образование оксида магния (MgO) в процессе горения магния (Mg) в кислороде (O₂). Обозначим реагенты и продукт реакции:
Чтобы схема стала уравнением, нужно расставить коэффициенты. В левой части схемы два атома кислорода, а в правой — один. Уравняем их, увеличив число молекул продукта:
Теперь число атомов кислорода до и после реакции одинаковое, а число атомов магния — нет. Чтобы уравнять их, добавим ещё одну молекулу магния. Когда количество атомов каждого из химических элементов в составе веществ уравнено, вместо стрелки можно ставить равно:
Уравнение химической реакции составлено.
Рассмотрим реакцию разложения. Нитрат калия (KNO₃) разлагается на нитрит калия (KNO₂) и кислород (О₂):
В обеих частях схемы по одному атому калия и азота, а атомов кислорода до реакции 3, а после — 4. Необходимо их уравнять.
Для начала удвоим коэффициент перед реагентом:
Теперь в левой части схемы шесть атомов кислорода, два атома калия и два атома азота. В левой по-прежнему по одному атому калия и азота и четыре атома кислорода. Чтобы уравнять их, в правой части схемы нужно удвоить коэффициент перед нитритом калия.
Снова посчитаем число атомов каждого химического элемента в составе веществ до и после реакции: два атома калия, два атома азота и шесть атомов кислорода. Равенство достигнуто.
Химические уравнения не только позволяют предсказать, что произойдёт при взаимодействии тех или иных веществ, но и помогают рассчитать их количественное соотношение, необходимое для реакции.
Учите химию вместе с домашней онлайн-школой «Фоксфорда»! По промокоду CHEMISTRY892021 вы получите бесплатный недельный доступ к курсам химии за 8 класс и 9 класс.
У нас вы сможете учиться в удобном темпе, делать упор на любимые предметы и общаться со сверстниками по всему миру.

Интересное по рубрике
Найдите необходимую статью по тегам
Подпишитесь на нашу рассылку
Мы в инстаграм
Домашняя онлайн-школа
Помогаем ученикам 5–11 классов получать качественные знания в любой точке мира, совмещать учёбу со спортом и творчеством

Рекомендуем прочитать
Реальный опыт семейного обучения
Звонок по России бесплатный
Посмотреть на карте
Если вы не нашли ответ на свой вопрос на нашем сайте, включая раздел «Вопросы и ответы», закажите обратный звонок. Мы скоро свяжемся с вами.
Неорганическая химия
Ни одна вещь не возникает, не уничтожается, но каждая составляется из смешения существующих вещей или выделяется из них. (Анаксагор)
Неорганическая химия изучает свойства и реакции неорганических соединений (т.е., кроме органических соединений углерода). Число неорганических веществ приближается к 400 тысяч.
Разделы страницы по химии неорганических соединений:
О %nbsp;свойствах химического элемента вы можете почитать, указав его в таблице Менделеева.
Когда появились молекулы?
Стюарт Кауфман из Института системной биологии в США и его коллеги Давид Еленфи и Габор Ваттаи из Будапештского университета в Венгрии построили модель формирования молекул на разных стадиях развития Вселенной, которая воспроизводит наблюдающееся сегодня распределение соединений в межзвездной и межгалактической среде. Так как количество возможных соединений растет быстрее экспоненты в зависимости от количества атомов, то авторы ограничились только рассмотрением общей массы образующихся молекул.
За основу ученые взяли базу данных PubChem, в которой содержится информация о 90 миллионах различных молекул, большинство из которых встречаются в природе. Масса наибольшего количество соединений составляет 290 дальтон, что примерно соответствует 24 атомам углерода. Эти данные ученые сравнили с содержанием веществ в Мурчисонском метеорите — древнем теле, появившемся во времена формирования Солнечной системы около 5 миллиардов лет назад. В нем было обнаружено не менее 58 000 различных молекул, распределение которых по массам напоминает полную базу данных, но больше всего молекул с массой около 240 дальтон.
Затем авторы привлекают теорию образования молекул, согласно которой есть два основных пути их формирования: посредством случайного скапливания атомов, которое быстро порождает всевозможные легкие комбинации, и предпочтительного присоединения, которое медленно порождает небольшое количество из всех возможных молекул с большой массой. Зная скорости этих процессов и различия в распределениях в Мурчисонском метеорите и на Земле в целом, можно экстраполировать данные в прошлое и вывести время образования соединений. Авторы приходят к выводу, что молекулы начали образовываться примерно 12,8 миллиардов лет назад, а аминокислоты появились спустя еще 165 миллионов лет.
Виды неорганических веществ
Неорганические вещества делятся на простые (металлы и неметаллы) и сложные (оксиды, соли, основания, кислоты). [Последние являются результатом окислительно-восстановительных реакций.]
Простые [моноатомные] вещества состоят из атомов одного химического элемента. По своим химическим свойствам они делятся на:
Сложные [гетероатомные] вещества состоят из атомов двух или более химических элементов. Они по своим химическим свойствам делятся на:
Существуют и другие сложные вещества:
Химические реакции между неорганическими веществами
В основе реакционной способности атомов лежит незаполненность их электронного слоя. В ходе химической реакции металлы обычно отдают электроны, а неметаллы – принимают.
Металлы вступают в реакцию с неметаллами с образованием солей: 2Na + S = Na2S.
Металлы в реакциях с кислородом образуют обычно основные оксиды: 4Na + O2 = 2Na2O. Неметаллы в реакциях с кислородом образуют кислотные оксиды: S + O2 = SO2. Основные оксиды реагируют с кислотными оксидами с образованием солей: Na2O + SO2 = Na2SO3.
Основные оксиды реагируют с водой с образованием оснований: Na2O + H2O = 2NaOH. Кислотные оксиды реагируют с водой с образованием кислот: SO2 + H2O = H2SO3. Основания реагируют с кислотами с образованием солей: 2NaOH + H2SO3 = Na2SO3 + 2H2O.
Основные оксиды способны реагировать с кислотами, при этом образуются соли: Na2O + H2SO3 = Na2SO3. Кислотные оксиды реагируют с основаниями также с образованием солей: SO2 + 2NaOH = Na2SO3 + H2O.
Наибольшую реакционную способность проявляют типичные металлы и их соединения, и типичные неметаллы и их соединения. К типичным металлам относятся щелочные металлы, а также барий, стронций кальция. Активность всех остальных металлов и их соединений снижена. Так магний вступает в химическую реакцию только с кипящей водой и нагретыми парами воды, а оксид магния не реагирует с водой. Медь, к примеру, не реагирует с кислотами (не может быть окислена ионом водорода). Примерно тоже самое можно сказать о неметаллах. Наибольшую активность проявляют фтор, кислород, галогены.
Соли (состав и свойства)
Соли разделяются на растворимые в воде и нерастворимые в воде. О растворимости солей можно узнать из таблицы растворимости. Хорошо растворимы обычно соли щелочных металлов и аммония.
Средние соли состоят только из остатка кислоты и основания: CaSO4, Ba(NO3)2. Кислые соли кроме катиона металла содержат катион водорода, следовательно, они проявляют все свойства солей и кислот: Ca(HCO3)2 + Сa(OH)2 = 2CaCO3 + 2H2O.
Основные соли включают в свой состав также гироксильную группу и проявляют свойства солей и оснований: (MgOH)2SO4 + H2SO4 = 2MgSO4 + 2H2O.
Основания и щёлочи
Основания делятся на растворимые в воде и нерастворимые в воде. Растворимые основания называют щелочами.
Щелочами являются гидроксиды щелочных металлов, а также гидроксиды бария, стронция кальция.
Кислоты
Все изучаемые в школе кислоты, кроме кремниевой растворимы в воде. Кислоты можно разделить на сильные и слабые. Сильные кислоты: это азотная HNO3, серная H2SO4, хлорная HClO4, хлороводородная (соляная) HCl, бромоводородная HBr, йодоводородная HI.
Как реагируют амфотерные вещества (простые и сложные)
Кроме вышеописанных существуют амфотерные простые вещества, оксиды и гидроксиды.
Амфотерные простые вещества
Амфотерными простыми веществами изучаемыми в школе являются бериллий Be, алюминий Al и цинк Zn. Амфотерные простые вещества реагируют как с кислотами, так и с основаниями. Например: Zn + 2HCl = ZnCl2 + H2; Zn + 2KOH + 2H2O = K2[Zn(OH)4] + H2.
Амфотерные оксиды
К амфотерным оксидам относят BeO, Al2O3, ZnO, H2O, Cr2O3, Fe2O3. Амфотерные оксиды реагируют с кислотами и основаниями, а также основными и кислотными оксидами: ZnO + 2HCl = ZnCl2 + H2O; ZnO + 2KOH + H2O = K2[Zn(OH)4]; SO3 + H2O = H2SO4; K2O + H2O = 2KOH.
Амфотерные гидроксиды
Амфотерные гидроксиды – сложные вещества, которые имеют свойства и кислот, и оснований. Все они — твердые вещества, не растворимые в воде. Они растворяются в кислотах и щелочах: Zn + 2OH = Zn(OH)2 = 2H + ZnO2 Cr + 3OH = Cr(OH)3 = H + CrO2 + H2O
Окраска амфотерных гидроксидов зависит от характера входящих в их состав катионов металлов. К амфотерным гидроксидам относят Be(OH)2, Zn(OH)2, Al(OH)3, Cr(OH)3, Fe(OH)3.
Направления реакционной способности основных классов неорганических веществ
Все вышесказанное удобно представить в виде схемы:
Хром, железо и медь
Твердый металл голубовато-белого цвета. Этимология слова «хром» берет начало от греч. χρῶμα — цвет, что связано с большим разнообразием цветов соединений хрома. Массовая доля этого элемента в земной коре составляет 0.02% по массе.
В промышленности хром получают прокаливанием хромистого железняка с углеродом. Также применяют алюминотермию для вытеснения хрома из его оксида.
Протекает в раскаленном состоянии.
С холодными концентрированными серной и азотной кислотой реакция не идет. Она начинается только при нагревании.
Хром способен вытеснить из солей металлы, стоящие в ряду напряжений правее него.
Соединения хрома (II)
Гидроксид хрома (II), как нерастворимый гидроксид, легко разлагается при нагревании на соответствующий оксид и воду, реагирует с кислотами, кислотными оксидами.
Соединения хрома (III)
Это наиболее устойчивые соединения, которые носят амфотерный характер. К ним относятся оксид хрома (III) гидроксид хрома (III).
H2O + NaOH + Cr2O3 → Na3[Cr(OH)6] (в растворе, гексагидроксохромат натрия)
Cr2O3 + 2NaOH → (t°) 2NaCrO2 + H2O (прокаливание, хромит натрия)
Cr2O3 + HCl = CrCl3 + H2O (сохраняем степень окисления Cr +3 )
Оксид хрома (III) реагирует с более активными металлами (например, при алюминотермии).
При окислении соединение хрома (III) получают соединения хрома (VI) (в щелочной среде).
Соединения хрома (VI)
Хроматы переходят в дихроматы с увеличением кислотности среды (часто в реакциях с кислотами). Цвет раствора меняется с желтого на оранжевый.
Разложение дихромата аммония выглядит очень эффектно и носит название «вулканчик» 🙂
В степени окисления +6 соединения хрома проявляют выраженные окислительные свойства.
Железо
Является одним из самых распространенных элементов в земной коре (после алюминия), составляет 4,65% ее массы.
Для железа характерны две основные степени окисления +2, +3, +6.
Основными сплавами железа являются чугун и сталь. В стали содержание углерода менее 2%, меньше содержится P, Mn, Si, S. Чугун отличается бо́льшим содержанием углерода (2-6%), содержит больше P, Mn, Si, S.
Fe + S = FeS (t > 700°C)
Качественной реакцией на ионы Fe 2+ также является взаимодействие с щелочью (гидроксидом натрия). В результате выпадает осадок зеленого цвета.
Соединения железа (III) проявляют амфотерные свойства. Оксид и гидроксид железа (III) реагирует и с кислотами, и с щелочами.
Fe(OH)3 + KOH = K3[Fe(OH)6] (гексагидроксоферрат калия)
При сплавлении комплексные соли не образуются из-за испарения воды.
Качественной реакцией на ионы Fe 3+ является взаимодействие с желтой кровяной солью K4[Fe(CN)6]. В результате реакции образуется берлинская лазурь (прусский синий).
Реакция хлорида железа (III) с роданидом калия также является качественной, в результате нее образуется характерный раствор ярко красного цвета.
Ферраты можно получить в ходе электролизом щелочи на железном аноде, а также действием хлора на взвесь Fe(OH)3 в щелочи.
Один из первых металлов, освоенных человеком вследствие низкой температуры плавления и доступности получения руды.
Основные степени окисления меди +1, +2.
Пирометаллургический метод получения основан на получении меди путем обжига халькопирита, который идет в несколько этапов.
Медь, как малоактивный металл, выделяется при электролизе солей в водном растворе на катоде.
Во влажном воздухе окисляется с образованием основного карбоната меди.
При нагревании реагирует с кислородом, селеном, серой, при комнатной температуре с: хлором, бромом и йодом.
4Cu + O2 = (t) 2Cu2O (при недостатке кислорода)
2Cu + O2 = (t) 2CuO (в избытке кислорода)
Медь способна восстанавливать неметаллы из их оксидов.
Соединения меди I
В степени окисления +1 медь проявляет основные свойства. Соединения меди (I) можно получить путем восстановления соединений меди (II).
Оксид меди (I) можно восстановить до меди различными восстановителями: угарным газом, алюминием (алюминотермией), водородом.
Оксид меди (I) окисляется кислородом до оксида меди (II).
Оксид меди (I) вступает в реакции с кислотами.
Гидроксид меди CuOH неустойчив и быстро разлагается на соответствующий оксид и воду.
Соединения меди (II)
Степень окисления +2 является наиболее стабильной для меди. В этой степени окисления у меди есть оксид CuO и гидроксид Cu(OH)2. Данные соединения проявляют преимущественно основные свойства.
Оксид меди (II) получают в реакциях термического разложения гидроксида меди (II), реакцией избытка кислорода с медью при нагревании.
При нагревании гидроксид меди (II), как нерастворимое основание, легко разлагается на соответствующий оксид и воду.
Как сказано выше, гидроксид меди (II) носит преимущественно основный характер, однако способен проявлять и амфотерные свойства. В растворе концентрированной щелочи он растворяется, образуя гидроксокомлпекс.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.









.jpg)
.jpg)
.jpg)
.jpg)


.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)