лимфогранулематоз что это за болезнь симптомы и причины у детей
Лимфома Ходжкина
Информация для родителей
Лимфома Ходжкина (болезнь Ходжкина или лимфогранулематоз) – злокачественное заболевание лимфатической системы.
Причины развития
Лимфома Ходжкина (ЛХ) возникает из-за злокачественного изменения (мутации) В-лимфоцитов. В-лимфоциты — это белые кровяные клетки крови, которые находятся в основном в лимфатической ткани. Поэтому лимфома Ходжкина может развиваться везде, где есть лимфатическая ткань, также она может поражать и другие органы (печень, костный мозг, лёгкие и/или селезёнку).
Распространенность
Формы
Морфологическим субстратом опухоли являются клетки Березовского-Штенберга-Рид, однако, их количество в опухолевой ткани редко превышает 10%. Второй вариант клеток – клетки Ходжкина, которые являются провариантом клетки Березовского-Штенберга-Рид. В зависимости от того, как выглядит ткань опухоли под микроскопом, выделяют пять форм лимфомы Ходжкина.
Клинические стадии
Клиническая стадия определяется согласно классификации Ann Arbor (1971), дополненной рекомендациями, принятыми в Котсвольде (1989):
I стадия — поражение одной или двух группы лимфатических узлов (I) или одного нелимфатического органа (или ткани) — (IE);
II стадия — поражение двух или более лимфатических областей по одну сторону диафрагмы (II) или вовлечение одного нелимфатического органа (или ткани) и одной (или более) лимфатических областей по одну сторону диафрагмы (IIE), поражение селезенки (IIS);
III стадия — поражение лимфатической системы по обе стороны диафрагмы (III), которое может сочетаться с локализованным вовлечением одного нелимфатического органа или ткани (IIIE), или с вовлечением селезенки (IIIS), или поражением того и другого (IIIES);
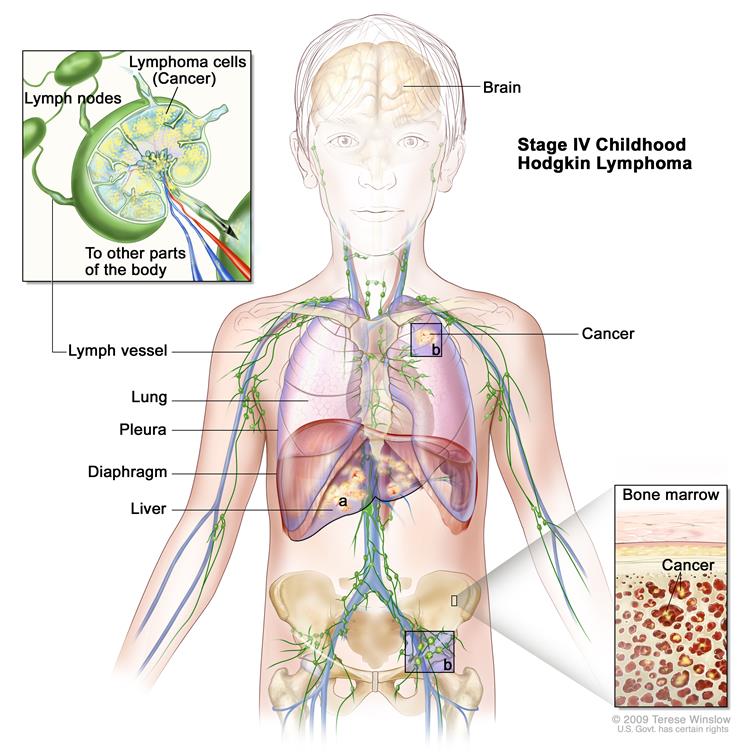
IV стадия — распространенное поражение одного и более нелимфатических органов (легких, плевры, перикарда, костного мозга, костей и проч.) в сочетании или без вовлечения лимфатических узлов.
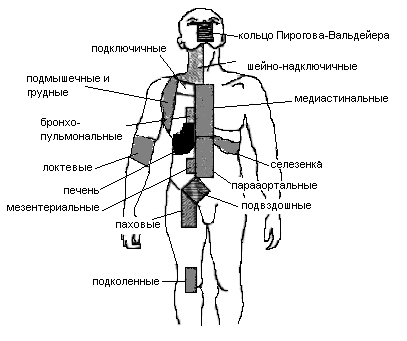
На рис. 1 представлены зоны поражения при лимфоме Ходжкина.
Рис. 1. Зоны поражения при болезни Ходжкина
Симптомы
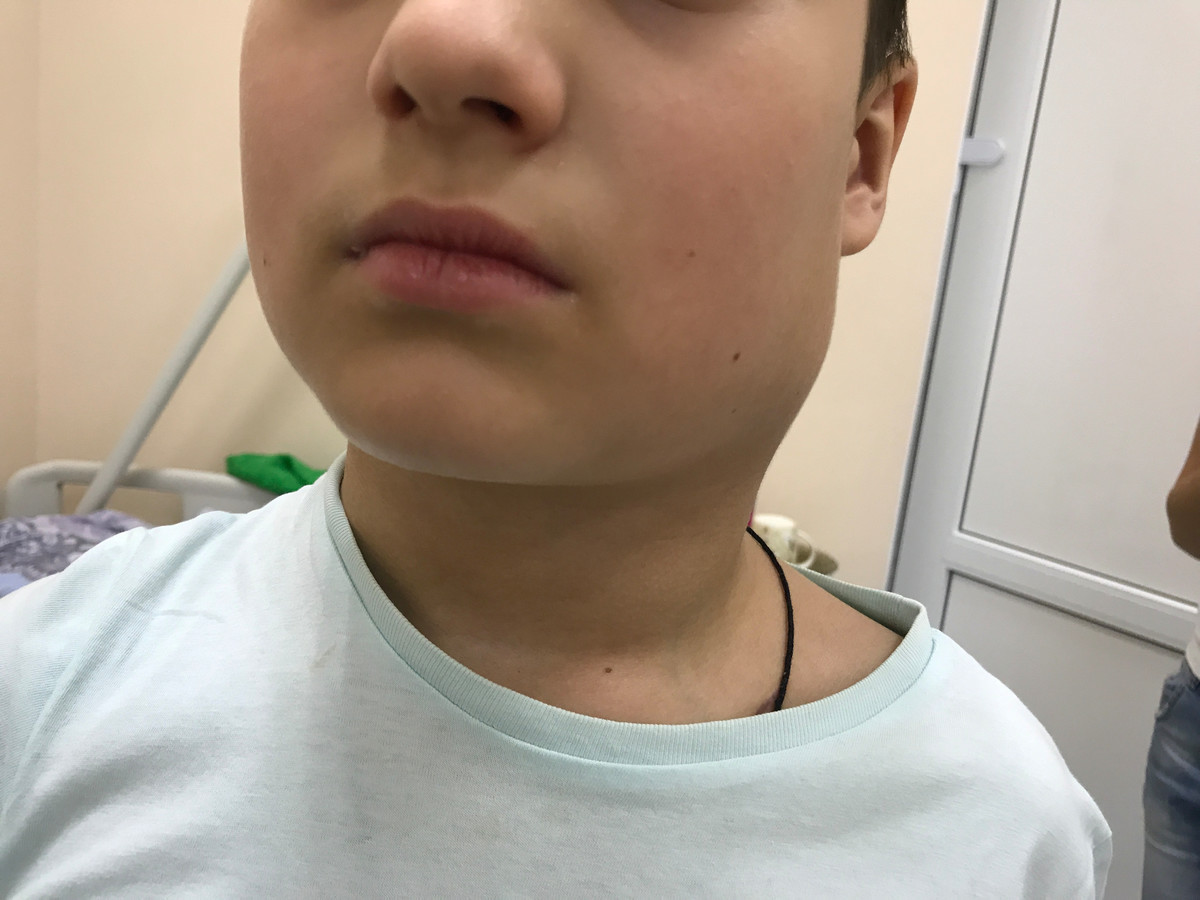
Первым и наиболее характерным симптомом при лимфоме Ходжкина является увеличение лимфатических узлов. Лимфатические узлы, как правило, безболезненные, плотные, подвижные, часто в виде конгломератов (напоминают «мешок с картошкой»). Наиболее часто увеличенные лимфоузлы можно заметить на шее (рис. 2), в области подмышек, рядом с ключицей, в паху или одновременно в нескольких местах. Лимфатические узлы могут увеличиваться и там, где их нельзя прощупать, например, в грудной клетке, животе, в области таза.
Рис. 2. Поражение шейных лимфатических узлов при лимфоме Ходжкина.
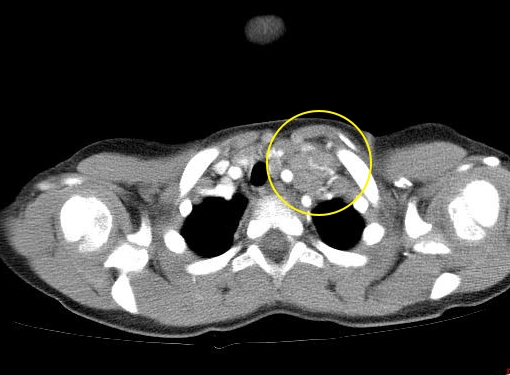
Если увеличенные лимфоузлы находятся в грудной клетке (средостении) (рис. 3), могут появляться приступы кашля или одышка.
Иногда увеличиваются печень и селезенка (в медицинской практике это называется гепатомегалия и спленомегалия).
Поражение ЦНС может развиться в далеко зашедших случаях лимфомы Ходжкина.
Поражение костей: чаще поражаются позвонки, тазобедренные суставы.
Вовлечение костного мозга встречается в 5-10% случаев болезни Ходжкина.
У детей могут появляться общие симптомы заболевания: повышение температуры тела выше 38°С в течение трех дней без признаков инфекционных заболеваний, сильные ночные поты, потеря веса более, чем на 10% за последние 6 месяцев без видимой причины, утомляемость, слабость, кожный зуд по всему телу. Эти симптомы в медицинской практике называют В-симптомами и обозначают буквой «В», их используют в определении стадии заболевания.
Для стадирования необходимо учитывать биологическую активность заболевания. Определяется она на основании двух и более следующих показателей: СОЭ ≥ 30 мм/час; фибриноген ≥ 4 г/л; альбумин ≤ 40 %; СРБ (++ и более); число лейкоцитов ≥ 12х10 /л; альфа-2-глобулин ≥ 12%
Диагностика
Если после тщательного осмотра педиатр находит признаки лимфомы Ходжкина, то он дает направление в специализированный стационар (клинику детской онкологии и гематологии).
В стационаре проводятся:
Рис. 3. Поражение внутригрудных лимфатических узлов при лимфоме Ходжкина
Современные подходы к лечению
Основное место в лечении лимфомы Ходжкина занимает химиотерапия.
Химиотерапия – это лечение лекарственными препаратами (цитостатиками), которые блокируют деление или убивают опухолевые клетки. Максимального эффекта можно добиться используя комбинации цитостатиков (полихимиотерапия — ПХТ), которые по-разному действуют на клетки.
Полихимиотерапия проводится в соответствии с группой риска, в которую отнесен больной при первичном стадировании, в специализированном стационаре.
Первый цикл ПХТ начинается сразу же после подтверждения диагноза и установления стадии, в случае проведения оперативного лечения полихимиотерапия начинается через 5 дней после операции.
После химиотерапии проводится лучевая терапия (облучение) пораженных зон. Лучевая терапия должна начинаться в течение 14 дней от окончания химиотерапии при нормальных показателях крови.
В России сегодня используются две основные программы лечения лимфомы Ходжкина: DAL-HD и СПбЛХ. Оба протокола включают в себя полихимиотерпию и завершающую лучевую терапию. Количество циклов ПХТ зависит от стадии болезни и от выбора терапевтической группы, по которой лечат пациента. Больные обычно получают следующую программу: при благоприятных вариантах (1-я группа риска) – 2 цикла химиотерапии, при промежуточном прогнозе (2-я группа риска) – 4 цикла химиотерапии, при неблагоприятных вариантах (3-я группа риска) – 6 циклов химиотерапии. Разделение больных на группы риска имеет некоторые отличия в зависимости от применяемого протокола.
В программе DAL-HD используются схемы OPPA/OEPA и COPP. В протоколе СПбЛХ – схемы VBVP и ABVD.
Лучевая терапия
Завершающим этапом лечения лимфомы Ходжкина является облучение всех пораженных зон лимфатических узлов. Как правило, лучевую терапию начинают через 2 недели после окончания лекарственной терапии при нормализации показателей крови.
Доза облучения зависит от полноты ремиссии после лекарственной терапии: при достижении полной ремиссии (исчезновение всех клинических и радиологических признаков заболевания) в лимфатической зоне по данным ПЭТ-КТ доза облучения составляет 20 Гр. Если размер опухоли после полихимиотерапии уменьшился на 75% и более от первоначальной опухоли и/или отмечается снижение гиперфиксации РФП по ПЭТ-КТ до 2-3 по Deauville, то доза облучения составляет 25 Гр. При уменьшении опухолевых образований менее чем на 75% и/или сохранении гиперфиксации РФП по ПЭТ-КТ 4-5 по Deauville, то дозу облучения увеличивают до 30 Гр.
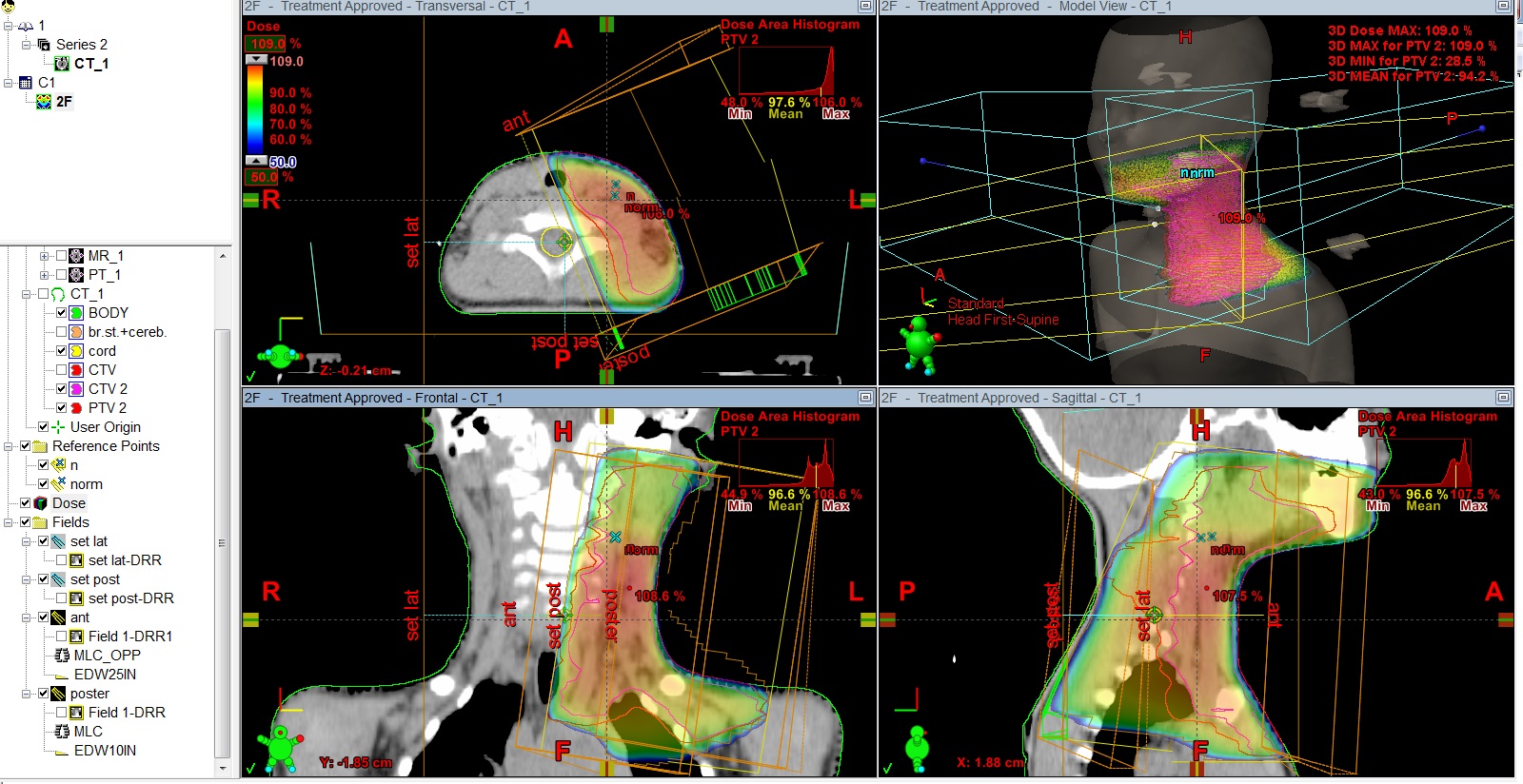
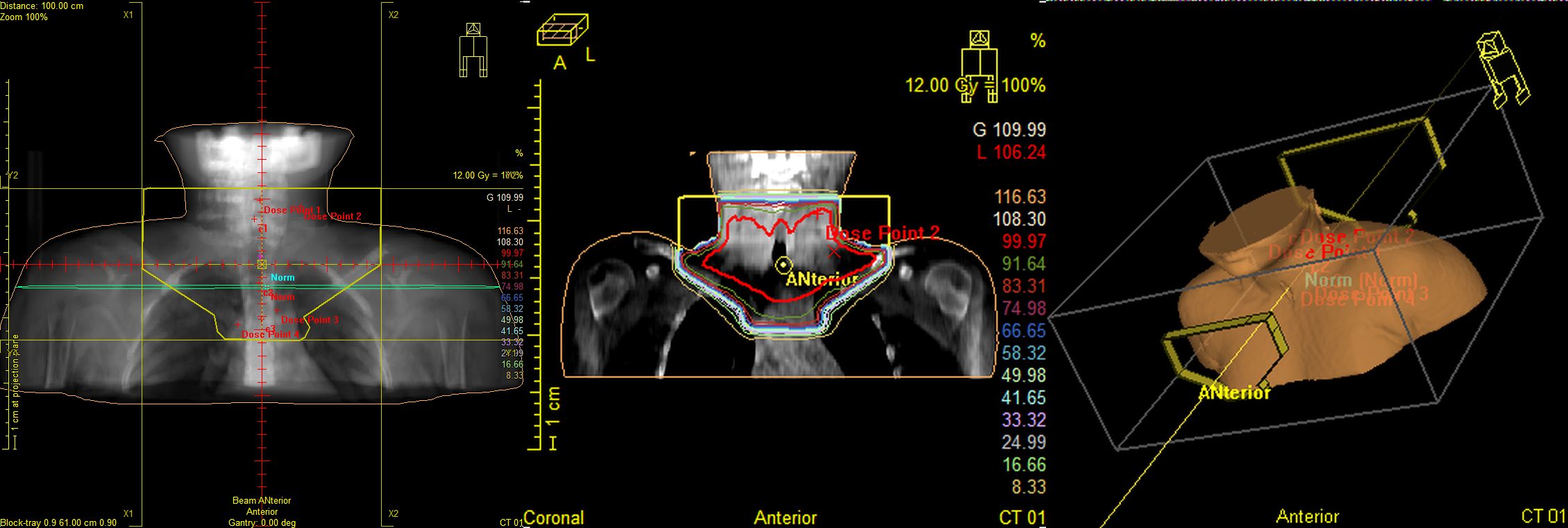
Рис.5 План лучевого лечения. Пациент И., 4 года 6 мес. Лимфома Ходжкина IIст. с поражением шейных, надключичных, подключичных л/у слева, вилочковой железы, носоглотки. Состояние после 4 курсов курсов ПХТ, ремиссия. Облучение шейно-над-подключичных л/у слева с консолидирующей целью, СОД 20 Гр.
Рис.6 Пациентка М., 11лет. Лимфома Ходжкина II ст. с поражением мягких тканей шеи, лимфатических узлов шеи. Состояние после 2 курсов ПХТ. По данным контрольного ПЭТ/КТ метаболически значимых очагов не выявлено, ремиссия. Проведение лучевой терапии первично вовлеченных зон в суммарной очаговой дозе 20,0Гр с целью консолидации.
Критерии оценки полноты ремиссии
Критерии оценки ремиссии нужны врачу для определения необходимости продолжения лечения или интенсификации программ терапии, либо перевода пациента под динамическое наблюдение.
Диспансерное наблюдение
Наблюдение детей и подростков с лимфомой Ходжкина проводится в течение не менее 3-х лет после завершения лечебной программы.
В первом квартале пациент обследуется каждый месяц, в последующие 9 месяцев – каждый квартал и в последующие годы – раз в полгода.
Лимфома Ходжкина относится к числу наиболее излечиваемых онкологических заболеваний и около 80% пациентов живут более 10 лет после окончания лечения.
Авторская публикация:
КУЛЕВА СВЕТЛАНА АЛЕКСАНДРОВНА
заведующая отделением химиотерапии и комбинированного лечения злокачественных опухолей у детей, доктор медицинских наук
Лимфогранулематоз
Общие сведения
Лимфогранулематоз (ЛГМ) – лимфопролиферативное заболевание, протекающее с образованием специфических полиморфно-клеточных гранулем в пораженных органах (лимфоузлах, селезенке и др.). По имени автора, впервые описавшего признаки заболевания и предложившего выделить его в самостоятельную форму, лимфогранулематоз также называют болезнью Ходжкина, или ходжкинской лимфомой. Средний показатель заболеваемости лимфогранулематозом составляет 2,2 случая на 100 тыс. населения. Среди заболевших преобладают молодые люди в возрасте 20-30 лет; второй пик заболеваемости приходится на возраст старше 60 лет. У мужчин болезнь Ходжкина развивается в 1,5-2 раза чаще, чем у женщин. В структуре гемобластозов лимфогранулематозу отводится втрое место по частоте возникновения после лейкемии.
Причины лимфогранулематоза
Этиология лимфогранулематоза до настоящего времени не выяснена. На сегодняшний день в числе основных рассматриваются вирусная, наследственная и иммунная теории генеза болезни Ходжкина, однако ни одна из них не может считаться исчерпывающей и общепризнанной. В пользу возможного вирусного происхождения лимфогранулематоза свидетельствует его частая корреляция с перенесенным инфекционным мононуклеозом и наличием антител к вирусу Эпштейна-Барр. По меньшей мере, в 20% исследуемых клеток Березовского-Штернберга обнаруживается генетический материал вируса Эпштейна-Барр, обладающего иммуносупрессивными свойствами. Также не исключается этиологическое влияние ретровирусов, в т. ч. ВИЧ.
Классификация лимфогранулематоза
В гематологии различают изолированную (локальную) форму лимфогранулематоза, при которой поражается одна группа лимфоузлов, и генерализованную – со злокачественной пролиферацией в селезенке, печени, желудке, легких, коже. По локализационному признаку выделяется периферическая, медиастинальная, легочная, абдоминальная, желудочно-кишечная, кожная, костная, нервная формы болезни Ходжкина.
В зависимости от скорости развития патологического процесса лимфогранулематоз может иметь острое течение (несколько месяцев от начальной до терминальной стадии) и хроническое течение (затяжное, многолетнее с чередованием циклов обострений и ремиссий).
На основании морфологического исследования опухоли и количественного соотношения различных клеточных элементов выделяют 4 гистологические формы лимфогранулематоза:
В основу клинической классификации лимфогранулематоза положен критерий распространенности опухолевого процесса; в соответствии с ним развитие болезни Ходжкина проходит 4 стадии:
I стадия (локальная) – поражена одна группа лимфоузлов (I) либо один экстралимфатический орган (IE).
III стадия (генерализованная) – пораженные лимфоузлы расположены с обеих сторон диафрагмы (III). Дополнительно может поражаться один экстралимфатический орган (IIIE), селезенка (IIIS) либо они вместе (IIIE + IIIS).
IV стадия (диссеминированная) – поражение затрагивает один или несколько экстралимфатических органов (легкие, плевру, костный мозг, печень, почки, ЖКТ и др.) с одновременным поражением лимфоузлов или без него.
Для обозначения наличия или отсутствия общих симптомов лимфогранулематоза на протяжении последних 6 месяцев (лихорадки, ночной потливости, похудания) к цифре, обозначающей стадию болезни, добавляются буквы А или В соответственно.
Симптомы лимфогранулематоза
К числу характерных для лимфогранулематоза симптомокомплексов относятся интоксикация, увеличение лимфатических узлов и возникновение экстранодальных очагов. Часто заболевание начинается с неспецифических симптомов – периодической лихорадки с температурными пиками до 39°С, ночной потливости, слабости, похудания, кожного зуда.
У 15-20% пациентов лимфогранулематоз дебютирует с увеличения лимфоузлов средостения. При поражении медиастинальных лимфоузлов первыми клиническими признаками болезни Ходжкина могут служить дисфагия, сухой кашель, одышка, синдром ВПВ. Если опухолевый процесс затрагивает забрюшинные и мезентериальные лимфоузлы, возникают абдоминальные боли, отеки нижних конечностей.
Лимфогранулематоз что это за болезнь симптомы и причины у детей
Понятие «лимфома» объединяет множество заболеваний, различных по своим клиническим проявлениям, течению и прогнозу. Все лимфомы делятся на две большие группы: лимфома Ходжкина (ЛХ) и неходжкинские лимфомы. Первая названа в честь ученого Томаса Ходжкина, который впервые описал ее в 1832 году (а само название введено ВОЗ в 2001-м). Синонимы — лимфогранулематоз, болезнь Ходжкина. ЛХ стала первой клинически и морфологически распознаваемой злокачественной опухолью и первым злокачественным заболеванием, при котором больные имели шанс на полное излечение при наличии в арсенале врача-онколога только лучевой терапии. Сегодня успехи в лечении ЛХ относятся к ярким победам онкологии.
Алеся Марковец, научный сотрудник лаборатории клинических исследований РНПЦ детской онкологии, гематологии и иммунологии. Статистика
По данным республиканского канцер-регистра, заболеваемость лимфомой Ходжкина у детей в Беларуси составляет 1,34:100 000. Заболевание встречается во всех возрастах за исключением детей до одного года, крайне редко — до 5 лет, наиболее часто — среди подростков от 15 до 19 лет. Ежегодно в нашей стране насчитывается около 30 случаев ЛХ среди детей и подростков.
Причины и факторы риска
Конкретная причина возникновения ЛХ в большинстве случаев остается неизвестной. В настоящее время изучается роль вирусов в этиологии злокачественных лимфом (Эпштейна — Барр, цитомегаловирус, вирус герпеса 6-го типа), однако бесспорных доказательств вирусной теории не получено. Кроме того, к факторам, предрасполагающим к развитию ЛХ, относятся различные иммунодефицитные состояния (прием лекарств, подавляющих иммунитет, ВИЧ-инфекция, врожденные иммунодефициты), воздействие ионизирующего излучения и генетические факторы.
Клиническая картина
При ЛХ опухоль представлена злокачественными клетками Рид — Штернберга и клетками Ходжкина. Могут поражаться различные внутренние органы, вызывая нарушение их нормальной работы.
Опухолевый конгломерат шейных лимфоузлов при лимфоме Ходжкина. Как правило, первым признаком заболевания является безболезненное увеличение одного или нескольких лимфатических узлов, чаще на шее, реже — в подмышечной, паховой области. Иногда опухолевый процесс начинается в недоступных для осмотра местах — грудной клетке (средостении) или брюшной полости. Тогда увеличивающиеся лимфоузлы могут сдавливать соседние органы, вызывая сухой кашель, одышку, боли в животе. Опухоль может распространяться на внутренние органы (легкие, печень, почки и др.).
Кроме увеличения лимфатических узлов могут наблюдаться такие симптомы, как повышение температуры, слабость, ночная потливость, зуд кожи, снижение веса. Эти симптомы учитываются при определении стадии заболевания.
Диагностика
Для диагностики ЛХ необходимо проведение биопсии пораженного лимфатического узла или его конгломерата с последующими гистологическим и иммуногистохимическим исследованиями. Опухолевый субстрат ЛХ — это клетки Рид — Штернберга (крупные двухъядерные клетки) и клетки Ходжкина, вытесняющие нормальные клетки лимфатического узла любой области организма. Злокачественные клетки окружены клеточным инфильтратом, состоящим из гистиоцитов, лимфоцитов, моноцитов, плазматических клеток и эозинофилов. Гистологический вариант ЛХ зависит от структуры реактивного микроокружения опухолевых клеток (клеточного состава).
Для определения распространенности опухолевого процесса перед началом лечения необходимо адекватное стадирование заболевания. До недавнего времени стандартными методами считались данные УЗИ периферических лимфатических узлов, органов брюшной полости и малого таза, КТ или МРТ. При необходимости выполнялась трепанобиопсия костного мозга и сцинтиграфия скелета.
В настоящее время стандартом обследования при ЛХ является позитронно-эмиссионная томография с 18F-флюородезокси-глюкозой, совмещенная с КТ (ПЭТ-КТ).
ПЭТ-КТ позволяет точнее определить вовлеченные в опухолевый процесс лимфатические узлы и области организма, определить стадию и объем лечения. В нашей стране данный метод стал доступен для всех пациентов с ЛХ с 2017 года. Определение стадии заболевания проводится по системе Энн-Арбор (Котсуолдский пересмотр стадирования, принятый на конференции в Энн-Арбор, США). Эта система стадирования учитывает количество вовлеченных в опухолевый процесс лимфатических зон и областей, расположение пораженных лимфатических узлов по одну либо по обе стороны диафрагмы, наличие либо отсутствие экстралимфатического распространения опухоли (Е), локализованный или диссиминированный процесс, а также наличие или отсутствие системных симптомом (А или В).
По Международной клинической классификации выделяют 4 стадии ЛХ.
Диагностические клетки лимфомы Ходжкина
Клетка Рид — Штернберга.
Клетка Ходжкина.
Прогноз
У детей и подростков ЛХ является одной из наиболее хорошо излечиваемых опухолей. Около 85–90 % пациентов с классической ЛХ излечиваются на ранних стадиях заболевания (в сравнении с 75–80 % пациентов с запущенной стадией). К сожалению, ежегодно от 15 % до 20 % первичных случаев ЛХ у детей и подростков в Беларуси выявляется в запущенной форме (4-я стадия).
Лечение
Лечение пациентов с ЛХ — длительный процесс, занимает от 3 до 12 месяцев и проводится по специальным протоколам. В зависимости от стадии заболевания пациенты делятся на 3 группы (со своей интенсивностью и длительностью терапии).
Терапия болезни Ходжкина состоит из двух этапов: полихимиотерапии, направленной на максимальное уничтожение злокачественных клеток и достижение ремиссии с помощью химиопрепаратов, и лучевой терапии, направленной на закрепление и длительное сохранение ремиссии путем уничтожения остаточных опухолевых клеток, которые могут в последующем стать причиной рецидива.
Результаты лечения ЛХ в РНПЦ ДОГИ
В течение последнего десятилетия в РНПЦ детской онкологии, гематологии и иммунологии используется протокол лечения ЛХ, разработанный немецкими детскими онкогематологами, показавший свою высокую эффективность. Пятилетняя общая выживаемость составляет 98 %, бессобытийная выживаемость 90 %, однако у пациентов с распространенным процессом (4-я стадия заболевания) она значительно ниже (89 % и 74 % соответственно). Наиболее значимым фактором, влияющим на эффективность лечения, является объем исходной опухоли, оцениваемый по размерам конгломератов лимфатических узлов (особенно лимфатических узлов средостения) и числу зон поражения. В последние десятилетия доля пациентов с отсутствием полного эффекта или рецидивом заболевания практически не меняется и составляет 25 % для взрослых. Среди детей и подростков с ЛХ в Беларуси таких пациентов 10 %.
В Европе и США были предприняты попытки проведения терапии у этой категории пациентов более интенсивными схемами полихимиотерапии (ПХТ). В РНПЦ ДОГИ с 2017 года также введен в практику новый протокол для лечения пациентов с ЛХ высокой группы риска. Интенсификация терапии у таких пациентов показала высокую эффективность и приемлемую токсичность.
В первые протоколы лечения ЛХ была обязательно включена лучевая терапия (ЛТ) в высоких дозах (35–40 Гр). Со временем стало очевидно, что доза облучения при комбинированном лечении может быть ниже. Кроме того, именно отсроченные эффекты ЛТ являются определяющими в развитии неблагоприятных отдаленных эффектов после проведения лечения ЛХ (вторичные опухоли, сердечно-сосудистые заболевания, нарушения функции легких).
С активным внедрением ПЭТ-КТ в диагностику лимфом началась новая эра в лечении детей с ЛХ. ПЭТ-КТ стала активно применяться не только для стадирования, но и для оценки статуса ремиссии и раннего ответа на терапию. Быстрое достижение ПЭТ-негативности является маркером чувствительности опухоли к химиотерапии. Появился способ выявлять пациентов, для которых возможно отказаться от ЛТ. С 2017 года ЛТ отменяют пациентам с ранними стадиями, достигшим полной ремиссии по данным ПЭТ-КТ после завершения этапа ПХТ.
Несмотря на существенные успехи терапии ЛХ у детей, сохраняется определенное количество терапевтических неудач, 5 % пациентов с ЛХ оказываются рефрактерными к терапии первой линии и 5 % пациентов имеют рецидив заболевания, причем в 90 % случаев он происходит в течение первых двух лет. Значительно чаще возврат заболевания наблюдается у пациентов с распространенными стадиями. Если у ребенка рецидив произошел поздно (после окончания лечения прошло больше года), то второй курс ХТ и ЛТ дают очень хорошие результаты (10-летняя выживаемость у более 90 % пациентов). Если у ребенка ранний рецидив (после окончания лечения прошло от 3 до 12 месяцев), требуется очень интенсивная терапия (высокодозная ХТ с аутологичной трансплантацией гемопоэтических стволовых клеток (аутоТГСК), чтобы иметь хорошие шансы на выздоровление. Применение стандартной ХТ второй линии у этих пациентов позволяет достичь ответа в 50 % случаев.
По мере развития знаний в области биологии, патологии и иммунологии появилась возможность находить терапевтические мишени и разрабатывать новые препараты, которые должны быть не только эффективными, но и менее токсичными. Особенно это актуально для пациентов детского и молодого возраста. Такой мишенью стал CD30-рецептор на клетках опухоли ЛХ. С 2011 года стало возможным использование схем с включением таргетного препарата (моноклональное антитело брентуксимаб ведотин для лечения пациентов с рефрактерными и рецидивными ЛХ), которое приводит к выраженному и устойчивому ответу на терапию. В РНПЦ ДОГИ с 2015 года данный препарат включен в противорецидивные схемы лечения, что позволило достичь полной ремиссии у 85 % больных с рефрактерной ЛХ.
В настоящее время продолжается разработка методов лечения, снижающих вероятность возникновения осложнений и отдаленных последствий у перенесших заболевание.
Клинический случай
Пациент М., 17 лет. Считает себя больным с июня 2016 года, когда появилась потеря в весе около 5 кг за 2 месяца, зуд кожи голеней и стоп, по вечерам подъем температуры до субфебрильных значений (макс. 37,9 °С), боли в коленных суставах и поясничной области. По месту жительства осмотрен ревматологом. Клинически при осмотре выявлено увеличение шейно-надключичных и подмышечных лимфатических узлов, в общем анализе крови отмечено повышение СОЭ до 62 мм/ч, лейкоцитоз до 12,4ґ109/л. Проведена антибактериальная терапия (амоксиклав в течение 7 дней), без эффекта. По данным УЗИ ОБП — очаговые изменения в структуре селезенки. Проконсультирован гематологом в диагностическом центре, с подозрением на лимфопролиферативное заболевание направлен в РНПЦ ДОГИ.
На момент поступления в центр (30.08.16): состояние средней тяжести. Температура 37,6 °С. Кожа и слизистые нормальной окраски, чистые. Периферические лимфатические узлы: пальпируются множественные шейные лимфоузлы с обеих сторон до 2,5 см, плотные, в надключичной области множественные плотные до 1,5 см с обеих сторон, подмышечные с двух сторон до 2,5 см, плотные, подвижные, в конгломератах. Другие группы периферических лимфоузлов не увеличены. Тоны сердца ясные, ритмичные, ЧСС — 80 в минуту. Дыхание везикулярное, хрипы не выслушиваются, ЧД — 18 в минуту. Живот мягкий, безболезненный. Печень, селезенка не увеличены.
ОАК: Нb 119 г/л, эритроциты 4,29ґ1012/л, тромбоциты 329ґ109/л, лейкоциты — 13,02ґ109/л, э — 1 %, с — 87 %, л — 7 %, м — 3 %, СОЭ — 62 мм/ч.
БАК: ЩФ — 107 МЕ/л, ЛДГ 248 МЕ/л, билирубин —17,8 мкмоль/л, АЛТ — 30, АСТ — 23, СРБ — 3,4 г/л (норма до 0,5), мочевина — 6,5 ммоль/л, креатинин — 72 ммоль/л, белок — 86,2 г/л.
УЗИ ОБП: подвздошные лимфоузлы достоверно не увеличены; структура селезенки неоднородная, единичные очаги до 10 мм в структуре селезенки; лимфоузлы у ворот печени до 14 мм.
УЗИ периферических лимфоузлов: гиперплазия нижнешейных, надключичных, подключичных и подмышечных л/узлов с обеих сторон с патологическими изменениями структуры (УЗ-картина лимфопролиферативного заболевания).
Выполнена открытая биопсия подмышечного лимфоузла слева, морфологически — участки ткани лимфоузла с наличием стертой структуры, формированием фиброзных септ и скоплений лакунарных, диагностических и клеток Ходжкина. ИГХ: CD3(+фоновые клетки), CD30(+++), CD15(++), pax5(++), CD20(-), EBV(-).
Лимфома Ходжкина, вариант нодулярный склероз, смешанноклеточный состав, grade 1. БДУ (9663/3).
ПЭТ-КТ: в переднем средостении верхнего этажа срединно с акцентом вправо опухолевая масса; 36ґ73ґ60 мм. Изолированно лежащие увеличенные лимфоузлы: паратрахеальные и бифуркационные, до 15 мм; парастернально справа, до 18 мм. По данным ПЭТ: накопление РФП помимо вышеописанных узлов — в правом корне (бронхопульмональные л/узлы), в л/узлах — прекардиально справа, в кардиодиафрагмальной области слева, параэзофагеально (на КТ узел, 14 мм).
Очагов патологической плотности в легочной паренхиме не выявлено. Легочной рисунок не изменен. Долевые и сегментарные бронхи проходимы. Корни легких не расширены, структурны. Подмышечные л/узлы не увеличены. Плевральные полости свободны. Мягкие и костные ткани грудной клетки без структурных изменений. Отмечается увеличение забрюшинных л/узлов, до 23 мм; общих подвздошных до 15 мм. На ПЭТ патологическое накопление РФП помимо вышеописанных узлов — в воротах печени, в наружных подвздошных л/узлах, в селезенке.
Патологических объемных образований в брюшной полости и забрюшинном пространстве не выявлено. Печень не увеличена, однородной структуры. Поджелудочная железа гомогенна, обычных размеров и положения. Почки без видимых изменений.
В левой подвздошной кости определяется очаг гиперденсивной плотности с мелкобугристыми контурами, размером 10,5ґ6,6 мм. На ПЭТ также отмечается повышенное накопление РФП в телах позвонков С6, Тн4, L5, S1; ребрах; костях таза.
Заключение: лимфопролиферативное заболевание с поражением лимфоузлов по обе стороны диафрагмы, селезенки, костей.
МРТ костей таза, пояснично-крестцового отдела позвоночника, бедренных костей: определяются множественные разновеликие очаги патологического сигнала в костях таза (лонных, подвздошных, седалищных с обеих сторон), бедренных костях с обеих сторон, крестце (теле с переходом на поперечный отросток слева тела L5 позвонка, а также небольшие в теле L4 (до 9–10 мм) и L2 (до 5 мм).
Заключение: МР-картина многоочагового поражения костей таза, бедренных с обеих сторон, крестца, L5, L4, L2 позвонков.
Диагноз: классическая лимфома Ходжкина (вариант нодулярный склероз) с поражением шейно-надключичных лимфоузлов с двух сторон, подключичных лимфоузлов с двух сторон, лимфоузлов средостения, корня правого легкого, подмышечных лимфоузлов с двух сторон, лимфоузлов ворот печени, парааортальных лимфоузлов, селезенки, подвздошных лимфоузлов с двух сторон, множественное поражение костей скелета. Стадия IVB.
Пациенту проведено 6 блоков ПХТ по схемам BEACOPP-escalated.
Получен полный метаболический ответ по данным ПЭТ-КТ после этапа ПХТ. С целью консолидации ремиссии проведена лучевая терапия на зоны инициального поражения в СОД=20 Гр.
Специальное лечение закончено 21.03.17. Пациент до настоящего времени находится в стойкой ремиссии, наблюдается у онколога по месту жительства.