лимфоцитарная анемия это что
Диагностика и лечение хронической аутоиммунной гемолитической анемии
Больная Ш., 80 лет, пенсионерка. Из анамнеза известно, что в течение последних двух лет неоднократно проходила амбулаторное и стационарное лечение по поводу хронической B12–фолиеводефицитной анемии, диагностированной на основании анемического синдрома в сочетании с гиперхромией и макроцитозом эритроцитов. Стернальная пункция, определение уровня витамина B12 и фолиевой кислоты не проводились. Отмечался временный незначительный положительный эффект лечения витамином B12. С конца 2011 года, несмотря на ежемесячное введение витамина B12 в дозе 500γ в сочетании с фолиевой кислотой, стала нарастать анемия (14.02.2012 г. гемоглобин – 54 г/л). Для обследования и лечения госпитализирована в больницу № 40 с диагнозом: B12–фолиеводефицитная анемия тяжелой степени. ИБС. Стенокардия напряжения II ф. к. Гипертоническая болезнь II ст. Желчнокаменная болезнь. Хронический калькулезный холецистит. Мочекаменная болезнь. Конкремент правой почки, простые кисты обеих почек. Полипы желудка.
При поступлении жалобы на выраженную общую слабость, головокружения, головную боль, учащенное сердцебиение, перебои в работе сердца.
При объективном осмотре отмечены субиктеричность кожи и слизистых оболочек, умеренная гепатомегалия (+2 см) и спленомегалия (+ 2 см).
Результаты клинического анализа в динамике представлены в таблице 1.
Таблица 1. Клинические анализы крови пациентки Ш. в динамике
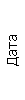 | 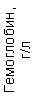 | 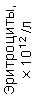 | 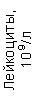 | 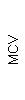 | 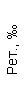 |  | 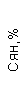 | 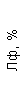 | 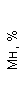 | 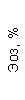 | 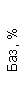 | 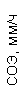 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 15.02.12 | 54 | 1.39 | 10.5 | 133 | 80 | 2 | 66 | 21 | 9 | 2 | — | 75 |
| 11.03.12 | 50 | 1.41 | 11.8 | 114 | 98 | 4 | 75 | 11 | 4 | 3 | 1 | 78 |
| 15.03.12 | 49 | 1.31 | 17.8 | 121 | 288 | 4* | 60 | 23 | 5 | 1 | — | 78 |
| 20.03.12 | 72 | 1.93 | 11.4 | 116 | 297 | 2 | 73 | 14 | 7 | 2 | 0 | 46 |
| 27.03.12 | 66 | 1.9 | 11 | 108 | 202 | 2 | 60 | 26 | 7 | 3 | 0 | 40 |
| 12.04.12 | 70 | 1.75 | 1.9 | 112 | 104 | 3 | 62 | 24 | 11 | 0 | 0 | 27 |
| 26.04.12 | 93 | 2.56 | 5.7 | 109 | 148 | 3 | 74 | 13 | 9 | 0 | 0 | 11 |
| 24.06.12 | 111 | 3.42 | 4.7 | 97 | 7 | 2 | 69 | 21 | 10 | 0 | 1 | 15 |
| 16.08.12 | 120 | 3.97 | 5.8 | 93 | 12 | — | 71 | 19 | 9 | 1 | 0 | 40 |
Примечание: * в лейкоцитарной формуле 15.03.12 выявлялись также миелоциты (2%) и метамиелоциты (5%).
В биохимическом анализе крови – повышение уровня креатинина (189 ммоль/л), билирубина (58 ммоль/л) за счет непрямого билирубина.
УЗИ органов брюшной полости: гепатоспленомегалия; камни желчного пузыря; диффузные изменения поджелудочной железы; простые кисты обеих почек, конкремент правой почки.
ФГДС: два полипа желудка размером до 0,5 см.
Учитывая высокий риск сердечно-сосудистых осложнений у пожилой пациентки с анемией тяжелой степени, проведены трансфузии эритроцитарной взвеси. На основании клинико-лабораторных данных (спленомегалия, гипербилирубинемия, гиперхромная анемия с ретикулоцитозом) и неэффективности лечения витамином B12 и фолиевой кислотой заподозрена гемолитическая анемия.
При исследовании крови на антиэритроцитарные антитела выявлены аутоантитела класса IgG ++++.
Результаты стернальной пункции представлены в таблице 2.
Таблица 2.Миелограмма пациентки Ш. от 17.02.12 г.
Заключение
Клеточный костномозговой пунктат. Эритропоэз – нормобластический. Гиперплазия эритроидного ростка – 74,8%. Со стороны эритрокариоцитов отмечаются клетки с цитоплазматическими мостиками, скопления в виде «эритроидных островков».
Мегакариоциты различной степени зрелости с умеренным тромбоцитообразованием.
На основании данных миелограммы (гиперплазия эритроидного ростка при нормобластическом типе кроветворения) и выявления антиэритроцитарных антител диагностирована аутоимунная гемолитическая анемия с тепловыми антителами. При дополнительном обследовании признаков вторичного характера анемии не выявлено.
С 11.03.12 г. начата пульс-терапия метипреднизолоном в дозе 500 мг 1 раз в день внутривенно в сочетании с пероральным приемом преднизолона в дозе 45 мг в сутки под прикрытием гастропротекторов. После 5 дней лечения анемический синдром продолжал нарастать, появился выраженный сдвиг лейкоцитарной формулы влево, увеличение количества ретикулоцитов (табл.1). Доза преднизолона перорально увеличена до 75 мг в сутки, к лечению добавлен азатиоприн по 100 мг/сутки per os, проведена трансфузия1 дозы эритроцитарной взвеси.
С 20.03.12 г. с учетом сохраняющегося гемолиза (ретикулоциты 297‰) проведен второй курс пульс-терапии метилпреднизолоном в дозе 500 мг в сутки № 4, однократно введен внутривенно циклофосфан в дозе 600 мг.
Лечение больная переносила хорошо. С 27.03.12 г. отмечена тенденция к увеличению уровня гемоглобина без поддерживающих гемотрансфузий. Решено продолжить введение циклофосфана по 200 мг в сутки, отменить азатиоприн. Анемический синдром продолжал уменьшаться: к 12.04.12 г. уровень гемоглобина достиг 70 г/л, снизился гемолиз (ретикулоцитов 104‰), однако развилась лейкопения (1,9×10 9 /л), в связи с чем циклофосфан был временно отменен. После восстановления количества лейкоцитов лечение циклофосфаном по 200 мг дважды в неделю было возобновлено на фоне постепенного снижения дозы преднизолона.
Больная в удовлетворительном состоянии 28.04.12 г. выписана из стационара. На амбулаторном этапе продолжено введение циклофосфана по 200 мг в сутки 2 раза в неделю, преднизолон в течение месяца полностью отменен.
В течение нескольких месяцев получала поддерживающую терапию циклофосфаном по 200 мг в сутки 2 раза в неделю (суммарная доза составила 7200 мг). На этом фоне уровень гемоглобина стабилен в пределах 100–120 г/л, количество ретикулоцитов не превышает 20%.
Комментарий к клиническому случаю
Аутоиммунная гемолитическая анемия (АИГА) – гетерогенная группа заболеваний и синдромов, обусловленных повышенным разрушением эритроцитов вследствие образования аутоантител. Частота АИГА во всех возрастных группах составляет 1:40000 – 1:80000, причем женщины болеют в 2 раза чаще мужчин. Выделяют первичные (идиопатические) и вторичные АИГА, которые чаще всего развиваются при лимфомах, солидных опухолях и заболеваниях соединительной ткани. По серологическим свойствам различают АИГА с тепловыми (85%) и холодовыми (15%) антителами; по месту разрушения эритроцитов выделяют АИГА с внутриклеточным (наиболее частым), внутрисосудистым и смешанным гемолизом.
Клинические проявления АИГА:
При внутрисосудистом гемолизе моча приобретает темно-бурую или черную окраску.
Лабораторные критерии:
Стандарт первой линии терапии АИГА – пероральные глюкокортикостероиды в начальной дозе 1 мг/кг в сутки, возможно проведение пульс-терапии метилпреднизолоном в дозе 0,5–1,0 г/сутки внутривенно в течение 3-5 дней. Второй линией терапии является спленэктомия, которая используется при отсутствии эффекта глюкокортикостероидов в течение 4–6 месяцев. У пожилых пациентов показано назначение иммунодепрессивных и цитостатических препаратов (азатипоприн, циклофосфон, циклоспорин). Значительно реже используют моноклональные антитела (ритуксимаб) и иммуноглобулин. Выживаемость больных АИГА в течение 5 лет составляет 75%.
При анализе данного случая обращает внимание длительное латентное течение заболевания у больной преклонного возраста с гиперхромной анемией, что послужило причиной ошибочного диагноза B12–дефицитной анемии (для АИГА характерен нормохромный характер анемии). С учетом возраста пациентки и наличия сопутствующих заболеваний было принято решение о подключении к лечению цитостатической терапии, позволившее получить ремиссию заболевания, отменить глюкокортикостероиды и отказаться от проведения спленэктомии.
Анемия: симптомы, степени, лечение
Анемия, или малокровие, – состояние, при котором уменьшается концентрация гемоглобина (переносчика кислорода) в крови. Часто сопровождается понижением количества эритроцитов (красных кровяных телец). Это не самостоятельное заболевание, а синдром других болезней.
Анемия у женщин диагностируется, если гемоглобин опускается ниже 120 г/л (при беременности – ниже 110 г/л), а у мужчин, если показатель понижается до 130 г/л.
При малокровии клетки и ткани не получают достаточного количества кислорода, что приводит к нарушению функционирования внутренних органов, способствует развитию других заболеваний.
Виды анемии
В зависимости от причины различают 4 группы патологии:
Известно несколько разновидностей дефицитной патологии:
Самые распространенные формы гемолитической анемии:
Вид анемии определяется врачом — терапевтом или гематологом на основе анализов крови.
Симптомы анемии
Признаки патологии зависят от ее вида и степени тяжести. Легкая форма часто протекает бессимптомно. Возможны общая слабость, повышенная утомляемость, ослабление внимания. В тяжелых случаях (при понижении гемоглобина ниже 50 г/л) может развиться ацидоз (закисление крови), сердечная недостаточность.
К общим признакам, сопровождающим все виды анемии, принадлежат:
Для железодефицитной формы характерны наличие трещин и заед в углах рта, поперечная исчерченность, слоистость и ломкость ногтей, сечение и выпадение волос, искажение вкусовых предпочтений (желание есть мел, землю), понижение артериального давления, обмороки.
При В12-дефицитной анемии человек ощущает покалывание и онемение в пальцах, чувство ползания мурашек, скованность и отечность конечностей, кожа приобретает желтоватый оттенок, а язык – малиновый, походка становится шаткой.
При апластическом малокровии в грудной области возникают колющие боли, физические усилия сопровождаются одышкой. На коже появляются мелкие кровоизлияния (петехии) в виде красной сыпи, кровоточат десны, менструации становятся длительными и обильными.
При фолиеводефицитной форме затрудняется пережевывание и глотание пищи, атрофируются слизистые оболочки ЖКТ, развивается непереносимость кислой пищи.
При постгеморрагической анемии кружится голова, понижаются давление и температура тела, учащается (но становится слабым) пульс, появляется холодный пот. Если кровотечение обильное, то возможны судороги, коматозное состояние и даже остановка сердца.
Для гемолитического малокровия характерны желтушность кожи и слизистых оболочек, потемнение мочи и кала, повышенная температура тела, увеличение размеров печени или селезенки.
При гипопластической форме усиливается кровоточивость десен, в ротовой полости образуются язвы, на коже появляются синяки, развивается тахикардия, постоянно хочется спать.
Степени анемии
В зависимости от уровня гемоглобина различают 3 степени анемии:
Причины возникновения анемии
Спровоцировать развитие анемии способны различные факторы:
Часто анемия развивается при:
В группу риска входят вегетарианцы, доноры, профессиональные спортсмены, беременные женщины.
Основная причина анемии у детей – быстрый рост, требующий усиленного питания, и несовершенство механизмов кроветворения. В результате ослабляется иммунная система, усиливается восприимчивость к инфекционным заболеваниям.
Лечение анемии
Метод терапии врач подбирает индивидуально в зависимости от причины малокровия и тяжести состояния.
При железодефицитной анемии доктор порекомендует включить в свой рацион продукты, богатые железом. При необходимости назначит железосодержащие препараты.
Если малокровие вызвано инфекцией или интоксикацией, то необходимо избавиться от возбудителя болезни и провести детоксикацию организма.
При постгеморрагической анемии следует остановить кровотечение. Дополнительно приписывают лекарства, нормализующие объем крови и количество кровяных клеток. Если возникает угроза для жизни, переливают кровь, вводят кровезаменители.
Гемолитическую анемию лечат анаболическими гормонами и глюкокортикоидами. Дополнительно назначают витамины. Если консервативное лечение оказывается неэффективным, то прибегают к операции, во время которой удаляют селезенку.
При гипопластической форме стимулируют процессы кроветворения, выполняют переливание крови, делают пересадку костного мозга.
Серповидно-клеточную анемию лечат вливанием кровезаменителей или эритроцитарной массы.
Диагностика и лечение хронической аутоиммунной гемолитической анемии
Больная Ш., 80 лет, пенсионерка. Из анамнеза известно, что в течение последних двух лет неоднократно проходила амбулаторное и стационарное лечение по поводу хронической B12–фолиеводефицитной анемии, диагностированной на основании анемического синдрома в сочетании с гиперхромией и макроцитозом эритроцитов. Стернальная пункция, определение уровня витамина B12 и фолиевой кислоты не проводились. Отмечался временный незначительный положительный эффект лечения витамином B12. С конца 2011 года, несмотря на ежемесячное введение витамина B12 в дозе 500γ в сочетании с фолиевой кислотой, стала нарастать анемия (14.02.2012 г. гемоглобин – 54 г/л). Для обследования и лечения госпитализирована в больницу № 40 с диагнозом: B12–фолиеводефицитная анемия тяжелой степени. ИБС. Стенокардия напряжения II ф. к. Гипертоническая болезнь II ст. Желчнокаменная болезнь. Хронический калькулезный холецистит. Мочекаменная болезнь. Конкремент правой почки, простые кисты обеих почек. Полипы желудка.
При поступлении жалобы на выраженную общую слабость, головокружения, головную боль, учащенное сердцебиение, перебои в работе сердца.
При объективном осмотре отмечены субиктеричность кожи и слизистых оболочек, умеренная гепатомегалия (+2 см) и спленомегалия (+ 2 см).
Результаты клинического анализа в динамике представлены в таблице 1.
Таблица 1. Клинические анализы крови пациентки Ш. в динамике
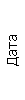 | 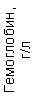 | 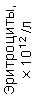 | 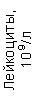 | 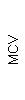 | 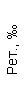 |  | 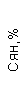 | 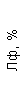 |  |  |  |  |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 15.02.12 | 54 | 1.39 | 10.5 | 133 | 80 | 2 | 66 | 21 | 9 | 2 | — | 75 |
| 11.03.12 | 50 | 1.41 | 11.8 | 114 | 98 | 4 | 75 | 11 | 4 | 3 | 1 | 78 |
| 15.03.12 | 49 | 1.31 | 17.8 | 121 | 288 | 4* | 60 | 23 | 5 | 1 | — | 78 |
| 20.03.12 | 72 | 1.93 | 11.4 | 116 | 297 | 2 | 73 | 14 | 7 | 2 | 0 | 46 |
| 27.03.12 | 66 | 1.9 | 11 | 108 | 202 | 2 | 60 | 26 | 7 | 3 | 0 | 40 |
| 12.04.12 | 70 | 1.75 | 1.9 | 112 | 104 | 3 | 62 | 24 | 11 | 0 | 0 | 27 |
| 26.04.12 | 93 | 2.56 | 5.7 | 109 | 148 | 3 | 74 | 13 | 9 | 0 | 0 | 11 |
| 24.06.12 | 111 | 3.42 | 4.7 | 97 | 7 | 2 | 69 | 21 | 10 | 0 | 1 | 15 |
| 16.08.12 | 120 | 3.97 | 5.8 | 93 | 12 | — | 71 | 19 | 9 | 1 | 0 | 40 |
Примечание: * в лейкоцитарной формуле 15.03.12 выявлялись также миелоциты (2%) и метамиелоциты (5%).
В биохимическом анализе крови – повышение уровня креатинина (189 ммоль/л), билирубина (58 ммоль/л) за счет непрямого билирубина.
УЗИ органов брюшной полости: гепатоспленомегалия; камни желчного пузыря; диффузные изменения поджелудочной железы; простые кисты обеих почек, конкремент правой почки.
ФГДС: два полипа желудка размером до 0,5 см.
Учитывая высокий риск сердечно-сосудистых осложнений у пожилой пациентки с анемией тяжелой степени, проведены трансфузии эритроцитарной взвеси. На основании клинико-лабораторных данных (спленомегалия, гипербилирубинемия, гиперхромная анемия с ретикулоцитозом) и неэффективности лечения витамином B12 и фолиевой кислотой заподозрена гемолитическая анемия.
При исследовании крови на антиэритроцитарные антитела выявлены аутоантитела класса IgG ++++.
Результаты стернальной пункции представлены в таблице 2.
Таблица 2.Миелограмма пациентки Ш. от 17.02.12 г.
Заключение
Клеточный костномозговой пунктат. Эритропоэз – нормобластический. Гиперплазия эритроидного ростка – 74,8%. Со стороны эритрокариоцитов отмечаются клетки с цитоплазматическими мостиками, скопления в виде «эритроидных островков».
Мегакариоциты различной степени зрелости с умеренным тромбоцитообразованием.
На основании данных миелограммы (гиперплазия эритроидного ростка при нормобластическом типе кроветворения) и выявления антиэритроцитарных антител диагностирована аутоимунная гемолитическая анемия с тепловыми антителами. При дополнительном обследовании признаков вторичного характера анемии не выявлено.
С 11.03.12 г. начата пульс-терапия метипреднизолоном в дозе 500 мг 1 раз в день внутривенно в сочетании с пероральным приемом преднизолона в дозе 45 мг в сутки под прикрытием гастропротекторов. После 5 дней лечения анемический синдром продолжал нарастать, появился выраженный сдвиг лейкоцитарной формулы влево, увеличение количества ретикулоцитов (табл.1). Доза преднизолона перорально увеличена до 75 мг в сутки, к лечению добавлен азатиоприн по 100 мг/сутки per os, проведена трансфузия1 дозы эритроцитарной взвеси.
С 20.03.12 г. с учетом сохраняющегося гемолиза (ретикулоциты 297‰) проведен второй курс пульс-терапии метилпреднизолоном в дозе 500 мг в сутки № 4, однократно введен внутривенно циклофосфан в дозе 600 мг.
Лечение больная переносила хорошо. С 27.03.12 г. отмечена тенденция к увеличению уровня гемоглобина без поддерживающих гемотрансфузий. Решено продолжить введение циклофосфана по 200 мг в сутки, отменить азатиоприн. Анемический синдром продолжал уменьшаться: к 12.04.12 г. уровень гемоглобина достиг 70 г/л, снизился гемолиз (ретикулоцитов 104‰), однако развилась лейкопения (1,9×10 9 /л), в связи с чем циклофосфан был временно отменен. После восстановления количества лейкоцитов лечение циклофосфаном по 200 мг дважды в неделю было возобновлено на фоне постепенного снижения дозы преднизолона.
Больная в удовлетворительном состоянии 28.04.12 г. выписана из стационара. На амбулаторном этапе продолжено введение циклофосфана по 200 мг в сутки 2 раза в неделю, преднизолон в течение месяца полностью отменен.
В течение нескольких месяцев получала поддерживающую терапию циклофосфаном по 200 мг в сутки 2 раза в неделю (суммарная доза составила 7200 мг). На этом фоне уровень гемоглобина стабилен в пределах 100–120 г/л, количество ретикулоцитов не превышает 20%.
Комментарий к клиническому случаю
Аутоиммунная гемолитическая анемия (АИГА) – гетерогенная группа заболеваний и синдромов, обусловленных повышенным разрушением эритроцитов вследствие образования аутоантител. Частота АИГА во всех возрастных группах составляет 1:40000 – 1:80000, причем женщины болеют в 2 раза чаще мужчин. Выделяют первичные (идиопатические) и вторичные АИГА, которые чаще всего развиваются при лимфомах, солидных опухолях и заболеваниях соединительной ткани. По серологическим свойствам различают АИГА с тепловыми (85%) и холодовыми (15%) антителами; по месту разрушения эритроцитов выделяют АИГА с внутриклеточным (наиболее частым), внутрисосудистым и смешанным гемолизом.
Клинические проявления АИГА:
При внутрисосудистом гемолизе моча приобретает темно-бурую или черную окраску.
Лабораторные критерии:
Стандарт первой линии терапии АИГА – пероральные глюкокортикостероиды в начальной дозе 1 мг/кг в сутки, возможно проведение пульс-терапии метилпреднизолоном в дозе 0,5–1,0 г/сутки внутривенно в течение 3-5 дней. Второй линией терапии является спленэктомия, которая используется при отсутствии эффекта глюкокортикостероидов в течение 4–6 месяцев. У пожилых пациентов показано назначение иммунодепрессивных и цитостатических препаратов (азатипоприн, циклофосфон, циклоспорин). Значительно реже используют моноклональные антитела (ритуксимаб) и иммуноглобулин. Выживаемость больных АИГА в течение 5 лет составляет 75%.
При анализе данного случая обращает внимание длительное латентное течение заболевания у больной преклонного возраста с гиперхромной анемией, что послужило причиной ошибочного диагноза B12–дефицитной анемии (для АИГА характерен нормохромный характер анемии). С учетом возраста пациентки и наличия сопутствующих заболеваний было принято решение о подключении к лечению цитостатической терапии, позволившее получить ремиссию заболевания, отменить глюкокортикостероиды и отказаться от проведения спленэктомии.
Аутоиммунная гемолитическая анемия у взрослых
Общая информация
Краткое описание
НАЦИОНАЛЬНОЕ ГЕМАТОЛОГИЧЕСКОЕ ОБЩЕСТВО
Рекомендации утверждены на IV Конгрессе гематологов России (апрель 2018г)
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ДИАГНОСТИКЕ И ЛЕЧЕНИЮ АУТОИММУННОЙ ГЕМОЛИТИЧЕСКОЙ АНЕМИИ (АИГА) У ВЗРОСЛЫХ
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
АИГА разделяют на первичные (идиопатические) и более распространенные вторичные, встречающиеся при других заболеваниях. Вторичные АИГА чаще всего сопряжены с лимфоцитарными опухолями, системной красной волчанкой (СКВ), ревматоидным артритом, а также с неспецифическим язвенным колитом, врожденными иммунодефицитами, раком толстой кишки, легких, желудка и яичников, некоторыми инфекциями. В одних случаях АИГА обнаруживают в ходе длительно текущей болезни, а в других гемолиз предшествует проявлению указанных заболеваний, нередко затрудняя своевременную диагностику.
По механизму разрушения эритроцитов выделяют внутриклеточный, внутрисосудистый и смешанный варианты гемолиза.
Cерологические свойства аутоантител легли в основу деления АИГА на четыре формы: 1) с неполными тепловыми агглютининами (80% всех больных); 2) с полными холодовыми агглютининами (12—15% всех случаев); 3) с тепловыми гемолизинами; 4) с двухфазными холодовыми гемолизинами Доната—Ландштейнера (крайне редкая и, как правило, вторичная форма при сифилисе и вирусных инфекциях). Тип антител во многом определяет клинические проявления гемолиза, выбор лечения и прогноз.
Этиология и патогенез
Причина развития АИГА — срыв иммунологической толерантности к собственным антигенам. Механизм этого процесса до сих пор не изучен. Поскольку АИГА — редкое заболевание, не исключено, что готовность к подобным нарушениям в какой-то мере обусловлена теми или иными генетическими дефектами T-лимфоцитов. Показано, что при АИГА, как и при многих других аутоагрессивных заболеваниях, имеет место подавление супрессорной функции T-лимфоцитов, что способствует увеличению популяции B-лимфоцитов, образующих антитела против собственных структур [22]. Срыв толерантности происходит, когда она формируется в присутствии малых количеств антигена. Толерантность, развившаяся после контакта с большим количеством антигена, практически не исчезает. В качестве примера обычно приводят отсутствие аутоагрессии против антигенов системы AB0. Различные формы АИГА могут иметь в своей основе разные ведущие причины. Имеются сведения о выявлении антилимфоцитарных антител и антилимфоцитотоксинов при различных аутоиммунных заболеваниях. При B-клеточных опухолях аутоантитела — продукт опухолевого клона.
Свойства аутоантител определяют особенности различных форм АИГА. Неполные аутоагглютины вызывают агглютинацию эритроцитов только в водно-солевой среде, в то время как действие полных проявляется в любой среде [19, 23]. Неполные тепловые антитела фиксированы на эритроцитах и взаимодействуют через Fc-фрагменты иммуноглобулинов с Fc-рецепторами макрофагов, из-за чего теряется часть мембраны эритроцита, изменяется ее биофизическое состояние и прежде всего — свойства ионных каналов. Это приводит к образованию микросфероцитов и резкому ускорению разрушения (секвестрации) эритроцитов в селезенке, а иногда и в печени [20]. Холодовые агглютинины вызывают транзиторное склеивание эритроцитов на холоде, что приводит к фиксации и активации комплемента на их поверхности с последующим повреждением мембраны. Гемолизины активируют комплемент, повреждающий мембрану внутри сосудистого русла. При этой форме АИГА инфекционный агент может иметь сходство с антигенными структурами эритроцита или на первом этапе несколько видоизменять их, что в дальнейшем приводит к аутосенсибилизации.
В развитии АИГА нередко принимают участие два класса антител: IgG и IgА или IgG и IgM, а также комплемент, что определяет как патофизиологию, так и лечение АИГА. У больных с аутоантителами IgM-класса, фиксирующими комплемент, спленэктомия не приводит к прекращению гемолиза, поскольку в разрушении эритроцитов активно участвуют фагоциты печени [24].
Клиническая картина
Cимптомы, течение
Основные клинические и лабораторные проявления АИГА — нормоцитарная анемия с быстро нарастающей слабостью и плохой адаптацией даже к умеренному снижению уровня гемоглобина, бледность и желтушность кожи и склер. Могут быть темная моча и боли в поясничной области, нередко субфебрильная температура и небольшое увеличение размеров селезенки. Спленомегалия у пациента старше 50—60 лет, как правило, заставляет думать о вторичной АИГА, связанной с лимфопролиферативным заболеванием. При холодовой гемагглютининовой болезни степень анемии колеблется в широком диапазоне, но, как правило, анемия выражена умеренно и сопровождается симптомами, связанными с феноменом склеивания эритроцитов, что затрудняет проведение анализа крови. При длительном охлаждении возможно развитие синдрома Рейно, некрозов и бронхоспазма.
Лабораторное обследование выявляет снижение уровня гемоглобина, от умеренного до 26—36 г/л, и соответствующее уменьшение количества эритроцитов при высоком ретикулоцитозе. Число лейкоцитов и тромбоцитов обычно не изменено, но при интенсивном гемолизе возможны лейкоцитоз с омоложением лейкоцитарной формулы, а также тромбоцитоз или тромбоцитопения. В мазке периферической крови, как правило, — сочетание микросфероцитов с крупными ортохромными эритроцитами, но в зависимости от свойств антител могут наблюдаться холодовая агглютинация и, иногда, шистоциты. Ключевые изменения биохимических показателей крови: гипербилирубинемия (преобладает непрямая, неконъюгированная фракция), повышение активности ЛДГ в сыворотке в 2—8 раз (в зависимости от интенсивности гемолиза).
Прямая проба Кумбса в большинстве случаев положительна, но при массивном гемолизе, а также при холодовых и гемолизиновых формах АИГА, вызванных IgА- или IgM-аутоантителами, может быть отрицательной [24]. При гемолизиновых формах АИГА и тяжелом гемолитическом кризе с активацией комплемента обнаруживают повышение уровня свободного гемоглобина плазмы (гемоглобинемия), темный, бурый или вишневый цвет мочи (гемоглобинурия). При первичном обследовании в стационаре с ограниченными возможностями лабораторной диагностики инкубация в плазме и/или сыворотке больного (при 37C в течение 24—48 ч) как его собственных, так и донорских эритроцитов помогает заподозрить гемолиз (скрининг-тесты Кросби и Хегглина—Майера). В таких случаях с помощью проточной цитометрии необходимо исключить наличие ПНГ-клона среди эритроцитов, нейтрофилов и моноцитов (приобретенный дефект клеточной мембраны, лишающий ее защиты от мембранатакующего комплекса комплемента, — определяется по отсутствию экспрессии рецепторов CD59, CD24, CD14, CD66 и CD16, а также по отсутствию фиксирующего их якорного белка в реакции с флюоресцентным аэролизином [FLAER]). В некоторых случаях АИГА транзиторное снижение экспрессии CD55, реже CD59 на части эритроцитов при отсутствии дефекта мембраны нейтрофилов и моноцитов не является свидетельством появления ПНГ-клона.
Имеет значение «снижение» уровня гаптоглобина сыворотки при всех видах гемолиза. Этот феномен обусловлен тем, что гаптоглобин, уже перенасыщенный гемоглобином из разрушенных эритроцитов, перестает связывать добавленный в пробирку меченый гемоглобин. Изменены биофизические свойства эритроцитов, их деформируемость (пластичность), распределение по плотности. К сожалению, эти простые тесты, информативные для диагностики разных анемий и контроля эффективности лечения, не входят в стандарт клинических лабораторий.
Диагностика
Лечение
Тактика лечения АИГА зависит в первую очередь от ее серологической разновидности и остроты гемолитического криза. При лечении криза первичной и вторичной АИГА принципиальных различий нет. Наибольшие успехи достигнуты в лечении самой распространенной формы АИГА — с положительной прямой пробой Кумбса, вызванной неполными тепловыми агглютининами. Основное содержание данного раздела касается именно этой формы. Сведения о лечении других, более редких, серологических форм АИГА разрозненны и противоречивы (эту информацию мы не стали выделять в отдельный раздел).
На протяжении полувека независимо от формы АИГА первой линией терапии остаются глюкокортикоиды (преднизолон и эквивалентные дозы дексаметазона, триамцинолона, метилпреднизолона). При этом начальная доза преднизолона зависела, как правило, от остроты процесса. Общепринятая начальная доза — 1 мг/кг в сутки (50—80 мг/сут). Увеличение дозы преднизолона до 2 мг/кг/сут (90—160 мг/сут) не улучшает результаты лечения, приводя к быстрому развитию характерных тяжелых осложнений. Первый гемолитический криз, как правило, удается купировать. В течение двух недель прекращается падение гемоглобина, исчезает гипертермия. Через 3—4 недели уровень гемоглобина может достигнуть нормы. Стремление к быстрому уменьшению дозы с момента нормализации гемоглобина из-за побочного действия глюкокортикоидов (кушингоид, стероидные язвы, артериальная гипертония, угревая сыпь с формированием гнойничков на коже, бактериальные инфекции, сахарный диабет, остеопороз, венозные тромбозы) всегда приводит к рецидиву гемолиза. Снижать дозу преднизолона начинают по 5—10 мг за 2—3 дня и продолжают до тех пор, пока суточная доза не достигнет 25—30 мг. Далее отмена препарата проводится значительно медленнее — по 2,5 мг за 5—7 дней. После достижения дозы ниже 10—15 мг должен сохраняться замедленный темп отмены. Такая тактика предполагает прием преднизолона в течение 3—4 месяцев. При меньшей продолжительности поддерживающей терапии рецидив гемолиза практически неизбежен. Стойкой ремиссии достигают только у 7—22% пациентов [2]. При большей длительности лечения число клинических ремиссий может увеличиться, но нарастают и нежелательные явления. Повторные курсы глюкокортикоиды нередко дают меньший эффект, в то время как осложнения превращаются в терапевтическую проблему, конкурирующую с самой АИГА. Основной причиной смерти таких больных является не гемолиз, а тромбозы, тромбоэмболии, бактериальные и грибковые инфекции (пневмония, уросепсис, септический эндокардит). Диагноз рецидивирующей формы АИГА, а точнее резистентности к первой линии терапии, фактически формируется после первого же рецидива гемолиза. При АИГА с холодовыми агглютининами глюкокортикоиды, как правило, малоэффективны, а необъяснимые колебания уровней эритроцитов и гемоглобина, чаще технические, корректируются при 37С (пример: эритроциты — 0,7 1012/л, после согревания кюветы — 2,9 1012/л, что предотвратило необоснованную трансфузию эритроцитов).
В литературе мало сведений о пульс-терапии метилпреднизолоном (10—30 мг/кг/сут) или дексаметазоном (40 мг/кг/сут) при АИГА [3, 4], но такой подход используют при СКВ и других коллагенозах. Метилпреднизолон обычно вводят по 1000 мг/сут в течение 2—5 дней (как правило, 3 дней). В мировой практике пульс-терапию чаще всего применяют для обрыва гемолиза на первом этапе тяжелой АИГА, а затем возвращаются к обычному приему глюкокортикоидов внутрь, описанному выше. Рандомизированные исследования отсутствуют. Результаты, полученные в НМИЦ гематологии у 28 пациентов (возраст от 18 до 72 лет), показали, что многократные пульсовые трехдневные введения метилпреднизолона значительно увеличивают частоту ремиссий и уменьшают риск осложнений по сравнению со стандартным режимом гормонотерапии. Кроме того, собственные наблюдения выявили, что мониторинг таких показателей, как нормализация фракции незрелых ретикулоцитов (IRF — Immature Reticulocyte Fraction), среднего уровня креатина в эритроцитах, распределения эритроцитов по плотности наряду с восстановлением уровней гемоглобина, эритроцитов, ретикулоцитов и активности ЛДГ дает более строгие критерии полной ремиссии. Перечисленные дополнительные показатели активности гемолиза достигали нормы только после 6—8 курсов пульс-терапии [4, 12].
Циклоспорин (Сандиммун Неорал) может приводить к развитию ремиссий у ранее резистентных больных [7—9]. Однако число описанных случаев невелико — около десяти. Препарат назначали либо в виде монотерапии, либо в сочетании с преднизолоном или даназолом, при этом начальные дозы существенно различались. При низкой поддерживающей дозе циклоспорина в течение длительного времени выраженные побочные явления отсутствовали. Emilia et al лечили трех пациентов, начиная с 5 мг/кг/сут в 2 приема. Через 6 дней дозу циклоспорина снизили до 3 мг/кг/сут, далее поддерживали в крови концентрацию препарата, равную 200—400 нг/мл. Литературные данные свидетельствуют о возможности длительных ремиссий (1—2 года) у ранее резистентных больных, в том числе при вторичных и гемолизиновых формах АИГА, а также синдроме Фишера—Эванса. Требуется продолжительная поддерживающая терапия. Однако отмечались и неудачи.
Даназол в практике лечения АИГА так и не нашел широкого применения. Этот препарат назначали на длительный период в дозе 200 мг/сут с последующим ее увеличением до 400 мг/сут и более при хорошей переносимости. Часто даназол назначали в составе комплексной терапии. Несмотря на то, что сообщалось о достижении ремиссии продолжительностью до 5 лет у резистентных больных с идиопатической формой АИГА в 77% случаев и с вторичной формой АИГА — в 60% случаев [10], даназол мало используют в лечении АИГА. За последние 10 лет на эту тему были единичные публикации [11]. Тем не менее интерес к препарату пока полностью не утрачен.
Правильная и своевременная диагностика АИГА с неполными тепловыми агглютининами обеспечивает адекватную тактику лечения и восстановление гематологических показателей через 3—5 недель. Признаки улучшения состояния больного, уменьшение «анемических» жалоб наблюдаются в течение первой недели лечения, повышение уровня гемоглобина — только через 7—10 дней. Адекватность терапии можно оценить по нормализации уровней гемоглобина, ретикулоцитов, билирубина, активности ЛДГ. Кроме того, после стабилизации показателей гемограммы желательно выбрать для мониторинга один или несколько дополнительных показателей активности гемолиза: фракцию незрелых ретикулоцитов (IRF) (при наличии клинического анализатора), распределение эритроцитов по плотности. В процессе лечения контрольные исследования гемограммы и биохимических показателей проводят не реже 3 раз в месяц, после достижения ремиссии — каждые 1,5—2 месяца.
Рекомендации по лечению АИГА, опубликованные в последние 5 лет, должны применяться с учетом индивидуальных особенностей каждого пациента и допускать обоснованные альтернативные решения [12].
Метилпреднизолон вводят в дозе 500 мг (редко 1000 мг) в/в капельно (1,5—2 ч) в течение 3 дней, иногда 4—5 дней. В начале лечения проводят два курса пульс-терапии с интервалом 5—10 дней, не допуская усиления гемолиза.
Одно из наиболее распространенных и серьезных осложнений после проведения спленэктомии — аспленический тромбоцитоз. Поэтому в зависимости от степени риска тромбозов проводится профилактика дезагрегантами и/или низкомолекулярными гепаринами, как указано выше. При тромбоцитозе более 1500 10 9 /л возможно назначение гидроксимочевины, 1000—1500 мг/сут, под контролем гемограммы 2 раза в неделю.
Основанием для повторного курса ритуксимаба являются доклинические признаки рецидива гемолиза, определяемые по динамике стандартных лабораторных показателей — уровня гемоглобина, количества эритроцитов и ретикулоцитов, активности ЛДГ, уровня билирубина, а также по результатам принятых в НМИЦ гематологии более чувствительных методов мониторинга — распределению эритроцитов по плотности, их деформируемости, фракции незрелых ретикулоцитов (IRF) и/или среднему уровню креатина эритроцитов, количеству иммуноглобулинов на мембране эритроцитов.
Информация
Источники и литература
Информация
Конфликт интересов: авторы не имеют конфликта интересов.




