митохондриальная патология что это
Митохондриальная миопатия
Митохондриальные миопатии — это группа заболеваний мышц, которые возникают в результате нарушения функции тканевого дыхания при патологиях митохондрий. Болезни проявляются нарастающей мышечной слабостью, атрофией мускулатуры, прогрессирующими двигательными расстройствами, которые могут сопровождаться судорогами, поражениями сердца, ухудшением слуха и зрения. Диагностика предполагает лабораторные (исследование мышечных биоптатов, генетическое тестирование, биохимические анализы), инструментальные методы (ЭМГ, церебральное МР-сканирование). Лечение включает симптоматические препараты, физиотерапию, ЛФК.
МКБ-10
Общие сведения
Термин «митохондриальная миопатия» объединяет в себе несколько патологий со сходным патогенезом. Наиболее часто дети страдают синдромами MELAS, MERRF, синдромом Кернса-Сайра с хронической прогрессирующей наружной офтальмоплегией. Изучение молекулярно-генетических особенностей этих болезней началось в 1980-х гг. Распространенность патологий у детей составляет около 11,5 случая на 100 тыс. населения. Из-за мультисистемности поражения, клинического полиморфизма, вариабельности течения этот вид миопатии представляет серьезные трудности в диагностике.
Причины
Миопатии обусловлены наследственными либо спорадическими мутациями в митохондриальной ДНК или в ядерных генах, контролирующих работу митохондрий. Известно более 300 вариантов генных дефектов — однонуклеотидных замен, делеций, вызывающих нарушения функционирования митохондрий. Митохондриальные миопатии имеют ряд генетических аспектов, выделяющих их среди всех наследственных заболеваний. Принципиальные различия:
Патогенез
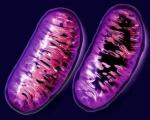
Митохондрия — универсальная органелла, присутствующая во всех клетках, кроме эритроцитов. Она имеет дыхательную цепь, которая включает 5 ферментных комплексов из нескольких десятков субъединиц каждый. Ферменты обеспечивают окислительное фосфорилирование для синтеза АТФ — аденозинтрифосфата, выступающего основным источником энергии в организме.
При митохондриальных заболеваниях может быть 4 варианта патогенетических механизмов развития. Как правило, при поражениях мышц наблюдаются дефекты электронного транспорта и окислительного фосфорилирования, что сопровождается нарушениями образования энергетических молекул. Другие варианты расстройств включают нарушения обмена пирувата, дефекты метаболизма жирных кислот, дисфункцию цикла Кребса.
При миопатиях отмечаются полисистемные расстройства. Мышечная и нервная ткань, больше других зависимые от энергопроизводства, страдают в первую очередь. Поражение проявляется нарушениями обмена веществ в мышцах, дегенеративными процессами, атрофией миофибрилл и их замещением соединительной тканью. Со временем патологический процесс распространяется на сердечную мышцу, эндокринную систему, почки и печень, что определяет различные «маски» миопатии.
Симптомы митохондриальной миопатии
Патологии манифестируют у детей раннего возраста, иногда они присутствуют с рождения. Общим признаком является миопатический синдром, который включает прогрессирующую мышечную слабость, снижение тонуса скелетной мускулатуры, непереносимость физических нагрузок. Типично отставание в моторном развитии: дети поздно начинают сидеть, ползать, ходить, у них сохраняется неуклюжесть движений, проблемы с поддержанием равновесия.
Клинические особенности определяются типом заболевания. При синдроме MERRF мышечная слабость сопровождается разнообразными судорожными приступами (атоническими, тонико-клоническими, миоклоническими), расстройствами координации вследствие мозжечковой атаксии. Для синдрома MELAS характерны повторные инсульты, умственная отсталость, нейросенсорная тугоухость.
У детей распространен синдром Кернса-Сайра, при котором клинические признаки дополняются расстройствами глотания, нарушениями работы проводящей системы сердца, снижением слуха. Хроническая прогрессирующая наружная офтальмопатия может возникать как компонент болезни Кернса-Сайра, так и развиваться изолированно, что чаще бывает в старшем возрасте.
Осложнения
Отличительными особенностями миопатического синдрома являются необратимость, неуклонное прогрессирование. Сначала мышечная слабость появляется в проксимальных отделах конечностей, затем поражает все тело ребенка: в процесс вовлекается гладкая мускулатура органов дыхания и пищеварения, что чревато дыхательной недостаточностью, аспирационными пневмониями, тотальным параличом. Такие пациенты теряют способность к самообслуживанию, требуют круглосуточного ухода.
Миопатии осложняются деформациями позвоночника, искривлениями нижних конечностей на фоне слабости мышечного корсета. Вследствие атрофии зрительных нервов у больных с синдромом MERRF возникает слепота. Опасным последствием многих вариантов митохондриальной патологии являются инсульты, эпилептический статус, мозговой отек, которые становятся основными причинами летального исхода.
Диагностика
Первичное обследование детей с подозрением на митохондриальную миопатию проводится у невролога, для уточнения диагноза показана консультация генетика. При осмотре учитывается неврологический статус ребенка, показатели мышечной силы и тонуса, уровень развития когнитивных навыков. Постановка диагноза требует комплексного обследования, включающего следующие методы:
Лечение митохондриальных миопатий
В клинической неврологии отсутствуют эффективные методы терапии патологии у детей. Суть медицинской помощи сводится к уменьшению моторного дефицита, своевременной коррекции осложнений, стимуляции обменных процессов в митохондриях. Наибольшую результативность демонстрируют следующие группы медикаментов:
Важным компонентом лечения у детей является нейродиетология, которая предполагает исключение веществ, оказывающих негативное влияние на обменные процессы (терапия «обхождения блока»). Рекомендована кетогенная диета, другие виды высокожировых диет. По показаниям проводится лечебное энтеральное или парентеральное питание, в тяжелых случаях устанавливается гастростома.
Прогноз и профилактика
Митохондриальные заболевания
Митохондриальные заболевания (МЗ) — группа наследственных заболеваний, связанных с дефектами в функционировании митохондрий, приводящими к нарушениям энергетических функций в клетках.
Историческая справка:
Понятие «митохондриальные болезни» сформировалось в медицине в конце ХХ века. В первую очередь были изучены болезни, связанные с мутациями митохондриальной ДНК, открытой в начале 60-ых годов. Полная первичная структура митохондриальной ДНК человека была опубликована в 1981 го¬ду и уже в конце 80-ых годов была доказана ведущая роль ее мутаций в развитии ряда наследственных заболеваний. К последним относятся: наследственная атрофия зрительных нервов Лебера, синдром NARP (нейропатия, атаксия, пигментный ретинит), синдром MERRF (миоклонусэпилепсия с «рваными» красными волокнами в скелетных мышцах), синдром MELAS (митохондриальная энцефаломиопатия, лактат-ацидоз, инсультоподобные эпизоды), синдром Кернса-Сейра (пигментный ретинит, наружная офтальмоплегия, блокада сердца, птоз, мозжечковый синдром), синдром Пирсона (поражение костного мозга, панкреатическая и печеночная дисфункции) и многие другие.
В меньшей степени изучены наследственные митохондриальные дефекты, связанные с повреждением ядерного генома.
Патогенез.
Митохондрии отвечают за выработку большей части энергии, необходимой для функционирования клеток. Фактически они являются настолько важным источником энергии, что в каждой клетке их сотни. При МЗ могут «выключиться» как часть митохондрий, так и все они, что приводит к прекращению выработки необходимой энергии
Поскольку наиболее энергоемкими являются нервные и мышечные клетки, при МЗ наиболее распространены мышечные и неврологические проблемы, такие, как мышечная слабость, непереносимость физических нагрузок, потеря слуха, нарушения баланса и координации, эпиприступы.
Когда клетка заполнена дефектными митохондриями, она не только лишена АТФ, но в ней могут накапливаться неиспользуемые молекулы топлива и кислород, что приводит к катастрофическим последствиям. В этом случае избыточные молекулы топлива используются для синтеза АТФ неэффективно, в результате чего могут образовываться потенциально опасные продукты, такие, как молочная кислота (Это также происходит, когда клетки испытывают недостаток кислорода, например – мышечные клетки при усиленных физических нагрузках). Накопление молочной кислоты в крови – лактатацидоз – ассоциировано с мышечной усталостью, и может вызывать повреждение нервной и мышечной тканей.
При этом неиспользуемый в клетке кислород может трансформироваться в разрушительные соединения, именуемые реактивными формами кислорода, включая т. н. свободные радикалы (Они являются мишенью для т. н. антиоксидантных препаратов и витаминов).
Синтезированная в митохондриях АТФ – основной источник энергии для сокращения мышечных и возбуждения нервных клеток (т. к. клетки этих тканей наиболее метаболически активны, энергетически зависимы). Таким образом, нервные и мышечные клетки особенно чувствительны к дефектам митохондрий. Комбинированный эффект от потери энергии и накопления токсинов в этих клетках, надо полагать, и вызывает развитие симптомов митохондриальных миопатий и энцефаломиопатий
Клиника
Характерные признаки митохондриальных цитопатий:
•скелетные мышцы: низкая толерантность к физической нагрузке, гипотония, проксимальная миопатия, включающая фациальные и фарингеальные мышцы, офтальмопарез, птоз
•сердце: нарушения сердечного ритма, гипертрофическая миокардиопатия
•центральная нервная система: атрофия зрительного нерва, пигментная ретинопатия, миоклонус, деменция, инсультоподобные эпизоды, расстройства психики
•периферическая нервная система: аксональная нейропатия, нарушения двигательной функции гастроинтестинального тракта
•эндокринная система: диабет, гипопаратиреоидизм, нарушение экзокринной функции панкреас, низкий рост
Таким образом, типичны для митохондриальных заболеваний вовлеченность разных органов и одновременное проявление внешне не связанных между собой аномалий. Примерами служат:
1. Мигрени с мышечной слабостью
2. Наружная офтальмоплегия с нарушением проводимости сердечной мышцы и мозжечковой атаксией
3. Тошнота, рвота с оптической атрофией и кардиомиопатией
4. Низкорослость с миопатией и инсультоподобным и эпизодами
5. Экзокринная дисфункция поджелудочной железы с сидеробластной анемией
6. Энцефало- миопатия с диабетом
7. Диабет с глухотой
8. Глухота с наружной офтальмоплегией, птозом и ретинопатией
9. Задержка развития или потеря навыков и офтальмоплегия, офтальмопарез
Характер и тяжесть клинических проявлений митохондриальных болезней определяется:
• тяжестью мутации мтДНК;
• процентным содержанием мутантной мтДНК в конкретных органах и тканях;
• энергетической потребностью и функциональным резервом органов и тканей, содержащих мтДНК (их “порогом чувствительности” к дефектам окислительного фосфори лирования).
Миопатия
Основные симптомы митохондриальной миопатии – истощение мышц и их слабость, и непереносимость физических нагрузок.
У некоторых индивидов слабость наиболее выражена в мышцах, контролирующих движения глаз и век. Два наиболее частых следствия такой слабости – это постепенный паралич движения глаз (прогрессирующая наружная офтальмоплегия, ПНО), и опущение верхних век (птоз). Зачастую люди автоматически компенсируют ПНО движениями головы для того, чтобы смотреть в различных направлениях, и могут даже не подозревать о каких либо проблемах. Птоз потенциально более неприятен, поскольку может ухудшить зрение, а также придает лицу апатичное выражение, но он может быть скорректирован хирургическим путем, либо использованием специальных очков с устройством для подъема века
Митохондриальные миопатии могут также вызывать слабость других мышц лица и шеи, что приводит к заплетающейся речи и трудностям с глотанием. В этих случаях могут помочь речевая терапия (занятия с логопедом) или включение в рацион питания таких продуктов, которые легче проглатываются.
Энцефаломиопатия
Митохондриальная энцефаломиопатия, как правило, включает некоторые из вышеупомянутых симптомов миопатии, дополненными одним или несколькими неврологическими симптомами. Также как и при миопатии, наблюдается значительная вариабельность симптомов обоего типа и тяжести течения у разных индивидов.
Среди наиболее частых симптомов митохондриальной энцефаломиопатии – нарушения слуха, мигренеподобные головные боли и эпиприступы. По крайней мере, в одном синдроме головные боли и эпиприступы часто сопровождается инсультоподобными эпизодами
Дополнительно к поражению глазных мышц, митохондриальная энцефаломиопатия может поражать как сами глаза, так и участки головного мозга, ответственные за зрение. Например, потеря зрения вследствие оптической атрофии (дегенерации зрительного нерва) или ретинопатии (дегенерации некоторых клеток, выстилающих глазное дно) – обычные симптомы митохондриальной энцефаломиопатии. По сравнению с мышечными проблемами, эти эффекты с большей вероятностью приводят к серьезным нарушениям зрения
Довольно часто митохондриальная энцефаломиопатия вызывает атаксию, или сложности с балансом и координацией.
Диагностика.
Ни один из отличительных симптомов митохондриального заболевания – мышечная слабость, непереносимость нагрузок, ухудшение слуха, атаксия, эпиприступы, неспособность к обучению, катаракта, диабет и низкорослость – не является уникальным именно для такого заболевания. Однако комбинация трех или более из этих симптомов у одного индивида свидетельствует в пользу митохондриального заболевания, особенно если симптомы затрагивают более одной системы организма
Физикальное обследование обычно включает в себя тесты на силу и выносливость, такие например, как повторяющиеся сжатия-разжатия кулака, или подъем и спуск по небольшой лестнице. Неврологическое обследование может включать в себя проверку рефлексов, зрения, речи и базовых когнитивных способностей.
Существует ряд рутинных клинических методов исследования, которые можно использовать при подозрении на митохондриальную цитопатию:
•лактатный ацидоз является практически постоянным спутником митохондриальных болезней (только этот признак является недостаточным для постановки диагноза, так как он может выявляться и при других патологических состояниях; в этом отношении может быть полезным измерение уровня лактата в венозной крови после умеренной физической нагрузки, например на велоэргометре)
•ЭЭГ – данные ЭЭГ не является достаточно специфическими
Образцы мышечных биоптатов целесообразно делить на три части – одна для микроскопического исследования (гистология, гистохимия и электронная микроскопия), вторая для энзимологического и иммунологического анализа (изучение характеристик компонентов дыхательной цепи) и третья – непосредственно для молекулярно-генетического анализа. Поиск известных мутаций на мышечном материале позволяет в большинстве случаев успешно осуществлять ДНК-диагностику болезни. При отсутствии из вестных мутаций мтДНК в мышечной ткани следующим этапом является развернутый молекулярно-генетический анализ – секвенирование всей цепи мтДНК (или кандидатных генов ядерной ДНК) с целью выявления нового варианта мутации.
Лечение.
Что касается терапии митохондриальных цитопатий, то речь может идти пока только о симптоматической.
Лечение митохондриальных болезней проводится обычно по двум основным направлениям:
•предупреждение повреждения митохондриальных мембран свободными радикалами с помощью антиоксидантов (витамин Е, a-липоевая кислота) и мембранопротекторов.
В практику входят всё новые препараты комбинированного действия, такие, например, как идебенон (Нобен) – улучшенный структурный аналог коэнзима Q10, благоприятно влияющий на активность дыхательного пути и обладающий выраженным антиоксидантным, антиапоптотическим и нейротрофическим действием.
Очевидно, что расширение терапевтического арсенала при митохондриальных болезнях диктует настоятельную необходимость того, чтобы практические врачи различных специальностей (неврологи, психиатры, педиатры, генетики, гематологи и др. ) были хорошо знакомы с алгоритмом диагностики этих заболеваний.
Особенности митохондриальных заболеваний
Митохондриальные заболевания – особый класс наследственных патологий, в основе которых лежит нарушение функционирования митохондрий, клеточных структур, чьей основной функцией принято считать выработку энергии в виде АТФ путем окислительного фосфорилирования. К дефектам работы митохондрий могут приводить как мутации в ДНК самих этих органелл(мтДНК), так и мутации генов ядерной ДНК (яДНК), продукты которых задействованы в метаболизме митохондрий. Клинически, дефекты в функционировании митохондрий по-разному проявляются со стороны конкретных органов и тканей, однако, в первую очередь страдают наиболее энергозависимые ткани, коими являются нервная и мышечная. Установлено, что митохондриальные заболевания относятся к наиболее частым наследственным неврологическим расстройствам. По некоторым мутациям частота встречаемости достигает 1 на 400 человек в европейской популяции, хотя фенотипически мутация проявляется значительно реже, примерно 1 на 8000 человек [1].
Мутации митохондриальной ДНК
В настоящее время выявлено более 400 точковых мутаций мтДНК, а также различных делеций и перестроек мтДНК. Известно более 200 заболеваний, вызванных этими мутациями [2]. Для митохондриальных заболеваний свойственна клиническая и генетическая гетерогенность. Одни мутации приводят к строго определенным клиническим признакам. Так, например, мутация 11778 G→A приводит только к наследственной оптической нейропатии Лебера (LHON). Другая мутация, например 3243 A→G, вызывает огромное количество клинических проявлений, которые могут затрагивать центральную нервную систему, периферическую нервную систему, эндокринную систему, сердце, глаза, уши, желудочно-кишечный тракт, почки и кожу. Причем, все эти органы и системы органов могут поражаться как в совокупности, так и индивидуально. Третьим вариантом гетерогенности является синдром Лея, который могут вызывать около 30 мутаций мтДНК, а также мутации более чем в 20 генах ядерной ДНК, кодирующей белки биогенеза митохондрий.
Особенностью митохондриальных заболеваний, обусловленных мутациями мтДНК, является материнский тип наследования (в норме митохондрии передаются только через ооциты). Стоит отметить, однако, что митохондриальное наследование, на первый взгляд, можно спутать с X-сцепленным рецессивным наследованием – в обоих случаях болеют дети больной женщины. Разница же заключается в соотношении полов больного потомства: при митохондриальном наследовании все дети имеют равный шанс заболеть, в то время как при X-сцепленном рецессивном наследовании мутация клинически проявляется лишь у мужского пола. Отдельно стоит выделить спорадические случаи – мутация, возникшая в мтДНК de novo, также может спутать понимание характера наследования. Таким образом, анализ родословных является неотъемлемой частью постановки диагноза.
Исследование митохондриальной ДНК
В отличие от яДНК, которая представлена в большинстве клеток человека в двух копиях, мтДНК насчитывает от сотен до тысяч копий на клетку. С практической точки зрения, огромное число копий мтДНК является несомненным преимуществом при анализе структуры этой молекулы, поскольку позволяет работать с минимальным количеством имеющегося биологического материала. Другой, не менее важной особенностью, являющейся следствием многокопийности мтДНК, является феномен гетероплазмии, то есть состояние, когда в рассматриваемой системе (клетка, орган, организм) наблюдается сосуществование мутантной и нормальной мтДНК, в отличие от гомоплазмии, когда все мтДНК идентичны. Интересно, что состояние гетероплазмии является одним из критериев патогенности мутации. Величина гетероплазмии, а также распределение мутантных мтДНК в организме, во многом определяет фенотипическое проявление мутации мтДНК, на практике – клиническую картину заболевания.
Для того чтобы патогенная мутация проявилась фенотипически, количество мтДНК, содержащее эту мутацию (уровень ее гетероплазмии) должны превысить определенное критическое значение. Считается, что превышение 70% барьера приводит к клиническому проявлению той или иной патогенной мутации мтДНК, и носит название порогового эффекта. Тем не менее, определенные мутации могут иметь довольно низкий пороговый эффект, что может привести к сложностям в выявлении таких мутации некоторыми молекулярно-генетическими методами (например, ПДРФ-анализом). Таким образом, существует необходимость точной оценки количества мутантных мтДНК [2]. Следует заметить, что оценка уровня гетероплазмии уже включает детекцию мутаций, в то время как некоторые используемые в лабораторной практике методы обнаружения мутации не всегда учитывают уровень ее гетероплазмии.
Диагностика наследственного заболевания
Молекулярно-генетическое подтверждение, в идеале, является конечным этапом дифференциальной диагностики любого наследственного заболевания, однако, в случае митохондриальной патологии лишь меньше, чем в половине случаев удается обнаружить патогенную мутацию. Для установления вердикта «митохондриальное заболевание», однако, достаточно выявить «рваные красные волокна» в биоптатах скелетных мышц и повышение уровня лактата и пирувата в крови и/или ликворе (лактатный ацидоз). С другой стороны, оба этих признака сами по себе не являются специфическими для митохондриальных заболеваний. В качестве диагностического критерия может быть наличие, на первый взгляд, не связанных между собой клинических признаков. Определение активности комплексов окислительного фосфорилирования также является одним из ключевых моментов дифференциальной диагностики [3, 4].
Свои особенности имеет биохимический профиль биологических жидкостей при митохондриальных патологиях. Сразу стоит отметить, что лабораторная диагностика митохондриальных заболеваний – это подчас весьма специфические исследования, которые может позволить себе не каждая лаборатория. В плазме и спинномозговой жидкости выявляют повышенный уровень таких аминокислот как аланин, глицин, пролин, саркозин и тирозин. Со стороны органических кислот наблюдаются следующая картина: повышен уровень компонентов цикла трикарбоновых кислот, этилмалоновой кислоты, 3-метилглутаконовой кислоты и бикарбоновых кислот. В крови наблюдается снижение уровня общего карнитина.
Возможно ли лечение?
Несмотря на значительный прогресс диагностике и понимании молекулярного патогенеза данного класса заболеваний, к настоящему времени, митохондриальные заболевания остаются неизлечимы. Используемые в клинической практике стратегии симптоматического лечения включают применение фармакологических средств, специальных диет, а также физических нагрузок. В некоторых случаях применяется хирургическое вмешательство. Также в настоящее время разрабатываются различные экспериментальные подходы, направленные на устранение дефектов дыхательной цепи митохондрий на молекулярном уровне [2, 5].
На сегодняшний день наиболее приемлемым методом предотвращения митохондриального заболевания остается предотвращение передачи мутантных генов следующему поколению [6]. Основными стратегиями предотвращения передачи дефектов генетического материала потомству принято считать пренатальную диагностику (ПНД) и преимплантационную генетическую диагностику (ПГД). Для мутаций ядерного генома такие процедуры считаются приемлемыми. Применение же подобных процедур к дефектам митохондриального генома имеет известные ограничения. Главным образом для большинства мутаций мтДНК это связано с плохой корреляцией между уровнем гетероплазмии и тяжестью заболевания, неравномерным распределением мутантной ДНК в тканях организма, и изменением уровня гетероплазмии в течение жизни человека [7].
Список литературы:
1. Turnbull H.E., Lax N.Z., Diodato D., Ansorge O., Turnbull D.M. The mitochondrial brain: From mitochondrial genome to neurodegeneration // Biochim. Biophys. Acta. 2010. V. 1802. P. 111–121.
2. Мазунин И.О., Володько Н.В., Стариковская Е.Б., Сукерник Р.И. Митохондриальный геном и митохондриальные заболевания человека // Мол. Биол. 2010. Т. 44. №. 5. С. 755– 772.
3. Иллариошкин С.Н. Алгоритм диагностики митохондриальных энцефаломиопатий // Атмосфера. Нервные болезни. 2007. Т. 3. С. 23–27.
4. Haas R.H., Parikh S., Falk M.J., Saneto R.P., Wolf N.I., Darin N., Wong L.J., Cohen B.H., Naviaux R.K. The in-depth evaluation of suspected mitochondrial disease // Mol. Genet. Metab. 2008. V. 94. P. 16–37.
5. Finsterer J. Treatment of mitochondrial disorders // Eur. J. Paediatr. Neurol. 2010. V. 14. P. 29–44.
6. Мазунин И.О., Володько Н.В. Митохондрии: жизнь в клетке и ее последствия // ПРИРОДА. 2010. № 10. С. 3–14.